
����Ŀ����CoCO3Ϊԭ�ϲ�����ˮ�ȷ��ͳ���ˮ�ȷ������Ƶ�H2O2�ֽ�ĸ�Ч����CoxNi��1-x��Fe2O4������Co��Ni��Ϊ+2�ۣ�����ͼ�������ֲ�ͬ�����Ƶõ�CoxNi��1-x��Fe2O4��10��ʱ���ֽ�6%��H2O2��Һ����Գ�ʼ������x�仯���ߡ�����˵������ȷ���ǣ�������
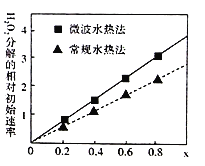
A.��ͼ����Ϣ����֪����ˮ�ȷ���ȡ�Ĵ������Ը��ߣ�Co2+�Ĵ�Ч������
B.��ЭͬCuO������H2O2��ȥ��̬�����������£�1molH2O2��NH3����ΪN2ת�Ƶ���Ϊ2mol
C.������0.1moL/L��ˮ��Һ��pH=a������Һϡ�͵�ԭ�����10��������ʹ��ҺpH=��a-1��
D.��֪����CoCO3ʱ���¶Ȳ�ͬ�����ﲻͬ����400��������CoCO3���õ����������������2.41g��CO2�����Ϊ0.672L������£������ʱ���ù���������Ļ�ѧʽΪCo3O4
���𰸡�A
��������
A����ͼ��֪��ˮ�ȷ���Ӧ��H2O2��Һ����Գ�ʼ���ʴ���������Ը��ߣ�Co2+�Ĵ�Ч�����ã���A����
B��H2O2��NH3����ΪN2��NԪ�صĻ��ϼ����ߣ���OԪ�صĻ��ϼ���-1�۽���Ϊ-2�ۣ���1mol H2O2��NH3����ΪN2ת�Ƶ���Ϊ1mol��2��[(-1)-(-2)]=2mol����B��ȷ��
C.0.1moL/L��ˮ��Һ��pH=a������Һϡ�͵�ԭ�����10����pH��С����ϡ�ʹٽ�һˮ�ϰ��ĵ��룬����Һ��pH��a-1����C��ȷ��
D����400��������CoCO3���õ����������������2.41g��CO2�����Ϊ0.672L(�����)��n(CO2)=n(CoCO3)=![]() =0.03mol�����������к�n(O)=
=0.03mol�����������к�n(O)=![]() =0.04mol��n(Co):n(O)=3:4�����ù���������Ļ�ѧʽΪCo3O4����D��ȷ��
=0.04mol��n(Co):n(O)=3:4�����ù���������Ļ�ѧʽΪCo3O4����D��ȷ��
�ʴ�ΪA��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮ�ĵ���ƽ����������ͼ��ʾ������˵���У���ȷ����
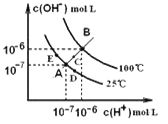
A. ͼ��A��B��D���㴦KW��Ĺ�ϵ�� B>A>D
B. 100������pH=2��ϡ��������μ�������pH=10��ϡ��ˮ����Һ�� c(NH4+)��c(NH3��H2O)��С����ַ�Ӧ����Һ����B��
C. �¶Ȳ��䣬��ˮ�м�������NH4Cl���壬�ɴ�A��仯��C��
D. ����Ũ��A����ʾ��Һ���ɴ�A��仯��B��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о������� FeCl3 ��Һ����ɫ��Ӧ��ʵ�����£�
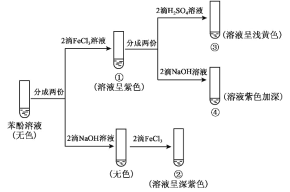
����˵������ȷ����( )
A.�����������ᣬ���뷽��ʽΪ![]()
![]() +H+
+H+
B.���Թܢ��еμ���������������Һ��ɫ��Ϊdz��ɫ
C.�ԱȢ٢��е�����˵�����μ�ϡ�����c(Fe3+)��С
D.�ԱȢ٢ڡ��٢��е�����˵����ɫ���ʵ���������Һ��c(![]() )���
)���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(NaClO2)��һ��ǿ������Ư�����㷺���ڷ�֯��ӡȾ��ʳƷ��ҵ�����ڼ��Ի������ȶ����ڡ�ijͬѧ�������Ϻ��������NaClO2����Ҫ�������£�
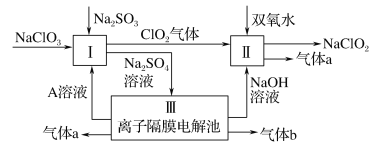
��1�����з�����Ӧ�Ļ�ԭ����____ (�ѧʽ)��
��2�����з�Ӧ�����ӷ���ʽ��____��
��3���������Ӹ�Ĥ���ص�װ�����£�
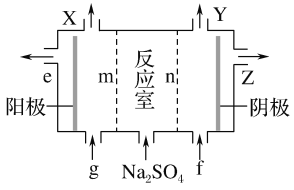
��A�Ļ�ѧʽ��________��A��____�ڲ�����
��mΪ____ (����������������)���ӽ���Ĥ��
�۽�ϻ�ѧ���������˵������NaOH������ԭ��________
��4��ClO2��һ�ָ�Чˮ�������������������ƺ�ϡ����Ϊԭ���Ʊ���5NaClO2��4HCl=5NaCl��4ClO2����2H2O
�ٸ÷�Ӧ���������ͻ�ԭ�������ʵ���֮����____��
���о�����������Ӧ��ʼʱ����Ũ��Խ�������������Cl2�ĺ���Խ������������ԭ��Ӧ���ɷ�����ԭ����____��
��5��NaClO2���ʿɷֽ�ΪNaClO3��NaCl��ȡ����������ǰ���NaClO2�����������Һ���ֱ�������FeSO4��Һ��Ӧʱ������Fe2�������ʵ���ǰ��____ (����>����<����������)���ߡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭ����ѧ����ѧ�ۺ��������õĺϽ𣬹㷺Ӧ�������������Ԫ���������Ǵ�ij�Ͼ��ͭԪ������BeO25%��CuS71%������FeS��SiO2���л������ͭ���ֽ��������̡�
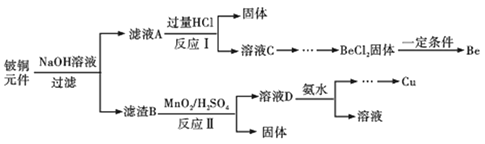
��֪��
���롢��Ԫ�ش������ڱ��еĶԽ���λ�ã���ѧ��������
�����£�Ksp[Cu��OH��2]=2.2��10-20��Ksp[Fe��OH��3]=4.0��10-38��Ksp[Mn��OH��2]=2.1��10-13
(1)����B����Ҫ�ɷ�Ϊ______���ѧʽ����
(2)д����Ӧ���к��뻯������������ᷴӦ�Ļ�ѧ����ʽ______��
(3)MnO2�ܽ����������е���Ԫ������Ϊ������д����Ӧ����CuS������Ӧ�����ӷ���ʽ______������ŨHNO3�ܽ��������ȱ����______����дһ������
(4)��BeCl2��Һ�еõ�BeCl2����IJ�����______��
(5)��ҺD�к�c��Cu2+��=2.2molL-1��c��Fe3+��=0.008molL-1��c��Mn2+��=0.01molL-1����μ���ϡ��ˮ����pH�����η������ȳ�������______�������ӷ��ţ���Ϊʹͭ���ӿ�ʼ������������Ӧ������Һ��pH����______��
(6)ȡ��ͭԪ��1000g�����ջ��Be������Ϊ72g����Be�IJ�����______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����SO2��O2�Ʊ�SO3���۵�16.8�棬�е�44.8�棩��ģ��װ������ͼ��ʾ�������Ⱥͼг�װ��ʡ�ԣ���

����˵����ȷ����
A. װ�â��е��Լ�Ϊ����NaHSO3��Һ
B. ʵ���ҿ���ͭ��ϡ�����ڼ�����������ȡSO2
C. �b�â۷�Ӧ���еIJ�ʯ��������Ӧ�Ĵ���
D. ��װ�â��ݳ��������й�����SO2��O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ��H2SO3HSO3����H���ĵ��볣��Ka��1��10��2������¶���NaHSO3��ˮ��ƽ�ⳣ��Kh��____________������NaHSO3��Һ�м���������I2������Һ��![]() ��__________(��������������С������������)��
��__________(��������������������������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й���Һ���������ʵ���Ũ�ȵĹ�ϵ����ȷ����
A.0.1 mol��L��1��NH4Cl��Һ��0.05 mol��L��1��NaOH��Һ�������ϵ���Һ��c(Cl��)>c(Na��)>c(![]() )>c(OH��)>c(H��)
)>c(OH��)>c(H��)
B.�����ʵ�����NaClO��NaHCO3�����Һ��c(HClO)��c(ClO-)��c(HCO3-)��c(H2CO3)��c(![]() )
)
C.pH��2��HA��Һ��pH��12��MOH��Һ�������ϣ�c(M��)��c(A��)>c(OH��)��c(H��)
D.ij��Ԫ�������ʽ��NaHA��Һ��c(OH��)��c(H2A)��c(H��)��2c(A2��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ����������(��Ҫ�ɷ�ΪAl2O3����Fe2O3����)Ϊԭ��ұ�����Ĺ����������£�
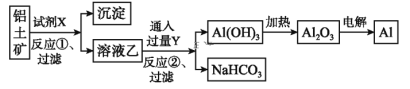
����������ȷ����(����)
A. �Լ�X����������������Һ��Ҳ����������
B. ��Ӧ�ٹ��˺����ó���Ϊ��������
C. ͼ����ʾת����Ӧ������������ԭ��Ӧ
D. ��Ӧ�ڵĻ�ѧ����ʽΪNaAlO2+CO2+2H2O=Al(OH)3��+NaHCO3
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com