
【题目】4.35g二氧化锰与浓盐酸(密度为1.19gcm﹣3、质量分数为36.5%)完全反应.求:
(1)浓盐酸的物质的量浓度为多少?_______
(2)将所得气体全部用石灰乳吸收,可得到漂白粉的质量.________
【答案】11.9mol/L 6.35g
【解析】
(1)根据c=![]() 计算盐酸的物质的量浓度;
计算盐酸的物质的量浓度;
(2)漂白粉的成分是氯化钙、次氯酸钙,利用生成氯气的物质的量,根据方程式计算生成的氯化钙、次氯酸钙的物质的量。
(1)密度为1.19gcm﹣3、质量分数为36.5%浓盐酸的物质的量浓度为![]() mol/L=11.9mol/L;
mol/L=11.9mol/L;
(2)4.35g二氧化锰的物质的量为0.05mol,则:
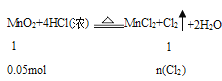
故n(Cl2)=0.05mol,用石灰乳吸收,则:
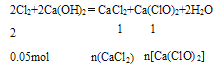
所以n(CaCl2)=n[Ca(ClO)2]=0.05mol×![]() =0.025mol,故可得漂白粉的质量为:0.025mol×111g/mol+0.025mol×143g/mol=6.35g。
=0.025mol,故可得漂白粉的质量为:0.025mol×111g/mol+0.025mol×143g/mol=6.35g。


科目:高中化学 来源: 题型:
【题目】铍及其化合物的应用正日益被重视。在周期表中,同一主族元素化学性质相似。目前也发现有些元素的化学性质和它在周期表中左上方或右下方的另一主族元素性质相似,这称为对角线规则。据此请回答:
(1)锂在空气中燃烧,除生成Li2O外,也生成微量的_________(填化学式)。
(2)铍的最高价氧化物对应的水化物属两性化合物,证明这一结论的有关离子方程式为_______________________________________________________________。
(3)氯化铍在气态时存在BeCl2分子(a)和二聚分子(BeCl2)2(b),a属于________(填“离子”或“共价”)化合物,写出它的一个等电子体_________。
(4)二聚分子(BeCl2)2中Be原子的杂化方式相同,且所有原子都在同一平面上。b 的结构式为__________(标出配位键)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】螺环化合物具有抗菌活性,用其制成的药物不易产生抗药性,螺[3,4]辛烷的结构如图,下列有关螺[3,4]辛烷的说法正确的是( )

A. 分子式为C8H16B. 分子中所有碳原子共平面
C. 与2—甲基—3—庚烯互为同分异构体D. 一氯代物有4种结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按要求作答:
(1)分子式为C4H8且属于烯烃的有机物的同分异构体(考虑顺反异构)有 _________种;![]() 高聚物的单体的结构简式是_____________ 和______________。
高聚物的单体的结构简式是_____________ 和______________。
(2) ![]() 的名称为:_______________;写出
的名称为:_______________;写出![]() 聚合生成高分子化合物的化学方程式________;
聚合生成高分子化合物的化学方程式________;
(3)已知-NH2表现碱性,-NO2表现中性,-COOH表现酸性。化学式为C7H7NO2的有机物,其分子结构中有1个苯环、2个取代基,试按照下列写出2种同分异构体(只写邻位即可)。
①该有机物既有酸性又有碱性______________。
②该有机物既无酸性又无碱性______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《必修1》中学习过:A过滤、B蒸发(结晶)、C蒸馏、D分液、E萃取、F配制一定物质的量浓度的溶液,根据所学的知识回答下列下列问题:
(1)选用适当的方法分离或提纯,应选用上述哪一种?(填序号)
①除去 NaCl 溶液中所含的少量 KNO3__________;
②从碘水中提取碘__________;
③用自来水制取蒸馏水__________;
④分离植物油和水__________;
(2)除过滤、蒸发(结晶)外还有_____实验用到了玻璃棒。需要加热的实验有蒸发(结晶)和__________;填序号)。
(3)图是硫酸试剂瓶标签上的内容。实验室用该硫酸配制240mL0.46mol/L的稀硫酸,则

a.需量取该硫酸的体积为__________mL;
b.有以下仪器:①烧杯 ②100mL量筒 ③250mL容量瓶④500mL容量瓶 ⑤玻璃棒 ⑥托盘天平(带砝码)⑦10mL量筒⑧胶头滴管,配制过程中,必须使用的仪器是_____(填代号);
(4)该同学实际配制得到的浓度为0.47mol/L,可能的原因是_______________
A.量取浓H2SO4时仰视刻度 B.容量瓶洗净后未经干燥处理
C.没有将洗涤液转入容量瓶 D.定容时仰视刻度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z在元素周期表中的相对位置如表所示,这四种元素的原子最外层电子数之和为21.则下列说法不正确的是
X | Y | ||
W | Z |
A.原子半径大小:![]()
B.W、Z的最高价氧化物的水化物的酸性,Z强于W
C.可用W与X的氧化物反应来制备X
D.Y与氢元素可以形成原子个数比为1:1的化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烷烃A(MA = 86)只有三种一氯取代产物B、C和D, B和D分别与强碱的醇溶液共热,都只能得到有机化合物E。以上反应及B的进一步反应如图所示。
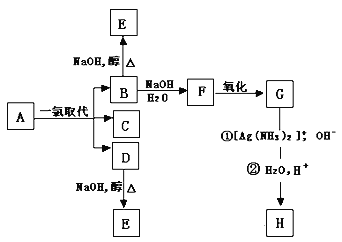
(1)A的结构简式是_____ E的结构简式是_____ F所含官能团名称是_____H所含官能团结构简式是_____
(2)A—B、C、D的反应条件_____
(3)B转变为E的反应属于_____(填反应类型名称)G转变为H的反应属于_____(填反应类型名称)
(4)B—F的化学方程式是 _____ F与H在浓H2SO4存在下加热所发生反应的化学方程式_____该反应属于_____(填反应类型名称)
(5)写出G的同系物中碳原子数最少的有机物与新制氢氧化铜在加热条件下发生的反应化学方程式:_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式及有关应用的叙述中,正确的是
A. 甲烷的燃烧热为890.3kJmol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+ 2O2(g) ═ CO2(g) + 2H2O(g) △H = -890.3kJmol-1
B. 已知强酸与强碱在稀溶液里反应的中和热为57.3kJmol-1,则![]() H2SO4(aq)+
H2SO4(aq)+![]() Ba(OH)2(aq)═
Ba(OH)2(aq)═![]() BaSO4(s)+H2O(l) △H < -57.3kJmol-1
BaSO4(s)+H2O(l) △H < -57.3kJmol-1
C. 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g) + 3H2(g)![]() 2NH3(g) △H = -38.6kJmol-1
2NH3(g) △H = -38.6kJmol-1
D. 已知25℃、101KPa条件下:4Al(s) + 3O2(g) ═ 2A12O3(s) △H = -2834.9kJmol-1,4Al(s) + 2O3(g) ═ 2A12O3(s) △H = -3119.1kJmol-1,则O3比O2稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将O2、CH4、Na2O2置于密闭容器中,在250℃下用电火花引发化学反应。反应停止后使容器内恢复至250℃,容器内的气压为零。由此得出的结论正确的是( )
A. 原O2、CH4、Na2O2物质的量之比为1∶2∶6,反应后容器内生成的固体是Na2CO3和NaHCO3
B. 原O2、CH4、Na2O2物质的量之比为2∶1∶4,反应后容器内生成的固体是Na2CO3和NaOH
C. 原O2、CH4、Na2O2物质的量之比为1∶2∶6,反应后容器内生成的固体是Na2CO3和NaOH
D. 原O2、CH4、Na2O2物质的量之比为2∶1∶4,反应后容器内生成的固体是NaHCO3和NaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com