
【题目】在相同的密闭容器中,不同温度下发生反应:2A(g)![]() 2B(g)+C(g) ΔH>0,气体A的浓度随时间t变化如下表所示。
2B(g)+C(g) ΔH>0,气体A的浓度随时间t变化如下表所示。
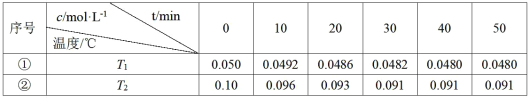
下列说法不正确的是( )
A.实验的温度:T2>T1
B.实验①前20min的平均反应速率v(C)=3.5×10-5molL-1min-1
C.实验②比实验①提前10min达到平衡
D.实验②中A的平衡转化率为9%
【答案】C
【解析】
A. 在相同的密闭容器中,根据反应,实验①中,A平衡是浓度为0.048mol/L,B平衡浓度为0.002mol/L,C平衡浓度为0.001mol/L,平衡常数=![]() 。同理,实验②中A平衡是浓度为0.091mol/L,B平衡浓度为0.009mol/L,C平衡浓度为0.00045mol/L,平衡常数=
。同理,实验②中A平衡是浓度为0.091mol/L,B平衡浓度为0.009mol/L,C平衡浓度为0.00045mol/L,平衡常数=![]() ,由于反应为吸热反应,温度越高,平衡正向进行的程度越大,平衡常数越大,故实验的温度T2>T1,由化学反应速率的大小关系也可以得到这个结论,A正确;
,由于反应为吸热反应,温度越高,平衡正向进行的程度越大,平衡常数越大,故实验的温度T2>T1,由化学反应速率的大小关系也可以得到这个结论,A正确;
B. 实验①前20min的平均反应速率![]() ,B正确;
,B正确;
C. 实验②在30min时已平衡,实验①在40min时已平衡,但是由于记数间隔是10min,无法判断具体的平衡时间, C不正确;
D. 实验②中,平衡是A的浓度为0.091mol/L,平衡转化量=0.091 mol/L -0.10 mol/L =0.009 mol/L ,![]() ,D正确。
,D正确。
本题选不正确的,故答案选C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】据预测,到2040年我国煤炭消费仍将占能源结构的三分之一左右。H2S在催化活性碳(AC)表面的迁移,对煤的清洁和综合应用起了很大的促进作用,其机理如图所示,其中ad表示物种的吸附状态。下列有关叙述错误的是

A.图中阴影部分表示H2S分子的吸附与离解
B.AC表面作用的温度不同,H2S的去除率不同
C.H2S在AC表面作用生成的产物有H2O、H2、S、SO2、CS2等
D.图中反应过程中只有H—S键的断裂,没有H—S键的形成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】多巴胺是一种重要的中枢神经传导物质,用来帮助细胞传送脉冲的化学物质,能影
响人对事物的欢愉感受。多巴胺可用香兰素与硝基甲烷等为原料按下列路线合成:
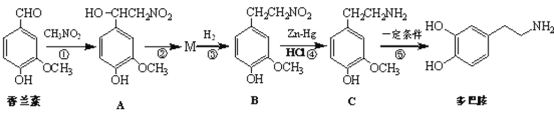
(1)香兰素保存不当往往会导致颜色、气味发生明显变化,其原因是___。
(2)多巴胺中的官能团的名称是___、___,反应①、⑤的反应类型分别为___、___。
(3)写出由A→M的化学方程式___。
(4)写出同时满足下列条件的B的一种同分异构体的结构简式:___。
①具有天然氨基酸的共同结构
②能与FeCl3溶液发生显色反应
③有6种不同化学环境的氢原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置不能达到实验目的的是
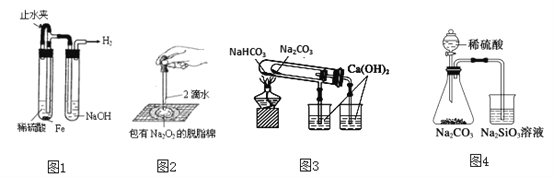
A. 图1:制备并观察氢氧化亚铁
B. 图2:证明过氧化钠与水反应放热
C. 图3:验证NaHCO3和Na2CO3的热稳定性
D. 图4:验证酸性强弱H2SO4>H2CO3>H2SiO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某二次电池装置如图所示,锂、充有催化剂的碳纳米管为电极,电解质能传导Li+。放电时生成的Li2CO3和C附着在电极上,充电时可使Li2CO3转化为Li、CO2和O2。下列说法不正确的是( )
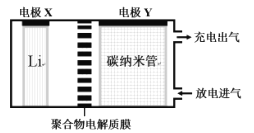
A.放电时,电流从电极Y经外电路流向电极X
B.充电时,电极X接外电源的正极发生氧化反应
C.充电时,电极Y的电极反应式为2Li2CO3-4e-=2CO2↑+O2↑+4Li+
D.应用该电池电镀铜,若析出64gCu,理论上消耗标况下33.6LCO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与人类生活密切相关。请按要求回答下列问题:
(1)K2FeO4是一种重要的净水剂,可用下列方法制得:2Fe(OH)3 +3Cl2 +10KOH![]() 2K2FeO4+6KCl+8H2O。在该反应中,还原剂是_____,当反应中有0.5mol K2FeO4生成时,消耗Cl2在标况下的体积为_________,转移电子的数目为_____。
2K2FeO4+6KCl+8H2O。在该反应中,还原剂是_____,当反应中有0.5mol K2FeO4生成时,消耗Cl2在标况下的体积为_________,转移电子的数目为_____。
(2)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式__________。
(3)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:___________。
(4)工业上制漂白粉的化学方程式为_______________________________,新制氯水在阳光照射下产生无色气体,该反应的化学方程式是______。
(5)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:_____________________。若向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是________。
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)比较给出H+的能力的相对强弱:H2CO3___C6H5OH(填“>”、“<”或“=”);用一个离子方程式说明CO32和C6H5O结合H+能力的相对强弱___。
(2)Ca(CN)2是离子化合物,各原子均满足8电子稳定结构。写出Ca(CN)2的电子式___。
(3)常压下,水晶的硬度比晶体硅的硬度大,其主要原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2.0molPCl3和1.0molCl2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3(g)+Cl2(g)PCl5(g)达平衡时,PCl5为0.4mol,如果此时移走1.0molPCl3和0.50molCl2,在相同温度下再达平衡时PCl5的物质的量是( )
A. 0.4mol
B. 0.2mol
C. 小于0.2mol
D. 大于0.2mol,小于0.4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯和溴的取代反应的实验装置如图所示。其中A为带支管的试管改成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入铁屑粉少量。

(1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应。写出A中所发生反应的化学方程式:____________、____________;试管C中苯的作用____________。
(2)反应开始后,D、E试管的现象分别为__________________、____________; E中所发生反应的离子方程式为____________。
(3)在上述整套装置中,具有防倒吸作用的仪器有(填字母) ____________。
(4)上述实验装置除①步骤简单,操作方便,成功率高;②各步现象明显;③对产品便于观察这3个优点外,还有一个优点____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com