
【题目】(1)比较给出H+的能力的相对强弱:H2CO3___C6H5OH(填“>”、“<”或“=”);用一个离子方程式说明CO32和C6H5O结合H+能力的相对强弱___。
(2)Ca(CN)2是离子化合物,各原子均满足8电子稳定结构。写出Ca(CN)2的电子式___。
(3)常压下,水晶的硬度比晶体硅的硬度大,其主要原因是___。
【答案】> C6H5OH+CO32-=HCO3-+C6H5O- ![]() 或
或![]() 两者都为原子晶体,氧原子半径比硅原子半径小,水晶中Si-O键比晶体硅中Si—Si更牢固
两者都为原子晶体,氧原子半径比硅原子半径小,水晶中Si-O键比晶体硅中Si—Si更牢固
【解析】
(1)H2CO3中羟基氢比乙醇中的羟基氢活泼,则H2CO3给出H+的能力比乙醇要强,由反应C6H5OH+CO32-=HCO3-+C6H5O-可说明CO32强于C6H5O结合H+能力,故答案为:>;C6H5OH+CO32-=HCO3-+C6H5O-;
(2)Ca核外电子为:2、8、8、2,失去两个电子为Ca2+;C最外层4个电子,碳原子和氮原子共用3电子对,一个碳周围就有7个电子,得到2电子达稳定结构,所以Ca(CN)2的电子式为![]() 或
或![]() ,故答案为:
,故答案为:![]() 或
或![]() ;
;
(3)水晶的主要成分是SiO2,晶体硅是硅单质,因为两者都为原子晶体,氧原子半径比硅原子半径小,所以水晶中Si-O键比晶体硅中Si—Si更牢固,水晶硬度更大,故答案为:两者都为原子晶体,氧原子半径比硅原子半径小,石英中Si-O键比晶体硅中Si—Si更牢固。


 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源: 题型:
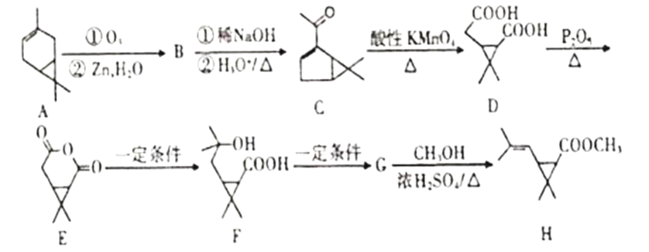
【题目】利用蒈烯(A)为原料可制得杀虫剂菊酯(H),其合成路线可表示如图。
已知①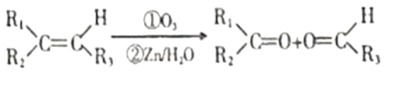
②R1CHO+R2CH2CHO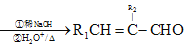 +H2O
+H2O
(1)A的分子式为___。
(2)B的结构简式___。
(3)C中含氧官能团名称为___。
(4)由D生成E,F生成G的反应类型分别是____和_____。
(5)写出由G生成H的化学方程式为____。
(6)满足下列条件D的同分异构体有___种。(不考虑立体异构)
①1molD与碳酸氢钠溶液反应生成标准状况下22.4LCO2气体;
②D分子与稀硫酸共热可水解生成异丙醇;
③该化合物能使溴水褪色。
(7)写出以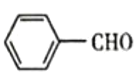 和CH3CH2OH为原料制备
和CH3CH2OH为原料制备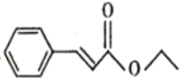 的合成路线流程图(无机试剂任用)___。
的合成路线流程图(无机试剂任用)___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.35Cl和37Cl互为同位素
B.乙酸和油酸(C17H33COOH)互为同系物
C.红磷和白磷互为同素异形体
D.乙醛和环氧乙烷(![]() )互为同分异构体
)互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在相同的密闭容器中,不同温度下发生反应:2A(g)![]() 2B(g)+C(g) ΔH>0,气体A的浓度随时间t变化如下表所示。
2B(g)+C(g) ΔH>0,气体A的浓度随时间t变化如下表所示。
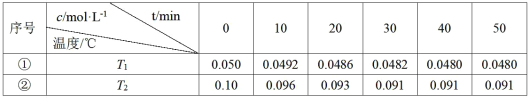
下列说法不正确的是( )
A.实验的温度:T2>T1
B.实验①前20min的平均反应速率v(C)=3.5×10-5molL-1min-1
C.实验②比实验①提前10min达到平衡
D.实验②中A的平衡转化率为9%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体X可能含有Na2O2、Fe2O3、Al2O3、SiO2、K2SO4、Na2SO3、NH4NO3、MgCl2中的一种或几种物质,进行如下实验以确定其组成:
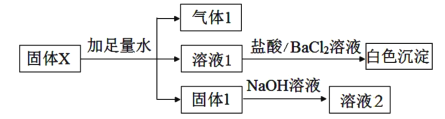
下列说法不正确的是( )
A.溶液1中不可能含有Cl-
B.气体1可能是二种气体的混合物
C.固体1可能是二种固体的混合物
D.固体X中,K2SO4和Na2SO3两种物质至少含一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定二氯化一氯五氨合钴([Co(NH3)5Cl]Cl2,摩尔质量用M表示)样品的纯度,将mg样品分为10等份,取其中一份于强碱溶液中,加热煮沸,蒸出所有氨气,用V1mLc1molL1稀硫酸充分吸收,吸收后的溶液用c2molL1NaOH中和,平均消耗NaOH溶液的体积为V2mL。
(1)该样品中[Co(NH3)5Cl]Cl2的纯度为___;
(2)写出简要计算过程:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中华人民共和国国家标准(G2762011)规定葡萄酒中c最大使用量为0.25g/L.某兴趣小组用图装置(夹持装置略)收集某葡萄酒中SO2,并对含量进行测定。
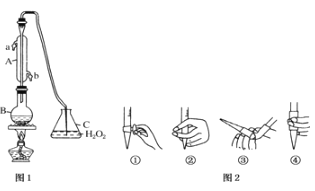
(1)仪器A的名称是________,水通入A的进口为_______________
(2)B中加入300.0ml葡萄酒和适量盐酸,加热使SO2全部逸出与C中H2O2完全反应其化学方程式为_________________________________
(3)除去C中过量的H2O2,然后用0.0900mol/LNaOH标准溶液进行滴定,滴定前排气泡时,应选择图2中的________;若滴定终点时溶液的pH=8.8,则选择的指示剂为________;若用50mL滴定管进行实验,当滴定管中的液面在刻度“20”处,则管内液体的体积______(填序号)
(①=20mL,②=30mL,③<20mL,④>30mL).
(4)滴定至终点时,消耗NaOH溶液12.50mL,该葡萄酒中SO2含量为:___g/L
(5)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案合理的是________
A.配制银氨溶液:在一定量![]() 溶液中,滴加氨水至沉淀恰好溶解
溶液中,滴加氨水至沉淀恰好溶解
B.检验RX中的卤素原子,把RX与烧碱水溶液混合加热后,将溶液冷却再加入硝酸银溶液
C.无水乙醇和浓硫酸共热至170℃,将制得的气体通入酸性高锰酸钾溶液,可检验制得的气体是否为乙烯
D.实验室制取乙烯时,必须将温度计的水银球插入反应液中,测定反应液的温度
E.乙烷中混有乙烯,通过氢气在一定条件下反应,使乙烯转化为乙烷
F.用氨水清洗做过银镜反应的试管
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com