
【题目】某固体X可能含有Na2O2、Fe2O3、Al2O3、SiO2、K2SO4、Na2SO3、NH4NO3、MgCl2中的一种或几种物质,进行如下实验以确定其组成:
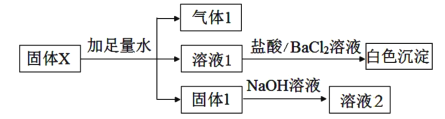
下列说法不正确的是( )
A.溶液1中不可能含有Cl-
B.气体1可能是二种气体的混合物
C.固体1可能是二种固体的混合物
D.固体X中,K2SO4和Na2SO3两种物质至少含一种
【答案】D
【解析】
固体X可能含有Na2O2、Fe2O3、Al2O3、SiO2、K2SO4、Na2SO3、NH4NO3、MgCl2中的一种或几种物质,Fe2O3、Al2O3、SiO2都难溶于水且与水不反应,K2SO4、Na2SO3、NH4NO3、MgCl2都为溶于水的盐;加入足量水,有气体1产生,则X中一定含有Na2O2,Na2O2与水的反应为2Na2O2+2H2O=4NaOH+O2↑,过氧化钠与水反应放热;
A.因为MgCl2与NaOH反应生成Mg(OH)2沉淀和NaCl,Mg(OH)2不溶于NaOH溶液,而固体X中加入足量水得到的固体1能与NaOH溶液反应得到溶液2,故固体1中不含Mg(OH)2,X中不含MgCl2,溶液1中不可能含Cl-,A正确;
B.若X中还含有NH4NO3,则固体X加入足量水后还会发生反应:NH4NO3+NaOH![]() NaNO3+NH3↑+H2O,气体1可能是O2、NH3的混合物,B正确;
NaNO3+NH3↑+H2O,气体1可能是O2、NH3的混合物,B正确;
C.若X中还同时含有Al2O3、SiO2,X与足量水反应后可能溶解部分Al2O3、SiO2,还有未溶解的Al2O3、SiO2在固体1中,Al2O3、SiO2都能溶于NaOH溶液,C正确;
D.溶液1中加入盐酸/BaCl2溶液产生白色沉淀,溶液1中可能含SO42-、SiO32-等,即溶液1中不一定含SO42-,则原固体X中不一定含有K2SO4、Na2SO3,D错误;
答案选D。


科目:高中化学 来源: 题型:
【题目】下列有机化学方程式书写正确的是( )
A. CH4+Cl2![]() CH2Cl2+H2
CH2Cl2+H2
B. H2C=CH2+Br2→CH3CHBr2
C. 2CH3CH2OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
D. CH3CH2OH+CH3COOH![]() CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸是极其重要的化工原料,在工业、农业、医药、军事等领域应用广泛。工业上通常用接触法制硫酸,主要原料是硫铁矿和空气。接触法制硫酸的生产过程大致可分为三个阶段:二氧化硫的制取和净化;二氧化硫转化为三氧化硫;三氧化硫的吸收和硫酸的生成。为了防止环境污染并对尾气进行综合利用,硫酸厂常用氨水吸收尾气的SO2、SO3等气体,再向吸收液中加入浓硫酸,以制取高浓度的SO2及(NH4)2SO4和NH4HSO4固体。为了测定上述(NH4)2SO4和NH4HSO4固体混合物的组成,现称取该样品四份,分别加入相同浓度的NaOH溶液50.00mL,加热至120℃左右,使氨气全部逸出[(NH4)2SO4和NH4HSO4的分解温度均高于200℃],测得有关实验数据如下(标准状况):
实验 | 样品的质量/g | NaOH溶液的体积/mL | 氨气的体积/L(标准状况) |
1 | 7.24 | 50.00 | 1.792 |
2 | 14.48 | 50.00 | 3.584 |
3 | 21.72 | 50.00 | 4.032 |
4 | 36.20 | 50.00 | 2.240 |
(1)由1组数据直接推测:1.81g样品进行同样实验时,生成氨气的体积(标准状况)为___L。
(2)试计算该混合物中(NH4)2SO4和 NH4HSO4的物质的量之比为___。
(3)求所用NaOH溶液的物质的量浓度___mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某二次电池装置如图所示,锂、充有催化剂的碳纳米管为电极,电解质能传导Li+。放电时生成的Li2CO3和C附着在电极上,充电时可使Li2CO3转化为Li、CO2和O2。下列说法不正确的是( )
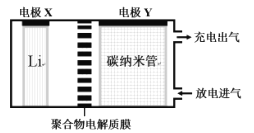
A.放电时,电流从电极Y经外电路流向电极X
B.充电时,电极X接外电源的正极发生氧化反应
C.充电时,电极Y的电极反应式为2Li2CO3-4e-=2CO2↑+O2↑+4Li+
D.应用该电池电镀铜,若析出64gCu,理论上消耗标况下33.6LCO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A转化为C和D分步进行:①A(g)![]() B(g)+2D(g)②B(g)
B(g)+2D(g)②B(g)![]() C(g)+D(g),其反应过程能量如图所示,下列说法正确的是( )
C(g)+D(g),其反应过程能量如图所示,下列说法正确的是( )
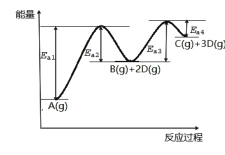
A.1molA(g)的能量低于1molB(g)的能量
B.B(g)![]() C(g)+D(g) ΔH=Ea4-Ea3
C(g)+D(g) ΔH=Ea4-Ea3
C.断裂1molA(g)化学键吸收的热量小于形成1molC(g)和3molD(g)化学键所放出的热量
D.反应过程中,由于Ea3<Ea1,反应②速率大于反应①,气体B很难大量积累
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)比较给出H+的能力的相对强弱:H2CO3___C6H5OH(填“>”、“<”或“=”);用一个离子方程式说明CO32和C6H5O结合H+能力的相对强弱___。
(2)Ca(CN)2是离子化合物,各原子均满足8电子稳定结构。写出Ca(CN)2的电子式___。
(3)常压下,水晶的硬度比晶体硅的硬度大,其主要原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,不能用勒夏特列原理解释的是
A. 红棕色的NO2,加压后颜色先变深后变浅
B. 高压比常压有利于合成SO3的反应
C. 加入催化剂有利于氨的合成
D. 工业制取金属钾Na(l)+KCl(l)![]() NaCl(l)+K(g)选取适宜的温度,使K变成蒸气从反应混合物中分离出来
NaCl(l)+K(g)选取适宜的温度,使K变成蒸气从反应混合物中分离出来
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将某一元酸HA和NaOH溶液等体积混合,分别进行编号为①②③
实验编号 | HA物质的量浓度/mol L-1 | NaOH物质的量浓度/moL- 1 | 混合溶液的pH |
① | 0.1 | 0.1 | pH=9 |
② | c | 0.2 | pH=7 |
③ | 0.2 | 0.1 | pH<7 |
请同答:
(1)根据①组实验情况,分析混合溶液的pH=9的原因是(用反应的离子方程式表示)___________________________
(2)在①组游液中下列关系式不正确的是(填序号字母)_______
A.c(Na+)+(H+)=c(OH-) +c(A-)
B.c(Na+ )=c(HA) +c(A-)
C.c(HA)+c(H+)=c(OH-)+c(Na+)
D. c(Na+)+(H+)=c(OH-) +c(A-)+c(HА)
(3)②组情况表明.c __________0.2 mol L-1(选填“> "、"<"或"="),混合溶液中离子浓度c(A-)________________c(Na+ )(选填“>"、"<"或=")
(4)从③组实验结果分析,说明HA的电离程度__________NaA的水解程度(选填“>"、“<"或“="),离子浓度由大到小的顺序是_____________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分类法在化学物质及反应的学习中起着重要的作用。有以下物质:①液氯②磁性氧化铁③碱石灰④石油⑤氢氧化铁胶体⑥浓硫酸⑦黑火药⑧铜
(1)上述物质中属于混合物的是___________。
(2)石油可以通过分馏(多次蒸馏)得到煤油、汽油等产物,该变化属于___(填“物理变化”或“化学变化”)。
(3)简述浓硫酸稀释的操作_________________。
(4)氢氧化铁胶体和氢氧化铁沉淀的本质区别在于________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com