
【题目】根据下面的反应路线及所给信息填空。

(1)A的名称__________,B的键线式 _________,C的结构简式 _____________。
(2)在①~⑥的各步反应中,属于取代反应的有_________,属于加成反应的有________。
(3)反应③的化学方程式是_____________________________________________________
(4)反应④的化学方程式是_____________________________________________________
(5)反应⑥的化学方程式是_____________________________________________________。
【答案】环己烷 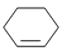
![]() ①⑥ ③⑤
①⑥ ③⑤  +Br2
+Br2![]()
![]()
![]() +2NaOH
+2NaOH![]()
![]() +2NaBr+2H2O
+2NaBr+2H2O ![]() +2NaOH
+2NaOH![]()
![]() +2NaBr
+2NaBr
【解析】
A与Cl2光照下反应生成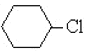 ,则A是环己烷
,则A是环己烷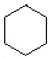 ;
;  与NaOH的乙醇溶液发生消去反应生成的B是环己烯
与NaOH的乙醇溶液发生消去反应生成的B是环己烯 ,环己烯
,环己烯 与Br2的CCl4溶液发生加成反应生成的C是1,2-二溴环己烷
与Br2的CCl4溶液发生加成反应生成的C是1,2-二溴环己烷![]() ,C发生消去反应生成
,C发生消去反应生成![]() ,
, ![]() 与Br2发生1,4-加成反应生成
与Br2发生1,4-加成反应生成![]() ,
,![]() 与NaOH水溶液发生取代反应生成
与NaOH水溶液发生取代反应生成![]() 。
。
(1)A的结构简式是 ,A的名称是环己烷,B是环己烯,B的键线式
,A的名称是环己烷,B是环己烯,B的键线式  ,C的结构简式是
,C的结构简式是![]() 。
。
(2)根据分析,①是取代反应;②是消去反应;③是加成反应;④是消去反应;⑤是加成反应;⑥是取代反应,故在①~⑥的各步反应中,属于取代反应的有①⑥,属于加成反应的有③⑤;
(3)反应③的化学方程式是 +Br2
+Br2![]()
![]() ;
;
(4)反应④的化学方程式是![]() +2NaOH
+2NaOH![]()
![]() +2NaBr+2H2O;
+2NaBr+2H2O;
(5)反应⑥的化学方程式是![]() +2NaOH
+2NaOH![]()
![]() +2NaBr。
+2NaBr。


 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案科目:高中化学 来源: 题型:
【题目】(1)第三周期8种元素按单质熔点高低的顺序如图,其中序号“8”代表___(填元素符号);其中电负性最大的是___(填图中的序号)。
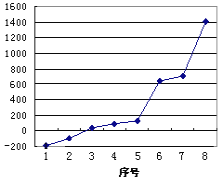
(2)请写出比元素1的原子序数大8的元素的基态原子电子排布式___。
(3)元素7的单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示。
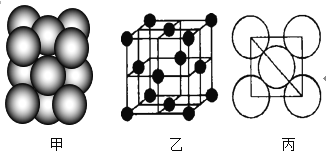
若已知7的原子半径为d cm,NA代表阿伏加德罗常数,7的相对原子质量为M,请回答:
①晶胞中7原子的配位数为___,一个晶胞中7原子的数目为___;
②该晶体的密度为___ g/cm3(用字母表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在①![]() Li ②石墨 ③C60 ④
Li ②石墨 ③C60 ④![]() Mg ⑤ CH3CH2OH ⑥
Mg ⑤ CH3CH2OH ⑥![]() C ⑦
C ⑦![]() Li ⑧ CH3OCH3 中:____互为同位素; ____互为同分异构体;___互为同素异形体(填序号)
Li ⑧ CH3OCH3 中:____互为同位素; ____互为同分异构体;___互为同素异形体(填序号)
(2)现有①CaCl2 ②金刚石 ③NH4Cl ④Na2SO4 ⑤冰 等五种物质,按下列要求回答:
①熔化时不需要破坏化学键的是___________,熔点最高的是_______。(填序号)
②只含有离子键的物质是______,晶体以分子间作用力结合的是______。(填序号)
(3)写出下列物质的电子式
①H2O______
②NaOH______
③NH3______
查看答案和解析>>
科目:高中化学 来源: 题型:
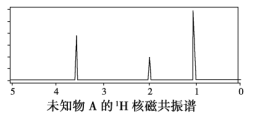
【题目】已知某有机物A的红外光谱和1H核磁共振谱如下图所示,下列说法中错误的是( )
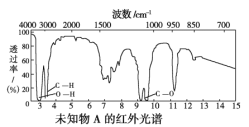
A. 由红外光谱图可知,该有机物中至少含有三种不同的化学键
B. 由1H核磁共振谱可知,该有机物分子中有三种不同的氢原子且个数比为1∶2∶3
C. 若A的化学式为C2H6O,则其结构简式为CH3CH2OH
D. 仅由其1H核磁共振谱就可得知其分子中的氢原子总数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按下列要求填空:
(1)甲基的电子式__________;
(2)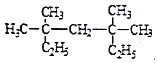 系统命名法为_________________;
系统命名法为_________________;
(3)键线式![]() 表示的有机物的结构简式是____________;
表示的有机物的结构简式是____________;
(4)烷烃A在同温同压下蒸气的密度是H2的36倍,烷烃A的结构简式为________________.
(5)相对分子质量为70的烯烃的分子式为_________,若该烯烃与足量H2加成后能生成含3个甲基的烷烃,则该烯烃可能的结构简式为_________。
(6)写出下列反应的化学方程式:
①实验室制取乙炔_____________________________________________________。
②2 -氯丙烷的消去反应_____________________________________________________。
③用甲苯制TNT的反应_____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是25℃时某些弱酸额的电离平衡常数。

(1)H2C2O4与含等物质的量的KOH的溶液反应后所得溶液呈______(填“酸性”、“碱性”或“中性”),该溶液中各离子浓度由大到小的顺序为_______。
(2)向0.1mol·L-1CH3COOH溶液中滴加NaOH溶液至c(CH3COOH):c(CH3COO-)=5:9,此时溶液pH=_______。
(3)向碳酸钠溶液中滴加少量氯水的离子方程式为________。
(4)若0.1mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,则c(Na+)-c(CH3COO-)=_______mol/L(填精确计算结果)。
(5)将CH3COOH溶液与大理石反应所产生的标况下44.8L气体全部通入到2L1.5mol/L的NaOH溶液中充分反应,则溶液中所有离子的物质的量浓度关系为______。
(6)已知某温度下,0.10mol/LNH4Cl溶液的pH=5,则该温度下NH3·H2O的电离常数约为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用“>”、“<”或“=”填空:
(1)同温同压下,H2(g)+Cl2(g)=2HCl(g),光照和点燃条件的ΔH(化学计量数相同)分别为ΔH1、ΔH2,ΔH1______ΔH2;
(2)相同条件下,2mol氢原子所具有的能量____1mol氢分子所具有的能量;
(3)已知常温时红磷比白磷稳定,比较下列反应中ΔH的大小:ΔH1_____ΔH2。
①4P(白磷,s) +5O2(g)=2P2O5(s) ΔH1,②4P(红磷,s)+5O2(g)=2P2O5(s) ΔH2;
(4)已知:101 kPa时,2C(s) +O2(g)=2CO(g) ΔH=-221kJ·mol-1,则碳的燃烧热数值____110.5 kJ·mol-1;
(5)已知:稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol,则浓硫酸与稀NaOH溶液反应生成1 mol水,放出的热量________57.3 kJ;
(6)可逆反应:aA(气)+bB(气)![]() cC(气)+dD(气);ΔH=Q,根据图回答:
cC(气)+dD(气);ΔH=Q,根据图回答:

P1______ P2;②(a+b)______(c+d);③t1℃______ t2℃。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关键环节题组:有机合成路线设计
(1)用丙醛(CH3—CH2—CHO)制取聚丙烯的过程中发生的反应类型为________
①取代 ②消去 ③加聚 ④缩聚 ⑤氧化 ⑥还原
A.⑥②③ B.⑤②③ C.②④⑤ D.①④⑥
(2)以CH2==CHCH2OH为主要原料(无机试剂任用)设计CH2==CHCOOH的合成路线流程图(已知CH2=CH2可被氧气催化氧化为 ![]() )_________________
)_________________
学法题:通过此题的解答,总结设计有机合成路线需注意(至少写2条)___________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向等物质的量浓度的![]() 、
、![]() 混合溶液中滴加稀盐酸。
混合溶液中滴加稀盐酸。
①在滴加盐酸过程中,溶液中![]() 与含硫各物质浓度的大小关系为______(选填字母)。
与含硫各物质浓度的大小关系为______(选填字母)。
a. ![]()
b. ![]()
c. ![]()
d. ![]()
②![]() 溶液中所有阴离子浓度由大到小排列是____________;
溶液中所有阴离子浓度由大到小排列是____________;![]() 溶液呈碱性,若向溶液中加入
溶液呈碱性,若向溶液中加入![]() 溶液,恰好完全反应,所得溶液呈强酸性,其原因是____________(用离子方程式表示)。
溶液,恰好完全反应,所得溶液呈强酸性,其原因是____________(用离子方程式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com