
【题目】甲醇是一种可再生能源,具有开发和应用的广阔前景,研究甲醇具有重要意义。有人模拟用CO和H2合成甲醇,其反应为:CO(g) + 2H2(g) CH3OH(g) △H<0
(1)在容积固定为1L的密闭容器内充入2 mol CO和4 mol H2发生上述反应,20min时用压力计监测容器内压强的变化如下:
反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
压强/MPa | 12.4 | 10.2 | 8.4 | 7.0 | 6.2 | 6.2 |
则反应从开始到20min时,以CO浓度变化表示的平均反应速率v(CO)=_________mol/(L·min),该温度下平衡常数K=___________,若平衡后增大压强,则K值_________(填“增大”、“减小”或“不变”)。
(2)在恒温恒容的密闭容器中,不能判定CO(g)+2H2(g) CH3OH(g) △H<0,反应达到平衡的是___________;
A、压强保持不变 B、气体的密度保持不变
C、气体平均摩尔质量保持不变 D、速率v(H2):v(CH3OH)=2:1
(3)如图是甲醇燃料电池结构示意图,C是________(填“正”或“负”)极,写出此电极的电极反应式__________________________________________。

(4)若以该电池为电源,用石墨做电极电解100mL CuSO4溶液,电解一段时间后,两极均收集到11.2L的气体(标准状况下),则原CuSO4溶液的物质的量浓度为________mol/L。
【答案】 0.075 3(mol/L)-2 不变 BD 负 CH3OH+8OH--6e-=CO32-+6H2O 5
【解析】(1)由表中数据可知,20min反应到达平衡,恒温恒容下,压强之比等于物质的量之比,则平衡时混合气体总物质的量为(2+4)mol×![]() =3mol,根据三段式求出平衡时各物质的物质的量,然后根据v=
=3mol,根据三段式求出平衡时各物质的物质的量,然后根据v=![]() 计算v(CO);根据K=
计算v(CO);根据K=![]() 计算平衡常数;平衡常数只与温度有关;
计算平衡常数;平衡常数只与温度有关;
(2)可逆反应到达平衡时,同种物质的正逆速率相等且保持不变,各组分的浓度、含量保持不变,据此判断;
(3)根据电子的流动方向可知,电极C为负极,据此分析解答;
(4)用石墨做电极电解100mL CuSO4溶液,阳极上氢氧根离子放电生成氧气,阴极上铜离子和氢离子放电,根据得失电子守恒求出生成的铜的物质的量,原CuSO4溶液的物质的量与铜的物质的量相等,据此分析解答。
(1)由表中数据可知,20min反应到达平衡,恒温恒容下,压强之比等于物质的量之比,则平衡时混合气体总物质的量为(2+4)mol×![]() =3mol,设反应的CO物质的量为x,
=3mol,设反应的CO物质的量为x,
CO(g)+2H2(g)CH3OH(g)
起始量(mol):2 4 0
变化量(mol):x 2x x
平衡量(mol):2-x 4-2x x
则(2-x)+(4-2x)+x=3mol,解得x=1.5mol,
从反应开始到20min时,以CO表示的平均反应速率v(CO)=![]() =0.075mol/(Lmin);该温度下平衡常数K=
=0.075mol/(Lmin);该温度下平衡常数K=![]() =
=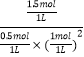 =3(mol/L)-2;若平衡后增大压强,温度不变,平衡常数不变,故答案为:0.075;3(mol/L)-2;不变;
=3(mol/L)-2;若平衡后增大压强,温度不变,平衡常数不变,故答案为:0.075;3(mol/L)-2;不变;
(2)A、该反应前后气体的物质的量发生变化,压强保持不变,能够说明是平衡状态,不选;B、气体的体积不变,质量不变,气体的密度始终保持不变,不能说明是平衡状态,选;C、该反应前后气体的物质的量发生变化,质量不变,气体平均摩尔质量保持不变,能够说明是平衡状态,不选;D、任何时候都存在v(H2):v(CH3OH)=2:1,不能说明是平衡状态,选;故选BD;
(3)根据电子的流动方向可知,电极C为负极,通入的是气体燃料甲醇,电极D为正极,通入的是氧气或空气,负极发生氧化反应,电极反应式为CH3OH+8OH--6e-=CO32-+6H2O,故答案为:负;CH3OH+8OH--6e-=CO32-+6H2O;
(4)用石墨做电极电解100mL CuSO4溶液,阳极上氢氧根离子放电生成氧气,物质的量为![]() =0.5mol,阴极上开始为铜离子放电,后来氢离子放电生成氢气,其中氢气的物质的量为
=0.5mol,阴极上开始为铜离子放电,后来氢离子放电生成氢气,其中氢气的物质的量为![]() =0.5mol,根据得失电子守恒,生成的铜的物质的量=
=0.5mol,根据得失电子守恒,生成的铜的物质的量=![]() =0.5mol,则原CuSO4溶液的物质的量浓度为
=0.5mol,则原CuSO4溶液的物质的量浓度为![]() =0.5mol/L故答案为:0.5。
=0.5mol/L故答案为:0.5。


 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:
【题目】(8分)A、B、C、D四种物质之间有下图所示的转化关系。已知:A是空气中的主要成分,B、C、D均为化合物,且C为红棕色气体。

请回答下列问题:
(1)写出A和C的名称或化学式: A ,C ;
(2)在上图D→C的过程中,D表现出强 (填“氧化性”或“还原性”);
(3)在D的稀溶液中滴入NaOH溶液,其反应的离子方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.π键是由两个p电子“头碰头”重叠形成的
B.σ键是镜面对称,而π键是轴对称
C.乙烷分子中的键全为σ键,而乙烯分子中含σ键和π键
D.H2分子中含σ键,而Cl2分子中还含π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中溴元素以Br-形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如图:
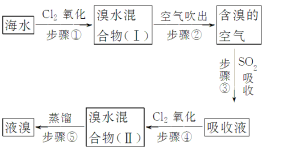
(1)步骤①反应的离子方程式是_____________________________。
(2)步骤③反应的化学方程式是______________________________。
(3)从理论上考虑,下列也能吸收Br2的是________。
A.NaOH B.FeCl2 C.Na2SO3 D.H2O
(4)步骤⑤蒸馏的过程中,温度应控制在80~90 ℃。温度过高或过低都不利于生产,请解释原因:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a、b、c、X是中学化学中常见的四种物质,且a、b、c中含有同一种元素,其转化关系如下图所示。下列说法不正确的是

A. 若a、b、c均为厨房中常用的物质,则构成c中的阳离子半径小于其阴离子半径
B. 若a为一种气态氢化物,X为O2,则a分子中可能含有10个或者18个电子
C. 若b为一种两性氢氧化物,则X可能是强酸,也可能是强碱
D. 若a为固态非金属单质,X为O2,则O元素与a元素的原子序数之差可能为8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A. 用碳酸氢钠溶液检验水杨酸中的羧基: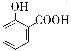 +2HCO3-→
+2HCO3-→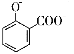 +2H2O+2CO2↑
+2H2O+2CO2↑
B. 在NaHCO3溶液中加入过量Ba(OH)2溶液:HCO3—+Ba2++OH—= BaCO3↓+H2O
C. 向Mg(HCO3)2溶液中加入过量NaOH溶液,产生白色沉淀:Mg2++2HCO3-+2OH- = MgCO3↓+2H2O
D. 用高锰酸钾溶液滴定草酸:2MnO4-+16H++5C2O42- = 2Mn2++10CO2↑+8H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下某溶液中由水电离产生的c(H+)等于10-10mol·L-1,该溶液的溶质不可能是( )
A.NaHSO4B.NaClC.HClD.Ba(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种原子序数依次增大的元素(原子序数均小于30)。A的基态原子2p能级有3个单电子;C的基态原子2p能级有1个单电子;E的内部各能层均排满,且最外层有一个电子;D与E同周期,价电子数为2。则:
(1)写出基态E原子的价电子排布式___________。
(2)A的单质分子中π键的个数为________。
(3)A、B、C三种元素第一电离能由大到小的顺序为_______(用元素符号表示)
(4)B元素的氢化物的沸点是同族元素中最高的,原因是_______。
(5)A的最简单氢化物分子的空间构型为_____,其中A原子的杂化类型是__。
(6)C和D形成的化合物的晶胞结构如图,已知晶体的密度为ρg·cm-3,阿伏加德罗常数为NA,求晶胞边长a=__________ pm. (用ρ、NA,C和D化合物的摩尔质量为M g.mol-1的计算式表示)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种化学名为 2,4,4—三氯—2— 羟基—二苯醚的物质(如下图),被广泛应用于肥皂、牙膏等日用化学品之中,有杀菌消毒等作用。则下列有关说法中正确的是 ( )

A. 该物质与 FeCl3溶液混合后不显色
B. 该物质中所有原子一定处于同一平面
C. 该物质苯环上的一溴取代物有 6 种
D. 物质的分子式为 C12H6Cl3O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com