
����Ŀ����������Ϊԭ�ϣ�ͨ��̼�Ȼ�ԭ���ɺϳɵ�����(AlN)��ͨ����ⷨ����ȡ���������ʱ����������CO2����ͨ��������̼���黯�����á�
��ش�
����֪��2Al2O3(s)=4Al(g)+3O2(g) ��H1=3351 kJ��mol-1
2C(s)+O2(g)=2CO(g) ��H2=-221 kJ��mol-1
2Al(g) + N2(g)=2AlN(s) ��H3=-318 kJ��mol-1
̼�Ȼ�ԭAl2O3�ϳ�AlN�����Ȼ�ѧ����ʽ��_____���÷�Ӧ�Է����е�����____________��
(2)�ڳ�ѹ��Ru/TiO2���£�CO2��H2�������(�����1��4�������ʵ���a mol)���з�Ӧ�����CO2ת���ʡ�CH4��COѡ�������¶ȱ仯����ֱ���ͼ1��ͼ2��ʾ(ѡ����:ת����CO2������CH4��CO�İٷֱ�)��
��ӦI CO2(g)+4H2(g)![]() CH4(g)+2H2O(g) ��H1
CH4(g)+2H2O(g) ��H1
��ӦII CO2(g)+H2(g)![]() CO(g)+H2O(g) ��H2
CO(g)+H2O(g) ��H2

������˵������ȷ����_____
A. ��H1����
B.�¶ȿ�Ӱ������ѡ����
C.CO2ƽ��ת�������¶���������������
D.�����������䣬��CO2��H2�ij�ʼ����ȸı�Ϊ1:3�������CO2ƽ��ת����
��350��ʱ����ӦI��t1ʱ�̴ﵽƽ�⣬ƽ��ʱ�������ΪVL�����¶��·�ӦI��ƽ�ⳣ��Ϊ________(��a��V��ʾ)��
��350����CH4���ʵ�����ʱ��ı仯������ͼ3��ʾ������400����0��t1ʱ��CH4���ʵ�����ʱ��ı仯���ߡ�________

�����ױ�����CO2�����ڼ���ˮ��Һ�е�����ɼ��飬���ɼ���ĵ缫��Ӧʽ��__________��
���𰸡� 3C(s)+Al2O3(s)+N2(g)=2AlN(s)+3CO(g) ��H=1026kJmol �����Է� AD 625V2/a2 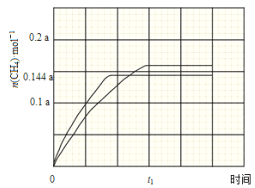 CO32-+8e-+7H2O=CH4+10OH-
CO32-+8e-+7H2O=CH4+10OH-
������������֪����2Al2O3(s)=4Al(g)+3O2(g) ��H1=+3351 kJ��mol-1����2C(s)+O2(g)=2CO(g) ��H2=-221 kJ��mol-1����2Al(g) + N2(g)=2AlN(s) ��H3=-318 kJ��mol-1�����ݸ�˹���ɢ�/2+�ڡ�3/2+�ۼ��õ�̼�Ȼ�ԭAl2O3�ϳ�AlN�����Ȼ�ѧ����ʽ��3C(s)+Al2O3(s)+N2(g)=2AlN(s)+3CO(g) ��H=+1026kJmol������Ӧ�����ȵ��ر����ӵķ�Ӧ����˸÷�Ӧ�Է����е��������¡�(2)��A. ����ͼ���֪CO2ƽ��ת�������¶��������������٣������¶�ת��������������Ӧ��������Ӧ����H1�����㡣�������ͣ�����ͼ2 ��֪������ѡ������ɵģ�A������B.����ͼ2���ж��¶ȿ�Ӱ������ѡ���ԣ�B��ȷ��C.����ͼ���֪CO2ƽ��ת�������¶��������������٣�C��ȷ��D.�����������䣬����������Ũ�ȿ����CO2ת���ʣ�D����ѡAD����350��ʱ����ӦI��t1ʱ�̴ﵽƽ�⣬ƽ��ʱ�������ΪVL����ʱCO��ʱ����
CO2(g)+4H2(g) ![]() CH4(g) + 2H2O(g)
CH4(g) + 2H2O(g)
��ʼ����mol�� 0.2a 0.8a 0 0
ת������mol�� 0.16a 0.64a 0.16a 0.32a
ƽ������mol�� 0.04a 0.16a 0.16a 0.32a
���¶��·�ӦI��ƽ�ⳣ��Ϊ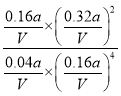 =625V2/a2��
=625V2/a2��
�۸���ͼ1��֪400����ʱCO2ת���ʽ��ͣ����ɵļ�����٣���0��t1ʱ��CH4���ʵ�����ʱ��ı仯����Ϊ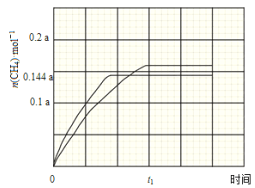 ��CO2�����ڼ���ˮ��Һ�е�����ɼ��飬��Ӧ��̼Ԫ�ػ��ϼ۽��ͣ����������ɼ��飬�缫��Ӧʽ��CO32-+8e-+7H2O=CH4+10OH-��
��CO2�����ڼ���ˮ��Һ�е�����ɼ��飬��Ӧ��̼Ԫ�ػ��ϼ۽��ͣ����������ɼ��飬�缫��Ӧʽ��CO32-+8e-+7H2O=CH4+10OH-��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��̬��0.5mol����1mol HCl��ȫ�ӳɣ��ӳɺ��������е���ԭ���ֿɱ�3mol Cl2��ȫȡ���������̬��������
A.CH3C��CCH3 B.CH2=CH2 C.CH��CCH3 D.CH2=CHCH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�����ӷ���ʽ������д��ȷ������ ��
A. ������ͭ��ϡ���ᷴӦ��OH����H��===H2O
B. ���ۼ���ϡ�����У�2Fe��6H��===2Fe3����3H2��
C. ̼�������ᷴӦ��CaCO3��2H��===Ca2����CO2����H2O
D. �Ȼ�����Һ�м��������ˮ��Al3����3NH3��H2O===Al(OH)3����3NH![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. ���Ƿ��ȷ�Ӧ�����Է��ģ��������ȷ�Ӧ���Ƿ��Է���
B. �Է���Ӧ��һ�������Է���Ӧ��һ����С��
C. �Է���Ӧ���ʵ������²���ʵ��
D. �Է���Ӧ���κ������¶���ʵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ�У�������ƽ���ƶ�ԭ�����͵���
A������ơ��ƿ��ƿ�����Ϸ��������ĭ
B����CO(g)+NO2(g)![]() CO2(g)+NO(g)ƽ����ϵ����ѹǿ��ʹ����ɫ����
CO2(g)+NO(g)ƽ����ϵ����ѹǿ��ʹ����ɫ����
C�������£���1mLpH=3�Ĵ�����Һ��ˮϡ�͵�100mL�������pH<5
D��ʵ�����г����ű���ʳ��ˮ�ķ����ռ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʾ���淴Ӧ2A(g)��B(g) ![]() 2C(g)(����ӦΪ���ȷ�Ӧ)����ȷͼ��Ϊ
2C(g)(����ӦΪ���ȷ�Ӧ)����ȷͼ��Ϊ


A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л���X�Ľṹ��ʽ��ͼ��ʾ�������й�˵������ȷ����

A. X�����к������ֹ�����
B. �������Ը��������Һ���𱽺�X
C. X��һ���������ܷ����ӳɡ��Ӿۡ�ȡ���������ȷ�Ӧ
D. �ڴ����������£�1 mol X�������5 mol H2�ӳ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���к͵ζ��ǻ�ѧ����ʵ��֮һ��ijѧ��������֪���ʵ���Ũ�ȵ��������ⶨδ֪���ʵ���Ũ�ȵ�����������Һ������д���пհף�
��1�����к͵ζ��Ĺ����������²��������ñ���Һ��ϴ�ζ��� �����ζ�����ע�����Һ �ۼ��ζ����Ƿ�©ˮ �ܵζ� ��ϴ�ӣ����ڲ�����������ȷ��˳����__________________����д��ţ�
��2��ѡ�õ�ָʾ���� ��(a��ʯ�� b������)
��3���ñ���������Һ�ζ����������������Һʱ�����ְ�����ʽ�ζ��ܵĻ���������ҡ����ƿ���۾�ע��______________________��
��4�����в����п���ʹ��������������Һ��Ũ����ֵƫ�͵���_______________��
A����ʽ�ζ���δ�ñ�������Һ��ϴ��ֱ��ע���������Һ
B���ζ�ǰʢ������������Һ����ƿ������ˮϴ����û�и���
C����ʽ�ζ����ڵζ�ǰ�����ݣ��ζ���������ʧ
D����ȡ�������ʱ����ʼ���Ӷ������ζ�����ʱ���Ӷ���
��5�����ζ���ʼ�ͽ���ʱ����ʽ�ζ����е�Һ����ͼ��ʾ���뽫���������������Ŀհ״���
�ζ����� | ��������������Һ�����/ mL | 0.1000 mol/L ��������/ mL | ||
�ζ�ǰ�̶� | �ζ���̶� | ��Һ���/ mL | ||
��һ�� | 25.00 | |||
�ڶ��� | 25.00 | 2.00 | 28.08 | 26.08 |
������ | 25.00 | 0.22 | 26.34 | 26.12 |
��6��������ϱ���������ʽ���������������Һ�����ʵ���Ũ����c(NaOH)�� ��
��7���ζ��յ���ж������� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com