
����Ŀ�����������[(NH4)2SO4��FeSO4��6H2O]�׳�Ī���Σ�������ˮ����100����110��ʱ�ֽ⡣�ڶ��������г������궨�ظ���ء�������ص���Һ�ı����ʣ�������ұ�𡢵�Ƶȡ�
��.��ѧ����С���о�Ī���ξ���ǿ��ʱ�ķֽ������
(1)����ͬѧ������ͼ��ʾ��װ�ý����о���װ��C�пɹ۲쵽��������___________���ɴ˿�֪�ֽ��������_____________��

(2)����ͬѧ��ΪĪ���ξ���ֽ�IJ����л�����SO3(g)��SO2(g)��N2��Ϊ������֤��ѡ�ü���ʵ���е�װ��A����ͼ��ʾ�IJ���װ�ý���ʵ����

������ͬѧ��ʵ���У�װ���������ӵĺ���˳��ΪA��__________________��
��װ��D�����������������____________������SO3��ʵ��������_______________��
��.Ϊ����������林��ȣ���ȡm gĪ������Ʒ�����500mL��Һ���ס��ҡ�����λͬѧ�������������ʵ�鷽������ش�
������ȡ25.00mL�����������Һ��0.1000mol��L-1������KMnO4��Һ�����ν��еζ���
�ҷ�����ȡ25.00mL�����������Һ��������ʵ����

����������ͨ��NH4+�ⶨ��ʵ�����ͼ����ͼ��ʾ��ȡ25.00mL�����������Һ���и�ʵ����

(3)�����е����ӷ���ʽΪ______________________����ʵ���������ȷ������ⶨ�������С���ҷ���������ԭ��Ϊ________________����֤�Ʋ�ķ���Ϊ___________________________________ ��
(4)�ҷ����г����Ƿ�ϴ�Ӹɾ��ļ��鷽����______________________________��
(5)��������������������Լ���__________________
a.ˮ b.����NaHCO3��Һ c.CCl4
(6)�����NH3�����������Ϊ��״���£�ΪV L������������林���Ϊ_________________��
���𰸡� ��Һ��� NH3 G D B C F ���հ���������Һ�ữ���ų�SO2�ĸ��� D�г��ְ�ɫ���� MnO4-+5Fe2+ 8H+ =Mn2++5Fe3+ + 4H2O Fe2+�ѱ������������� ȡ���������������Һ����������KSCN��Һ������Һ��ΪѪ��ɫ��˵��Fe2+���������������� ȡ���һ��ϴ�ӵ���Һ����AgNO3��Һ����û�г�����˵����ϴ�ɾ� c 175V/m ��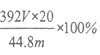
������������(1)Ī����[(NH4)2Fe(SO4)26H2O]���ȷֽ⣬�ֽ�ʱ����������Ͷ�����������������������壬����װ��ͼ��֪����ʯ�ҿ��������������壬����������̪��Һ����ɫ������װ��C�пɹ۲쵽����������Һ��죬�ɴ˿�֪Ī���ξ���ֽ�IJ������� NH3��װ��B����Ҫ������ ���շֽ�������������壬�ʴ�Ϊ����Һ��죻NH3��
(2)��Ҫ��������SO3(g)��SO2(g)��N2���ڼ���ʵ���е�װ��A�������������ȫƿ��ͨ���Ȼ�����Һ����SO3����ͨ��Ʒ����Һ����SO2����Ũ�������Ƴ�ȥ������������ˮ�������ռ�����������װ���������ӵĺ���˳��ΪA��G��D��B��C��F���ʴ�Ϊ��G��D��B��C��F��
�����ڲ������������а����������Ȼ�����Һ�м������������ᣬ�������հ�������ֹ���������ᱵ�������ų�SO2�ĸ��ţ�SO3ͨ���Ȼ�����Һ�п��Բ������ᱵ����������������ʹƷ����ɫ������װ��D����������������� ���հ���������Һ�ữ���ų�SO2�ĸ��ţ�����SO3��ʵ�������� D���а�ɫ�������ʴ�Ϊ�����հ���������Һ�ữ���ų�SO2�ĸ��ţ�D���а�ɫ������
����(3)���������Һ���������ԣ���������������Ϊ�����ӣ���Ӧ�����ӷ���ʽΪ��MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O���������Ӿ��л�ԭ�ԣ��ױ������������ӣ��ʲ�����������Ũ��ƫС���ɼ����������ӵ��������������ӣ��������Ϊ��ȡ���������������Һ����������KSCN��Һ������Һ��ΪѪ��ɫ��˵��Fe2+�ѱ����������������ʴ�Ϊ��MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O��Fe2+�ѱ���������������ȡ���������������Һ����������KSCN��Һ������Һ��ΪѪ��ɫ��˵��Fe2+�ѱ���������������
(4)�ҷ����г����Ƿ�ϴ�Ӹɾ����������ʵ�����ϴ��Һ���Ƿ��������Ӽ������ϴ���Ƿ�ɾ������岽��Ϊ��ȡ���һ��ϴ�ӵ���Һ����AgNO3��Һ����û�г�����˵����ϴ�ɾ����ʴ�Ϊ��ȡ���һ��ϴ�ӵ���Һ����AgNO3��Һ����û�г�����˵����ϴ�ɾ���
(5)��װ���е�����Һ�����ϣ�������Һ���ռ�����Ҫ����������Һ��Ӧ�����ܽⰱ��������������ˮ�ͱ���̼������Һ�����������Ȼ�̼�����������Ȼ�̼���ռ����ʴ�Ϊ��c��
(6)VL���������ʵ���Ϊ�� ![]() =
=![]() mol��m g�����������Ʒ�к�N�����ʵ���Ϊ
mol��m g�����������Ʒ�к�N�����ʵ���Ϊ![]() ��
��![]() mol=
mol=![]() mol����������淋Ĵ���Ϊ��
mol����������淋Ĵ���Ϊ�� 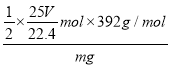 ��100%=
��100%=![]() ��100%���ʴ�Ϊ��
��100%���ʴ�Ϊ�� ![]() ��100%��
��100%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������0.1mol/L��ˮ��Һ��pH =a��������ʹ��ҺpH =��a -1���Ĵ�ʩ��
A. ����Һϡ�͵�ԭ�����10��B. �����������Ȼ�粒���
C. ��������0.1 mol/L�ռ���ҺD. ��������0.1 mol/L����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ٵ����������̼���������ڴ����е��ŷ��ǻ�����������Ҫ����֮һ��
��1����֪��N2(g)��O2(g)��2NO(g) ��H����180.5kJ��mol-1
C(s)��O2(g)��CO2(g) ��H����393.5 kJ��mol-1
2C(s)��O2(g)��2CO(g) ��H����221 kJ��mol-1
��ij��Ӧ��ƽ�ⳣ������ʽΪ��K�� ����д���˷�Ӧ���Ȼ�ѧ����ʽ________��
����д���˷�Ӧ���Ȼ�ѧ����ʽ________��
��2����CH4����ԭNOx����������Ⱦ��������ӦCH4��2NO2��CO2��2H2O��N2���Ϊԭ��أ�����ڲ��Dz��������Ƶ�����ﯾ��壬���Դ���O2-����õ�ص�������ӦʽΪ________��
��3������H2��CO2��һ�������¿��Ժϳ���ϩ��6H2(g)��2CO2(g) ![]() CH2=CH2(g)��4H2O(g)����֪��ͬ�¶ȶ�CO2��ת���ʼ�������Ч��Ӱ������ͼ��ʾ�������й�˵������ȷ����________������ţ���
CH2=CH2(g)��4H2O(g)����֪��ͬ�¶ȶ�CO2��ת���ʼ�������Ч��Ӱ������ͼ��ʾ�������й�˵������ȷ����________������ţ���

�ٲ�ͬ�����·�Ӧ��N����������
��M��ʱƽ�ⳣ����N��ʱƽ�ⳣ����
���¶ȵ���250��ʱ�����¶�������ϩ�IJ�������
��ʵ�ʷ�ӦӦ�������ڽϵ͵��¶��½��У������CO2��ת����
��4�����ܱ������г���5 mol CO��4 mol NO������������1����ij��Ӧ����ͼΪƽ��ʱNO������������¶ȡ�ѹǿ�Ĺ�ϵ��

�ش��������⣺
���¶ȣ�T1________T2����������������������
��ij�¶��£�����Ӧ���е�10���Ӵﵽƽ��״̬D��ʱ�����������Ϊ2 L�����ʱ��ƽ�ⳣ��K��________�������ȷ����λС��������CO��Ũ�ȱ仯��ʾ��ƽ����Ӧ����v(CO)��________��
������D��Է�Ӧ�������µ�ͬʱ�����������ϵѹǿ��С�����´ﵽ��ƽ��״̬������ͼ��A��G���е�________�㡣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����
��1���������ǿ�����̬��Ϊȼ�ϣ��µķ���ʽΪN2H4 �� �µĵ���ʽΪ ��
��2�����������䡱�еġ�����ָ��Ȼ��������Ҫ�ɷֵĽṹʽ�� �� һ�����ĸ����巴Ӧ���̵������仯��ͼ��ʾ���÷�ӦΪ������ȡ������ȡ�����Ӧ��25�棬101kPaʱ��1mol��������������ȼ�շų�����ΪakJ��������ȼ�յ��Ȼ�ѧ����ʽΪ �� 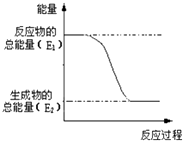
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������һ����Ҫ�������ըҩ�����Ի������о�����Ԫ�زⶨ����Խ��Խ�������ǵ����ӣ������������(HN3)��һ�����ᣬ���ӽṹʾ��ͼ�ɱ�ʾΪ��
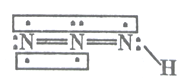
����������������ʱ��������������(HN3)��N2H4+HNO2=2H2O+HN3���������������ڴ��ᣬ�������H+��N3-���Իش��������⣺
(1)�ӳɼ�ԭ�ӵĵ縺�ԽǶ���HN3�к��еĹ��ۼ�����Ϊ_______________�����ӵļ���Ϊ_____________��
(2)������������Fe3+��Cu2+��Co3+���γ������磺Co[(N3)(NH3)5]SO4���ڸ������������_________�ۣ����ݼ۲㻥�����ۿ�֪SO42-�ռ���״Ϊ______________��д����ԭ���ڻ�̬ʱ�ĺ�������Ų�ʽ_____________��
(3)�ɵ�������(NaN3)�ȷֽ�ɵô�N2��2NaN3(s)=2Na(l)+3N2(g)���й�˵����ȷ����__________(ѡ�����)
A.NaN3��KN3�ṹ���ƣ�ǰ�߾����ܽ�С
B.�ƾ����ṹ��ͼ![]() �������з�̯2����ԭ��
�������з�̯2����ԭ��
C.���ĵ�һ�����ܴ�����
D.���������º��ȶ�������Ϊ���ĵ縺��С
(4)��N3-��Ϊ�ȵ�����ķ�����___________________ (��2����
(5)���������������Ӳ�Ƚ����ڽ��ʯ��ԶԶ�����������ϣ����������ʯͳ��Ϊ��Ӳ���ϡ�������������ͼ��ʾ���Է�����
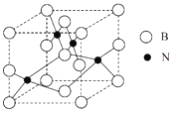
���þ�������Ϊ____________���塣
�ھ�����ÿ��Nͬʱ����________��B��
����þ����Ħ������ΪMg��mol-1��������ܶ�Ϊ��g��cm-3�������ӵ�������ֵΪNA���������������������B֮��ľ���Ϊ___________cm��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڿ��淴ӦA(g)+3B(s)![]() 2C(g)+2D(g)���ڲ�ͬ�����µĻ�ѧ��Ӧ�������£����б�ʾ�ķ�Ӧ����������
2C(g)+2D(g)���ڲ�ͬ�����µĻ�ѧ��Ӧ�������£����б�ʾ�ķ�Ӧ����������
A����(A)=0.5mol/(L��min) B����(B)=1.2mol/(L��s)
C����(C)=0.1mol/(L��s) D����(D)=0.4mol/(L��min)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Կ��淴Ӧ4NH3��g��+5O2��g��![]() 4NO��g��+6H2O��g����������ȷ��
4NO��g��+6H2O��g����������ȷ��
A. ��λʱ��������x mol NO��ͬʱ������x mol NH3����Ӧ��ƽ��״̬
B. �ﵽ��ѧƽ��ʱ��4v����O2��=5v����NO��
C. ��ѧ��Ӧ���ʹ�ϵ�ǣ�2v����NH3��=3v����H2O��
D. �ﵽƽ��ʱ�����������������������Ӧ���ʼ�С���淴Ӧ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������Դ����Ҫ������ ��
�ٺ��� �ڲ�� �۽�̿ ��̫���� ������ ��Һ��ʯ���� ��ˮú�� ����Ȼ��
A. �ڢۢޢ� B. �٢ܢ� C. �ۢޢߢ� D. �٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У�������ʹ�ú�������������ֵ���
A.2-�����顢3-������B.1-������1-�嶡��
C.�����ױ�D.1-������1-����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com