
按要求完成以下方程式:
(1)磁性氧化铁溶于盐酸的化学方程式:_________________________________________。
(2)氯化铁溶液中通入SO2气体的离子方程式:_______________ ____________________。
(3)偏铝酸钠溶液中通入过量CO2的离子方程式:_________________________________。
(4)碳单质和浓硝酸反应的化学方程式:_________________________________________。
(8分)(1)Fe3O4+8HCl=FeCl2+2FeCl3+4H2O
(2)2Fe3++SO2+2H2O=2Fe2++SO42-+4H+
(3)AlO2-+CO2+2H2O= Al(OH)3↓+HCO3-
(4)C +4HNO3(浓) CO2↑+4NO2↑+2H2O
CO2↑+4NO2↑+2H2O
解析试题分析:磁性氧化铁就是四氧化三铁,溶于盐酸生成氯化铁和氯化亚铁以及水;铁离子具有氧化性,能把SO2氧化生成硫酸;碳酸的酸性强于偏铝酸的,但偏铝酸的酸性强于碳酸氢钠的,所以偏铝酸钠溶液中通入过量CO2生成的是氢氧化铝和碳酸氢钠;浓硝酸具有强氧化性,能把碳氧化生成CO2,而浓硝酸的还原产物是NO2。
考点:考查常见方程式的书写


科目:高中化学 来源: 题型:填空题
按图的装置连接好仪器,先在烧杯中加入20mL左右的Ba(OH)2溶液,接通电源后,逐渐滴加稀硫酸至过量。
(1)当逐渐滴加稀硫酸时,烧杯中观察到的现象是: 。
(2)灯泡的现象是: ;原因是: 。
(3)发生反应的离子方程式为:
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
甲容器中发生了某化学反应,测得反应过程中,容器中存在Na+、H2O、CN-、ClO-、HCO3-、N2、Cl-七种粒子,其中ClO-和N2的物质的量随时间变化的曲线如图所示。根据题意完成下列填空: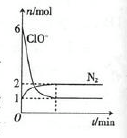
(1)CN一中氮元素的化合价是 。
(2)甲容器中发生反应的离子方程式是 。该反应的氧化产物是 (填化学式)。
(3)乙容器中用ClO2代替ClO-,溶液呈碱性,若最终两容器中N2的物质的量相同。则甲、乙两容器中参加反应的氧化剂的物质的量之比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大损害,必须进行处理。常用的处理方法有两种。其中一种方法是还原沉淀法,
该法的工艺流程为:CrO42-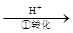 Cr2O72-
Cr2O72-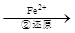 Cr3+
Cr3+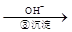 Cr(OH)3↓
Cr(OH)3↓
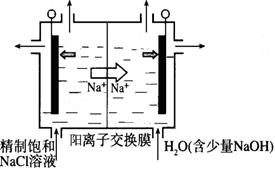
其中第①步存在平衡:2CrO42-(黄色)+2H+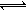 Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O
(1)若该平衡处在强酸性环境,则溶液显________色。
(2)能说明第①步反应达平衡状态的是 。
A.Cr2O72-和CrO42-的浓度相同 B.2v(Cr2O72-)=v(CrO42-) C.溶液的颜色不变
(3)第②步中,还原1molCr2O72-离子,需要 mol的FeSO4·7H2O。
写出第②步中反应的离子方程式_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(12分)某无色透明溶液中可能存在大量Ag+、Mg2+、K+、Cu2+中的一种或几种,请填写下列空白。
(1)不用做任何实验就可以肯定溶液中不存在的离子是________________。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是________,反应的离子方程式为_______________。
(3)取(2)的滤液加过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定有________,有关反应的离子方程式为________________。
(4)原溶液中可能大量存在的阴离子是
| A.Cl- | B.NO3- | C.CO3 2- | D.OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。
(1)工业上制备ClO2的反应原理常采用:2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
① 浓盐酸在反应中显示出来的性质是_______(填序号)。
| A.只有还原性 | B.还原性和酸性 | C.只有氧化性 | D.氧化性和酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
已知某无色溶液中可能含有Na+、Ba2+、Fe3+、MnO4—、SO32—、Cl—、HCO3— 中的几种,依次进行以下实验,观察到的现象如下:①用PH试纸检验,溶液的PH>7;
②向溶液中滴加氯水,没有气体产生,得到无色溶液;
③向②的溶液中滴加硝酸酸化硝酸银溶液,产生白色沉淀;
④向②的溶液中滴加BaCl2溶液,产生不溶于盐酸的白色沉淀。
则(1)原溶液中一定含有的阴离子是 ;肯定没有的阳离子是 。
(2)步骤②的离子反应方程式为 。
(3)能否确定含有阳离子 ,(若有,写出离子符号,没有则写没有),其理由是 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
食盐中含有一定量的镁、铁等杂质,加碘盐中碘的损失主要是由于杂质、水分、空气中的氧气以及光照、受热而引起的。已知:
氧化性:IO3->Fe3+>I2;还原性:S2O32->I-
3I2+6OH-=IO3-+5I-+3H2O;KI+I2 KI3
KI3
(1)某学习小组对加碘盐进行如下实验:取一定量某加碘盐(可能含有KIO3、KI、Mg2+、Fe3+),用适量蒸馏水溶解,并加稀盐酸酸化,将所得试液分为3份。第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显淡黄色,用CCl4萃取,下层溶液显紫红色;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色。
①加KSCN溶液后显红色,该红色物质是_____________(用化学式表示);CCl4中显紫红色的物质是___________(用电子式表示)。
②第二份试液中加入足量KI固体后,反应的离子方程式为_______________________________________、__________________________________________________________________。
(2)KI作为加碘剂的食盐在保存过程中,由于空气中氧气的作用,容易引起碘的损失。
写出潮湿环境下KI与氧气反应的化学方程式:_____________________。
将I2溶于KI溶液,在低温条件下,可制得KI3·H2O。该物质作为食盐加碘剂是否合适?___________ (填“是”或“否”),并说明理由_________________________________________________。
(3)为了提高加碘盐(添加KI)的稳定性,可加稳定剂减少碘的损失。下列物质中有可能作为稳定剂的是_______。
| A.Na2S2O3 | B.AlCl3 | C.Na2CO3 | D.NaNO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
向某FeBr2溶液中,通入1.12L(标准状况下)的Cl2,测得溶液中c(Br-)=3c
(Cl-)=0.3mol/L。反应过程中溶液的体积变化忽略不计,则下列说法中正确的是
| A.原溶液的浓度约为0.13mol/L | B.反应后溶液中c(Fe3+)=0.1mol/L |
| C.反应后溶液中c(Fe3+)=c(Fe2+) | D.原溶液中c(Br-)= 0.4mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com