
【题目】用质量分数为36.5%的浓盐酸(密度为1.16 g·cm-3)配制成1 mol·L-1的稀盐酸。现实验室仅需要这种盐酸220 mL,试回答下列问题:
(1)经计算需要________mL浓盐酸。
(2)在配制稀盐酸溶液时,选用的仪器除了玻璃棒、烧杯、胶头滴管、还有______________。
(3)在量取浓盐酸后,进行了下列操作:
①等稀释的盐酸的温度与室温一致后,沿玻璃棒注入250 mL容量瓶中。
②往容量瓶中小心加蒸馏水至液面离容量瓶刻度线1~2 cm时,改用胶头滴管加蒸馏水,使溶液的液面最低处与瓶颈的刻度标线相切。
③在盛盐酸的烧杯中注入蒸馏水,并用玻璃棒搅动,使其混合均匀。
④用蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是(填序号)___________________________。
(4)在上述配制过程中,用刚刚洗涤洁净的量筒来量取浓盐酸,其配制的稀盐酸浓度________(填“偏高”“偏低”或“无影响”)。若未用蒸馏水洗涤烧杯内壁或未将洗涤液注入容量瓶,则配制的稀盐酸浓度______(填“偏高”“偏低”或“无影响”)。
【答案】21.6mL 量筒、250mL容量瓶 ③①④② 偏低 偏低
【解析】
(1)先依据![]() 计算浓盐酸的物质的量浓度,再依据溶液稀释过程中所含溶质的物质的量不变计算需要浓盐酸的体积;
计算浓盐酸的物质的量浓度,再依据溶液稀释过程中所含溶质的物质的量不变计算需要浓盐酸的体积;
(2)依据配制一定物质的量浓度溶液的操作步骤选择需要的仪器;
(3)依据配制一定物质的量浓度溶液的操作步骤排序;
(4)分析操作对溶质的物质的量和溶液的体积的影响,依据![]() 进行误差分析。
进行误差分析。
(1)质量分数为36.5%的盐酸(密度为1.16gcm3)的物质的量浓度![]() ,已知需配制1 mol·L-1的稀盐酸220 mL,需要用250mL容量瓶,则配制稀盐酸的体积为250mL,设需要浓盐酸体积为V,则依据溶液稀释过程中所含溶质的物质的量不变得,V×11.6mol/L=1mol/L×0.25L,解得,V=21.6mL;
,已知需配制1 mol·L-1的稀盐酸220 mL,需要用250mL容量瓶,则配制稀盐酸的体积为250mL,设需要浓盐酸体积为V,则依据溶液稀释过程中所含溶质的物质的量不变得,V×11.6mol/L=1mol/L×0.25L,解得,V=21.6mL;
故答案为:21.6;
(2)配制1molL1的稀盐酸220mL,应选择250mL容量瓶,用浓溶液配制一定物质的量浓度稀溶液的操作步骤为:计算、量取、稀释、冷却、移液、洗涤、定容等,用到的仪器:量筒、烧瓶、玻璃棒、250mL容量瓶、胶头滴管,所以还需要的是:量筒、250mL容量瓶;
故答案为:量筒、250mL容量瓶;
(3)用浓溶液配制一定物质的量浓度稀溶液的操作步骤为:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀等,所以正确的操作顺序为:③①④②;
故答案为:③①④②;
(4)用刚刚洗涤洁净的量筒来量取浓盐酸,导致浓盐酸被稀释,量取的盐酸中含有氯化氢物质的量偏小,溶液浓度偏低;若未用蒸馏水洗涤烧杯内壁或未将洗涤液注入容量瓶,导致溶质的物的量偏小,溶液浓度偏低;
故答案为:偏低;偏低。


科目:高中化学 来源: 题型:
【题目】根据下列实验装置图回答问题:
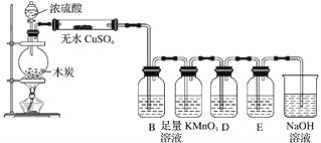
(1)浓H2SO4和木炭在加热时发生反应的化学方程式是__,如果有0.2mol电子转移,则在标准状况下产生气体__。
(2)若用图示中的装置检验上述反应的全部产物,写出有关仪器中应加入的试剂和作用:无水CuSO4试剂作用是__,B中加入的试剂是__,作用是__,足量KMnO4溶液作用是___,D中加入的试剂是__,作用是__,NaOH溶液的作用是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为Zn-聚苯胺二次电池的示意图,下列说法正确的是( )
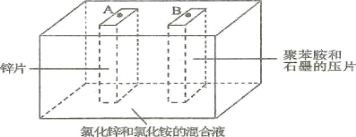
A.放电时,Zn片做负极,发生的电极方程式为Zn + 2e-=Zn2+
B.放电时,混合液中的Cl-向B移动
C.充电时,聚苯胺被氧化
D.充电时,A端接电源的正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下各种模型图都由C、H、O、N中的一种或多种元素构成。下列说法正确的是( )

A. 图①是球棍模型,其化学式为:C3H7O2N,是一种蛋白质
B. 图②是比例模型,其化学式为:C9H13NO,该物质既能与盐酸反应,又能与氢氧化钠溶液反应
C. 图③是球棍模型,其化学式为:C9H10O3,1 mol该物质能消耗3 mol氢氧化钠
D. 图③是比例模型,其化学式为:C9H13ON,能够发生消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】α-鸢尾酮香料的分子结构如图,下列说法不正确的是

A. α-鸢尾酮可与某种酚互为同分异构体
B. 1 mol α-鸢尾酮最多可与3molH2加成
C. α-鸢尾酮能发生银镜反应
D. α-鸢尾酮经加氢→消去→加氢三步反应可转变为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学活动小组设计以下装置进行不同的实验。其中a为用于鼓入空气的气囊,b 为螺旋状铜丝,c中盛有冰水。

(1)若用A装置做乙醇与乙酸的酯化反应实验,则还需连接的装置是____________(填序号),该装置中应加入试剂____________。从实验安全角度考虑,A装置试管中除加入反应液外,还需加入的固体物质是____________。
(2)该小组同学欲做乙醇氧化成乙醛的实验,则应选用的装置是____________(填序号),再用制得的乙醛溶液进行银镜反应,正确的操作顺序是____________(填序号)。
①向试管中滴入3滴乙醛溶液
②一边振荡一边滴入2%的稀氨水,直至最初产生的沉淀恰好溶解为止
③振荡后放入热水中,水浴加热
④在洁净的试管中加入1 mL 2%的AgNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼是新型无机材料中的明星元素。

(1)磷化硼是一种耐磨涂料,可由三溴化硼和三溴化磷高温下在氢气中反应合成,其化学方程式为 ______,图为磷化硼晶体结构中最小的重复单元,磷化硼的晶体类型是 ______,一个晶胞中含 ______个P原子,每个B或P均形成4个共价键,其中有一个配位键,提供空轨道的是 ______原子。
(2)氮化硼是一种重要的功能陶瓷材料,其结构与磷化硼相似,B和N相比,电负性较大的是 ______(填元素符号),其基态原子的电子排布式为 ______,氮化硼中B元素的化合价为 ______。
(3)环硼氮烷与苯是等电子体,其一氯代物有两种结构、二氯代物有四种结构,写出环硼氮烷分子结构式 ______。
(4)BF3用作有机合成中的催化剂,也用于制造火箭的高能燃料。在BF3分子中,F-B-F的键角是 ______ 度,B原子采用 ______ 杂化;BF3和过量NaF作用可生成NaBF4,BF4-的立体构型为 ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)3—甲基—1一丁炔的结构简式为_____________
(2)![]() 的分子式为_____________
的分子式为_____________
(3)烃A在同温、同压下蒸气的密度是H2的35倍,其分子式为_____________。
(4)分子式为C8H10属于芳香烃的同分异构体共有_____________种,其中____________(填结构简式)在苯环上的一氯取代产物有两种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关离子方程式正确的是( )
A.将氟气通入水中: ![]() =
=![]()
B.硝酸银溶液中滴加过量氨水: ![]() =
=![]()
C.将磁性氧化铁溶于盐酸: ![]() =
=![]()
D.往![]() 溶液中滴入
溶液中滴入![]() 溶液至沉淀的物质的量最大
溶液至沉淀的物质的量最大![]() =
=![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com