
【题目】以淀粉为基本原料可制备许多物质,如:

下列有关说法中正确的是
A.淀粉是糖类物质,有甜味,与纤维素互为同分异构体
B.反应③是消去反应,反应④是加聚反应,反应⑤是氧化反应
C.乙烯、聚乙烯分子中均含有碳碳双键,均可被酸性KMnO4溶液氧化
D.反应②是葡萄糖发生水解生成了CH3CH2OH
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列说法正确的是( )
A.标准状况下,22.4 L庚烷的分子数约为NA
B.1 L0.1mol/L的Na2S溶液中S2-和HS-的总数为0.1NA
C.4.0 g![]() 与D2O的混合物中所含中子数为2NA
与D2O的混合物中所含中子数为2NA
D.50 mL12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.对于有气体参加的反应,增大压强,反应速率加快,是因为活化分子百分数增加
B.设NA为阿伏加德罗常数的值,500mL1mol/L氯化铁溶液中Fe3+的数目等于0.5NA
C.常温下将干燥的pH试纸浸泡在0.01mol/L的NaOH溶液中来测溶液的pH,测得pH=12
D.要判断反应进行方向,须综合考虑体系的焓变和熵变,焓减且熵增的反应为自发反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一个固定体积的密闭容器充入 2mol A 和 1mol B,发生如下反应:2A(g)+B(g) 3C(g)+D(g),2 分钟后,反应达到平衡,C 的浓度为 1.2mol/L。
(1)用 A 表示 2 分钟内平均反应速率为_____,A 在第 1 分钟平均速率_______第 2分钟平均速率(填“<”、“>”、“=”)。
(2)容器温度升高,平衡时混合气体的平均相对分子质量减小,则正反应为_____(填“吸热”或“放热”)反应.
(3)增大 B 的转化率,可采取的措施是_____(用序号填空)
①加入 A ②加入 B ③加压④再加入 1.6mol A+0.8mol B ⑤将 C 分离出容器
(4)若在相同条件下,在上述容器中充入 1.5mol C 和 0.5mol D 发生上述反应,为使平衡后,C 的浓度仍为 1.2mol/L,则应再充入_____molA 和_____molB.
(5)若在一体积可变的容器中,该反应达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况如下图,a 点改变的条件可能是_____;b 点改变的条件可能是_____;若升高温度时,请将反应速率变化情况画在 c-d 处。_____________

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作无不当之处的是( )
A.用稀硫酸和锌粒制取![]() 时,加几滴
时,加几滴![]() 溶液以加快反应速率
溶液以加快反应速率
B.用蒸馏水润湿的pH试纸测某气体的酸碱性
C.淀粉水解实验中可加银氨溶液并水浴加热检验淀粉的水解产物葡萄糖
D.在50mL酸式滴定管中装入盐酸,调整初始读数为![]() 后,将剩余盐酸放入锥形瓶,可以量出
后,将剩余盐酸放入锥形瓶,可以量出![]() 的盐酸
的盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷化硼是一种超硬耐磨涂层材料。下图为其晶体结构中最小的重复结构单元,其中的每个原子均满足8电子稳定结构。下列有关说法正确的是( )

A.磷化硼晶体的化学式为BP,属于离子晶体
B.磷化硼晶体的熔点高,且熔融状态下能导电
C.磷化硼晶体中每个原子均形成4条共价键
D.磷化硼晶体结构微粒的空间堆积方式与氯化钠相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】As2O3(砒霜)是两性氧化物(分子结构如图所示),溶于盐酸生成AsCl3,AsCl3用LiAlH4还原生成AlH3。下列说法正确的是( )
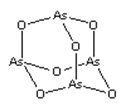
A.As2O3 分子中As原子的杂化方式为sp2
B.LiAlH4为共价化合物
C.AsCl3空间构型为平面正三角形
D.AlH3分子键角大于109.5°
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子。
(1)该融雪剂的化学式______________;X与氢元素形成的化合物的电子式_____________。
(2)元素D、E原子的最外层电子数均为电子层数的2倍,D与Y相邻,则D离子的原子结构示意图是____________ ;D与E能形成一种非极性分子,该分子的结构式____________;写出与其互为等电子体的一种分子和阴离子________________、___________________。
(3)元素W与Y同周期,其单质是原子晶体;元素Z的单质分子Z2中有3个共价键;W与Z能形成一种新型无机非金属材料,其化学式是____________。
(4)元素R与Y同主族,其氢化物能用于刻蚀玻璃,写出该反应的化学方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等量的固体Mg(OH)2,置于等体积的下列液体中,最终固体剩余最少的是( )
A.在纯水中B.在0.1mol/L的MgCl2溶液中
C.在0.1mol/L的NH3·H2O中D.在0.1mol/L的CH3COOH溶液中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com