
元素性质呈周期性变化的决定因素是 ( )
A.元素原子核外电子层排布呈周期性变化 B.元素相对原子质量依次递增
C.元素原子半径大小呈周期性变化 D.元素的最高正化合价呈周期性变化
 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
某研究性学习小组在研究化学反应中的能量变化时,做了下面的实验:

在一个小烧杯里,加入20 g已研磨成粉末的Ba(OH)2·8H2O,将小烧杯放在事先已滴有3~4滴水的玻璃片上,然后向烧杯中加入约10 g NH4Cl晶体,根据实验步骤,填写下表,并回答问题。
| 实验步骤 | 实验现象及结论 |
| 将晶体混合,立即快速搅拌 | 有刺激性气味能使湿润的紫色石蕊试纸变蓝的 ① 产生 |
| 用手摸烧杯下部 | 感觉烧杯变凉说明此反应是 ② 反应 |
| 用手拿起烧杯 | 烧杯下面的带有几滴水的玻璃片粘到了烧杯底部 |
| 将粘有玻璃片的烧杯放在盛有热水的烧杯上 | 玻璃片脱离上面烧杯底部 |
| 反应后移走多孔塑料片观察反应物 | 混合物成糊状,证明有 ③ 生成 |
① ② ③
④写出实验过程中发生反应的化学方程式:____________________。
⑤实验中要立即用玻璃棒迅速搅拌的原因是: __________________。
⑥在上述实验过程中,为什么用浸有稀硫酸的湿棉花置于多孔塑料板上?
______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
纯碱(Na2CO3)在生产生活中具有广泛的用途。以下是实验室模拟制碱 原理制取Na2CO3的流程图。
原理制取Na2CO3的流程图。

已知:向饱和食盐水中通入NH3、CO2后发生的反应为NaCl+NH3+CO2+H2O===NaHCO3↓+NH4Cl。请回答以下问题:
(1)粗盐中含有的杂质离子有Ca2+、Mg2+、SO42-等。
精制除杂的步骤顺序是a→________→________→________→b(填字母编号)。
a.粗盐溶解,滤去沉渣 b.加入盐 酸调pHc.加入Ba(OH)2溶液 d.加入Na2CO3溶液
酸调pHc.加入Ba(OH)2溶液 d.加入Na2CO3溶液
e.过滤
向饱和食盐水中先通入NH3,后通入CO2,理由是_________________________ _________________________________________________________________。
(2)灼烧固体A制Na2CO3在________(填字母序号)中进行。
a.坩埚 b.蒸发皿 c.烧杯 d.锥形瓶
证明滤液A中含有NH4+的方法是_____________________________________ _________________________________________________________________。
对滤液A进行重结晶能够获得NH4HCO3,向pH=13含Na+、K+的溶液中加入少量NH4HCO3使pH降低,反应的离子方程式为____________________。
(3)下图装置中常用于实验室制备CO2的是________(填字母编号);用b装置制备NH3,分液漏斗中盛放的试剂是________(填试剂名称),烧瓶内可加入的固体试剂是________(填试剂名称)。

(4)一种天然碱晶体成分是aNa2CO3·bNa2SO4·cH2O,某同学利用下列提供的试剂,设计了如下简单合理测定Na2CO3的质量分数的实验方案。(仪器自选)请把实验方案填全:
供选择的试剂:1.0 mol·L-1 H2SO4 溶液、1.0 mol·L-1 BaCl2溶液、稀氨水、碱石灰、Ca(OH)2溶液、蒸馏水
溶液、1.0 mol·L-1 BaCl2溶液、稀氨水、碱石灰、Ca(OH)2溶液、蒸馏水
①称取m1g天然碱晶体样品,溶于适量蒸馏水中。
②_______________________________________________________________。
③_______________________________________________________________。
④计算天然碱晶体中含Na2CO3的质量分数。
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数的值,下列说法正确的是( )
①用铜作电极电解饱和NaCl溶液,当线路中通过NA个电子时,阳极产生11.2 L气体(标准状况下) ②常温常压下,16 g O2和16 g O3含氧原子数均为NA ③标准状况下,22.4 L CH3CH2OH中含有的碳原子数为2NA ④6.5 g锌全部溶于一定量的浓硫酸,生成SO2与H2的混合气体,气体分子总数为0.1NA ⑤10.6 g Na2CO3粉末中含有CO 数为0.1NA
数为0.1NA
A.②④⑤ B.①③⑤
C.①②④⑤ D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是无机物A~M在一定条件下的转化关系(部分产物及反应条件未列出)。其中,I是由第三周期元素组成的单质中熔点最高的金属,K是一种红棕色气体。
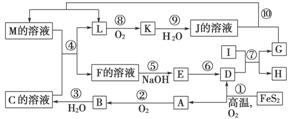
提示:4FeS2+11O2高温,2Fe2O3+8SO2
请填写下列空白:
(1)在周期表中,组成单质G的元素位于第________周期________族。
(2)在反应⑦中氧化剂与还原剂的物质的量之比为________。
(3)在②、③、⑥、⑨中既属于化合反应又属于非氧化还原反应的是________(填序号)。
(4)反应④的离子方程式是_____________________________________。
(5)将化合物D与KNO3、KOH共熔,可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾),同时还生成KNO2和H2O。该反应的化学方程式是
______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
据报道,全球每年发生金属腐蚀而造成的直接经济损失达数千亿美元。下列各电极反应
式中,能表示铁的电化学腐蚀的是 ( )
① Fe-2e-=Fe2+ ② 2H++2e-=H2↑ ③ Fe-3e-=Fe3+
④ 2H2O+O2+4e-=4OH- ⑤ 4OH--4e-=2H2O+O2↑
A.①②⑤ B.②③④ C.①②④ D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
下列能说明氯元素比硫元素非金属性强的是 ( )
①HCl比H2S稳定;②HClO4酸性比H2SO4强;③Cl2能与H2S反应生成S;④Cl原子最外层有7个电子,S原子最外层有6个电子;⑤Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS;⑥盐酸是强酸,而氢硫酸是弱酸
A.①②③④⑤⑥ B.①②③④⑥ C.①②③⑤ D.②④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:C(s)+ O2(g)===CO(g) ΔH=-110.5 kJ·mol-1①
O2(g)===CO(g) ΔH=-110.5 kJ·mol-1①
C(s)+O2(g)===CO2(g) ΔH=-393.51 kJ·mol-1②
计算反应C(s)+CO2(g)===2CO(g)的反应热ΔH的值为
A.-283.01 kJ·mol-1 B.+172.51 kJ·mol-1 C.+283.1 kJ·mol-1 D.+504.00 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列溶液中,各组离子一定能够大量共存的是( )
A.能使广泛pH试纸显蓝色的溶液:K+、Ba2+、Cl-、Br-
B.常温下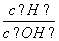 =1012的溶液:Fe2+、Mg2+、NO
=1012的溶液:Fe2+、Mg2+、NO 、Cl-
、Cl-
C.含有大量Al3+的溶液:Na+、Cl-、AlO 、OH-
、OH-
D.能使淀粉碘化钾试纸显蓝色的溶液:K+、SO 、S2-、SO
、S2-、SO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com