
����Ŀ�������ѽ��������ܶ�����Խ���ں��պ���������;�㷺���ش��������⣺
��1����Ԫ�ػ�̬ԭ�ӵĵ����Ų�ʽΪ______________��δ�ɶԵ�����Ϊ_______________����
��2��[TiO(H2O2)2]2+�����ӳʻ�ɫ���ṩ����ԭ�ӹµ��ӶԵijɼ�ԭ����_____________(��Ԫ�ط��ţ�������ԭ�ӵĻ��ϼ�Ϊ_____________������֮һH2O2����ԭ���ӻ�����Ϊ__________��H2O2��������ԭ�ӵļ۲���ӶԻ���ģ����______________��
��3�����ʷ����Ѷ�����______________���γɵľ��壬��֪���������������ܶѻ��������������������ѻ�����__________(������������������)�Ŀռ������ʽϴ�
��4��̼������Ҫ�������췰�ּ�̼����Ӳ�ʺϽ����Ӽ����侧���ṹ��ͼ��ʾ��
 (С��ΪVԭ��)
(С��ΪVԭ��)
��������̼ԭ���뷰ԭ�ӵ�������Ϊ____________��
���þ�������̼ԭ�Ӿ����������ȵ�̼ԭ�Ӹ���Ϊ_____________��
�����Ͻ���ܶ�Ϊdg�� cm-3������������=______nm��
���𰸡� [Ar]3d24s2 2 O +4 sp3 �������� ���� �� 1��1 �������10��12 ![]() ��107
��107
����������1����Ԫ�ػ�̬ԭ�ӵĵ����Ų�ʽΪ[Ar]3d24s2��δ�ɶԵ���Ϊ3d����ϵ�2�����ӣ���Ϊ���ݺ��ع�����2������Ҫ��ռ������ͬ�Ĺ��������״̬��ͬ��
��2��[TiO(H2O2)2]2+�����ӳʻ�ɫ���ṩ����ԭ�ӹµ��ӶԵijɼ�ԭ����O������ԭ�ӵĻ��ϼ�Ϊ+4������֮һH2O2����ԭ�ӵļ۲���Ӷ���4�����������ӻ�����Ϊsp3��H2O2��������ԭ�ӵļ۲���ӶԻ���ģ�����������Ρ�
��3�����ʷ����Ѷ����ɽ������γɵľ��壬��֪���������������ܶѻ��������������������ѻ������ѵĿռ������ʽϴ�
��4����̼���������ṹ��֪���þ�����Vԭ����Ϊ12![]() +1=4��Cԭ����Ϊ8
+1=4��Cԭ����Ϊ8![]() ��
��
�پ�����̼ԭ���뷰ԭ�ӵ�������Ϊ1��1��
���Ծ�������Ϊ���ģ������ҵ�3�����ഹֱ�������Σ����ĵ������ε��ĸ���������������ȣ�������һ�����������ҵ��þ�������̼ԭ�Ӿ����������ȵ�̼ԭ�Ӹ���Ϊ12��
�����Ͻ���ܶ�Ϊdg�� cm-3��1mol�˾���������Ϊ63![]() g��1mol�˾��������ΪNAa3����dg�� cm-3=
g��1mol�˾��������ΪNAa3����dg�� cm-3=![]() ������������=
������������= ![]() cm=
cm=![]() ��107nm��
��107nm��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����б仯��һ��Ҫ��������������
A. CaCO3 �� CO2
B. NaCl �� NaNO3
C. Zn �� ZnCl2
D. Cl2��HCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵõ���������ֵ��������������ȷ���ǣ� ��
A.1 mol NH3�����еĵ�����Ϊ9NA
B.���³�ѹ�£�22.4 L����������ԭ����Ϊ2NA
C.46 g NO2��N2O4�Ļ���ﺬ�еĵ�ԭ����Ϊ1NA
D.���ʵ���Ũ��Ϊ0.5 mol/L��MgCl2��Һ�У�����Cl�� ����Ϊ NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������̵���Ҫ������ͳ��õ��������������ǹ�ҵ�������̿��Ʊ�������ص�һ�ֹ������̣� 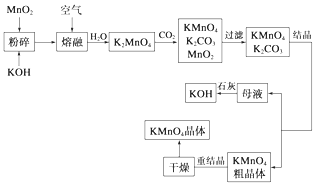
��1��KMnO4ϡ��Һ��һ�ֳ��õ���������������ԭ��������������ţ��������ƣ�
A.75%�ƾ�
B.˫��ˮ
C.84����Һ��NaClO��Һ��
��2��д��MnO2��KOH�����ڻ������ͨ�����ʱ��������Ҫ��Ӧ�Ļ�ѧ����ʽ�� ��
��3����K2MnO4��Һ��ͨ��CO2���Ʊ�KMnO4 �� �÷�Ӧ�еĻ�ԭ���� ��
��4��������������ѭ�����Ʊ������е���ʧ����1mol MnO2���Ƶ�mol KMnO4 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڱ�״���¢�6.72L CH4��3.01��1023��HCl���� ��13.6g H2S ��0.2mol NH3 �� ���ж�����������Ĺ�ϵ�Ӵ�С������ȷ���ǣ� ��
A.����ڣ��ۣ��٣���
B.�ܶȢڣ��ۣ��٣���
C.�����ڣ��٣��ۣ���
D.��ԭ�Ӹ����٣��ۣ��ڣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������ơ���װ��ʹ�÷�������ѧ��ѧʵ��Ļ�������ͼΪ����ʵ��װ�ã� 
��1��д���������������ƣ� ������������
��2�������١����У�ʹ��ʱ�������Ƿ�©ˮ������ͼIʵ�������ʹ��������ʱӦ������ˮ��������ţ���
��3��������װ��I�������Ȼ�̼�;ƾ��Ļ�����ȱ�ٵ���������������������������е�ʵ�����������Ϊ�� �� ��������500ml 0.2mol/L NaCl��Һ��װ��II��ijͬѧת����Һ��ʾ��ͼ��ͼ�еĴ����� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com