
【题目】某化学小组设计“全氢电池”如图中甲池(其中a、b为多孔石墨电极),拟用该电池电解处理生活污水,达到絮凝净化的目的。其工作原理示意图:
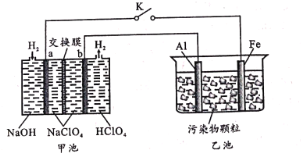
闭合K工作过程中,下列分析错误的是
A.甲池中a极反应为:H2-2e-+2OH-=2H2O
B.乙池中Fe电极区附近pH增大
C.一段时间后,乙池的两极间出现污染物颗粒沉降现象
D.如果Al电极上附着较多白色物质,甲池中Na+经过交换膜速率定会加快
【答案】D
【解析】
根据此装置电解处理生活污水可知,甲池为原电池,乙为电解池,a为负极,b为正极,铁为阴极,铝为阳极,a极反应为:H2-2e-+2OH-=2H2O,b极反应为2H++2e-=H2↑,总的电极反应为H++ OH-=H2O,利用甲池产生的电流电解乙池,乙池中,铝为阳极,铁为阴极,阳极反应为:Al-3e- =Al3+,阴极反应为2H++2e-=H2↑由此分析。
A.甲池为原电池,a为负极,a极通入氢气,氢气在负极上失去电子生成氢离子,结合氢氧根离子生成水,电极反应为H2-2e-+2OH-=2H2O,故A正确;
B.乙池中,铁作阴极,电极反应为:2H++2e-=H2↑,溶液中氢离子的浓度减小,氢氧根离子的溶度相对增大,pH增大,故B正确;
C.乙为电解池,铝为阳极,铁为阴极,阳极反应为:Al-3e- =Al3+,阴极反应为2H++2e-=H2↑,溶液中的氢离子的浓度减小,氢氧根离子向阳极移动,在阳极结合铝离子生成氢氧化铝胶体,吸附污染物颗粒一起沉降,在阴极,一段时间后, 铝离子向阴极移动,铝离子可以在溶液中形成氢氧化铝胶体,吸附水中的污染物颗粒一起沉降,故C正确;
D.如果Al电极上附着较多白色物质,白导致色物质为氢氧化铝,阻止了铝电极继续放电,导致导线中电荷的数目减小,甲池中Na+经过交换膜速率定会减慢,故D错误;
答案选D。


科目:高中化学 来源: 题型:
【题目】A、B、C为短周期元素,在周期表中所处的位置如右图所示。A、C两元素的原子核外电子数之和等于B原子的质子数。B原子核内质子数和中子数相等。
![]()
(1)写出A、B、C三种元素的名称________、________、________。
(2)B位于元素周期表中第________周期________族。
(3)C的原子结构示意图为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、用如图仪器组装成一套简易量热计测定室温下中和反应的反应热。
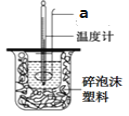
(1)碎泡沫塑料的作用是__________;图中仪器a的名称是____________;
(2)中和反应的实质是_______________(用离子方程式表示)。
Ⅱ、.某研究性学习小组的同学对Zn、Cu、稀硫酸组成的原电池进行了探究,其中甲同学利用下图I装置进行探究,乙同学经过查阅资料后设计了图II装置进行探究(盐桥内含有某种电解质的饱和溶液,起到连通电路的作用)。
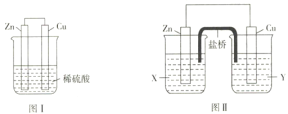
(3)实验表明,图I中两个电极上均有气泡产生,锌电极上有气泡产生,说明反应中有一部分化学能转化为_____能;铜电极上有气泡产生,说明反应中有一部分化学能转化为____能。
(4)图II中的X、Y是ZnSO4溶液及稀硫酸中的一种,实验过程中只有正极上产生气泡,则X是_________,正极上的电极反应式为__________。
(5)当图I装置的溶液质量增加63g时,生成的氢气共有______L(标准状况;当图II中锌电极质量减少65g时,电路中转移的电子数为______NA。
Ⅲ、在一定条件下甲烷也可用于燃料电池。下图是甲烷燃料电池的原理示意图:

(6)若正极的反应式为O2+4e-+4H+=2H2O,则负极反应式为___________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是五种短周期元素的原子序数与其在氢化物中化合价的关系图,则下列说法不正确的是( )
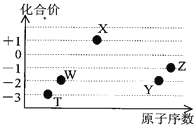
A.X的氢化物具有很强的还原性
B.YW2、ZW2、X2W2都能使品红溶液褪色,且褪色原理相同
C.Y、Z元素的最高价氧化物对应的水化物都呈酸性,而且酸性:HZO4 > H2YO4
D.元素W、T的氢化物的沸点比同主族中相邻的氢化物高,是因为这两种氢化物分子间存在氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠广泛用于媒染剂、漂白剂等。某兴趣小组用下列装置制取较纯净的NaNO2。
甲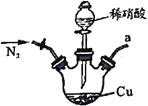 乙
乙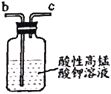 丙
丙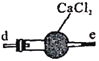 丁
丁![]()
反应原理为:2NO+Na2O2=2NaNO2。已知:NO能被酸性KMnO4氧化成NO3-,MnO4-被还原为Mn2+。下列分析错误的是
A.甲中滴入稀硝酸前需通人N2
B.仪器的连接顺序为a-f-g-d-e-b
C.丙中CaCl2用于干燥NO
D.乙中吸收尾气时发生的离子反应为3MnO4-+5NO+4H+=3Mn2++5NO3-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卫生部发出公告,自2011年5月1日起,禁止在面粉生产中添加过氧化钙(CaO2)等食品添加剂。CaO2和Na2O2在结构和性质上有很多相似的地方。请完成下列问题:
(1)CaO2属于____(填“离子化合物”或“共价化合物”),其电子式为_____,其阴、阳离子个数比为______。
(2)CaO2与水反应的化学方程式为______,生成1mol单质气体,转移的电子数为__________。(用NA代表阿伏加德罗常数)
(3)CaO2与二氧化碳反应的化学方程式为_________,该反应属于____________。
A.置换反应 B.氧化还原反应 C.复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把铁和氧化铁组成的某混合物放入250 mL 2.0 mol·L-1的硝酸溶液中,充分反应后,生成的一氧化氮气体在标准状况下的体积为1.12 L,再向反应后的溶液中加入1.0 mol·L-1的氢氧化钠溶液,要使铁元素完全沉淀下来,加入的氢氧化钠溶液的体积最少是
A.400 mLB.450 mLC.500 mLD.550 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.CH4和C15H32为同系物
B.分子式为C4H8BrCl的有机物共有11种(不含立体异构)
C.化合物![]() (b)、
(b)、![]() (d)、正戊烷(p)中只有b的所有碳原子可能处于同一平面
(d)、正戊烷(p)中只有b的所有碳原子可能处于同一平面
D.CH3CH=CHCH3分子中的四个碳原子在同一直线上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体A的化学式为NH5(也可写为:NH4H),它的所有原子的最外层均满足2个或8个电子的稳定结构。则下列有关说法中错误的是( )
A.它与水反应的化学方程式为NH5 + H2O ═ NH3H2O + H2↑
B.NH5中既有共价键又有离子键
C.NH5的电子式为 
D.1 mol NH5中含有5NA个N﹣H键(NA表示阿伏加德罗常数的值)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com