
【题目】用98%的浓硫酸(其密度为1.84 g·cm-3)配制250 mL0.4 mol·L-1稀硫酸,有以下实验仪器供选:A 10mL量筒 B 托盘天平 C 玻璃棒 D 250 mL容量瓶 E 500 mL容量瓶 F 胶头滴管 G. 烧杯
(1)需量取浓硫酸的体积为___________mL。
(2)实验时不可选用的仪器有(填序号) __________________。
(3)配制过程中,下列情况会使配制结果偏高的是_____(填序号)
①容量瓶使用时未干燥;
②定容时俯视刻度线观察液面;
③将浓硫酸在烧杯中稀释后未经冷却就转移至容量瓶中,并定容;
④定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线。
(4)配置过程中,实验操作步骤为: __________
A.在烧杯中注入蒸馏水(溶液体积少于250mL),沿烧杯壁注入量取的浓硫酸用玻璃棒搅拌,使其混匀。
B.待稀释的硫酸冷却后,沿玻璃棒注入250mL的容量瓶中。
C.用量筒量取密度为1.84g/cm3质量分数为98%的浓硫酸。
D.用蒸馏水洗涤烧杯2~3次,将洗涤液注入容量瓶中。
E.往容量瓶中小心加蒸馏水至液面接近刻度1-2cm处,改用胶头滴管加蒸馏水,使溶液凹液面恰好与刻度线相切。
【答案】5.4 BE ②③ CABDE
【解析】
(1)先根据c=![]() 计算出浓硫酸的物质的量浓度,然后根据溶液稀释定律c浓V浓=c稀V稀计算;
计算出浓硫酸的物质的量浓度,然后根据溶液稀释定律c浓V浓=c稀V稀计算;
(2)根据配制步骤是计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶来分析需要的仪器,并分析解答(4);
(3)根据c=![]() 并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析。
并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析。
(1)浓硫酸的物质的量浓度为c=![]() =
=![]() =18.4mol/L,设所需的浓硫酸的体积为VmL,根据溶液稀释定律c浓V浓=c稀V稀可知:18.4mol/L×VmL=0.4mol/L×250mL,解得:V=5.4mL,故答案为:5.4;
=18.4mol/L,设所需的浓硫酸的体积为VmL,根据溶液稀释定律c浓V浓=c稀V稀可知:18.4mol/L×VmL=0.4mol/L×250mL,解得:V=5.4mL,故答案为:5.4;
(2)根据配制一定物质的量浓度的溶液的步骤有:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶可知,所需的仪器有10mL量筒、烧杯、玻璃棒、250mL容量瓶、胶头滴管,故不需要使用的仪器有托盘天平、500 mL容量瓶,故答案为:BE;
(3)①容量瓶使用时未干燥,对浓度无影响,故错误;②定容时俯视刻度线观察液面,则溶液体积偏小,浓度偏高,故正确;③将浓硫酸在烧杯中稀释后未经冷却就转移至容量瓶中,并定容,则冷却后溶液体积偏小,浓度偏高,故正确;④定容后经振荡、摇匀、静置,发现液面低于刻度线是正常的,再加蒸馏水补至刻度线则浓度偏低,故错误;故答案为:②③;
(4)配制一定物质的量浓度溶液的步骤为:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶,所以正确的顺序为:CABDE,故答案为:CABDE。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】A、B、M、N四种有机物的有关信息如下表所示:
A | B | M | N |
比例模型为; | 球棍模型为: | 键线式结构为: | ①能与钠反应,但不能与NaOH溶液反应;②能与M反应生成相对分子质量为100的酯 |
请回答:
(1)A在一定条件下可合成包装塑料,反应的化学方程式为____________。
(2)在Ni作催化剂的条件下,B与氢气加热时反应的化学方程式为______________。
(3)M的分子式为__________,M与N反应的化学方程式为_______________。
(4)满足下列条件的M的同分异构体的结构简式为______________。
I:链状 ii:只含一种官能团 iii:能与新制氢氧化铜在加热条件下生成砖红色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,有错误的是( )
A.Na2CO3溶液能与石灰水反应,而NaHCO3溶液不能与石灰水反应
B.在相同温度下,NaHCO3的溶解度比Na2CO3小
C.Na2CO3很稳定,而NaHCO3受热时容易分解
D.将等物质的量的NaHCO3粉末与Na2CO3粉末同时分别倒入适量的相同浓度的稀盐酸中,前者的反应更剧烈
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)亚硝酰氯(ClNO)是有机合成中常用试剂,已知:2NO(g)+Cl2(g)![]() 2ClNO(g) △H<0,一定温度下,将2 molNO与2 molCl2置于2L密闭容器中发生反应。
2ClNO(g) △H<0,一定温度下,将2 molNO与2 molCl2置于2L密闭容器中发生反应。
①下列可判断反应达平衡状态的是___________(填序号字母)。
A. 混合气体的平均相对分子质量不变 B. 混合气体密度保持不变
C. NO和Cl2的物质的量之比保持不变 D. 每消耗1 moI NO同时生成1molClNO
②为了加快化学反应速率,同时提高NO的转化率,其他条件不变时,可采取的措施有_________(填选项序号字母)。
A. 升高温度 B. 缩小容器体积 C. 再充入Cl2气体 D. 使用合适的催化剂
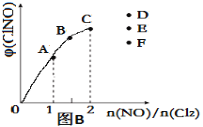
③一定条件下在恒温恒容的密闭容器中,按一定比例充入NO(g)和Cl2(g),平衡时ClNO的体积分数随n(NO)/n(Cl2)的变化图像如图(B)所示,当n(NO)/n(Cl2)=2.5时,达到平衡状态,ClNO的体积分数可能是下图中D、E、F三点中的________点。
(2) 在体积为10 L的密闭容器中充入3 mol NO和2 mol Cl2,在不同温度下发生反应2NO(g)+Cl2(g)![]() 2ClNO(g),ClNO的百分含量随时间的变化如图所示。已知T1>T2>T3。
2ClNO(g),ClNO的百分含量随时间的变化如图所示。已知T1>T2>T3。
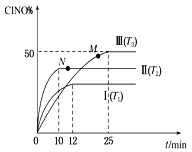
①与实验Ⅰ相比,实验Ⅱ除温度不同外,还改变的条件是__________________。
②实验Ⅲ反应至25 min达到平衡,用NO物质的浓度变化表示的反应速率为__________________。达到平衡时,若实验Ⅲ达到平衡时的热量变化为Q kJ,则该反应的热化学方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积可变的400 ℃密闭容器中,一定量的SO2和O2在催化剂作用下发生反应:2SO2(g)+O2(g) 2SO3(g)+QkJ,下列叙述错误的是( )
2SO3(g)+QkJ,下列叙述错误的是( )
A.增大压强,正反应速率一直增大至不变,平衡正移
B.降低温度,正反应速率比逆反应速率减小的程度小
C.若将三氧化硫分离出,则平衡正向移动,平衡常数K值不变
D.若气体的物质的量减少0.5mol时达到平衡,则该条件下反应放出0.5QkJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】东晋![]() 华阳国志
华阳国志![]() 南中志
南中志![]() 卷四中已有关于白铜的记载,云南镍白铜
卷四中已有关于白铜的记载,云南镍白铜![]() 铜镍合金
铜镍合金![]() 闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)已知:丁二酮肟[HON=(CH3)CC(CH3)=NOH]是检验Ni2+的灵敏试剂。丁二酮肟分子中C原子轨道杂化类型为___,1mol丁二酮肟分子所含σ键的数目为___。
(2)单质铜及镍都是金属晶体;铜晶体的堆积方式为___;元素铜与镍的第二电离能分别为:ICu=1958kJ·mol-1、INi=1753kJ·mol-1,ICu>INi的原因是___。
(3)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构见图(1)。写出该反应的化学方程式:___。
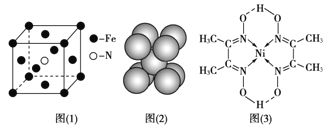
(4)下列关于铁和镍及其化合物说法正确的是___
a.金属镍能与CO形成配合物Ni(CO)4,常温下为液态,易溶于CCl4、苯等有机溶剂。所以Ni(CO)4固态时属于分子晶体
b.[Ni(NH3)6]SO4中阴离子的立体构型是正八面体
c.Ni2+和Fe2+的半径分别为69pm和78pm,则晶格能NiO>FeO,熔点NiO>FeO
d.铁晶胞结构见图(2),每个晶胞含有2个铁原子
(5)配合物Y的结构见图(3),Y中含有的化学键有___![]() 填序号
填序号![]() ;
;
a.极性共价键 b.非极性共价键 c.配位键 d.氢键 e.离子键 f.金属键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应:4CO(g)+2NO2(g)=4CO2(g)+N2(g)△H=-1200KJ/mol,温度不同(T2>T1)其他条件相同时,下列图像正确的是

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,向密闭容器中加入一定量的C(s)与H2O(g)发生可逆反应C(s) + H2O(g)![]() CO(g) + H2(g),反应达到平衡后C(s)与H2O(g)转化率为2:1关系,则下列说法正确的是
CO(g) + H2(g),反应达到平衡后C(s)与H2O(g)转化率为2:1关系,则下列说法正确的是
A.开始加入的C(s)与H2O(g)物质的量为2:1
B.若增大压强,H2O(g)转化率不变化
C.达到平衡后混合气体平均式量可能为16
D.开始反应后混合气体平均式量一直减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇:
(1)已知:①H2(g)+1/2O2(g)![]() H2O(l) ΔH1=-285.8 kJ/mol;
H2O(l) ΔH1=-285.8 kJ/mol;
②CO (g)+1/2O2 (g)![]() CO2 (g) ΔH2=-283kJ/mol
CO2 (g) ΔH2=-283kJ/mol
③CH3OH(g)+3/2O2(g)![]() CO2(g)+2H2O(l) ΔH3=-764.6 kJ/mol
CO2(g)+2H2O(l) ΔH3=-764.6 kJ/mol
则工业制备甲醇的可逆反应热化学方程式为_______________________________;
(2)恒温恒容条件下,下列描述中能说明上述反应已达平衡状态的是__________。
A.单位时间内生成n mol CO的同时生成2n mol H2 B.ν(H2)正=2ν(CH3OH)逆
C.容器内气体的密度保持不变 D.容器中气体的压强保持不变
(3)某化学研究性学习小组模拟工业合成甲醇的反应,在容积固定为2L的密闭容器内充入1 molCO和 2 molH2,加入合适催化剂(体积可以忽略不计)后在250°C开始反应,CO物质的量随时间变化如下:
反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
n(CO)/mol | 1.00 | 0.79 | 0.63 | 0.54 | 0.50 | 0.50 |
则从反应开始到20min时,以ν(H2)=________,该温度下平衡常数K=_______。
(4)加入催化剂后在250 ℃开始反应,CO的平衡转化率与温度、压强的关系如图所示。
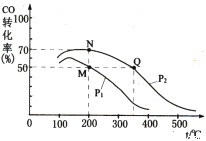
①M、N、Q三点的平衡常数KM、KN、KQ的大小关系为___________________________。
②由M点到N点改变的外界条件是_________。
A、降低温度 B、增大压强
C、改用更好的催化剂 D、通入更多的CO
(5)25℃时以稀硫酸为电解质溶液制成甲醇燃料电池,则负极的电极方程式为_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com