
【题目】东晋![]() 华阳国志
华阳国志![]() 南中志
南中志![]() 卷四中已有关于白铜的记载,云南镍白铜
卷四中已有关于白铜的记载,云南镍白铜![]() 铜镍合金
铜镍合金![]() 闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)已知:丁二酮肟[HON=(CH3)CC(CH3)=NOH]是检验Ni2+的灵敏试剂。丁二酮肟分子中C原子轨道杂化类型为___,1mol丁二酮肟分子所含σ键的数目为___。
(2)单质铜及镍都是金属晶体;铜晶体的堆积方式为___;元素铜与镍的第二电离能分别为:ICu=1958kJ·mol-1、INi=1753kJ·mol-1,ICu>INi的原因是___。
(3)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构见图(1)。写出该反应的化学方程式:___。
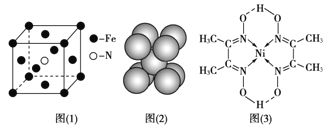
(4)下列关于铁和镍及其化合物说法正确的是___
a.金属镍能与CO形成配合物Ni(CO)4,常温下为液态,易溶于CCl4、苯等有机溶剂。所以Ni(CO)4固态时属于分子晶体
b.[Ni(NH3)6]SO4中阴离子的立体构型是正八面体
c.Ni2+和Fe2+的半径分别为69pm和78pm,则晶格能NiO>FeO,熔点NiO>FeO
d.铁晶胞结构见图(2),每个晶胞含有2个铁原子
(5)配合物Y的结构见图(3),Y中含有的化学键有___![]() 填序号
填序号![]() ;
;
a.极性共价键 b.非极性共价键 c.配位键 d.氢键 e.离子键 f.金属键
【答案】sp3和sp2 15NA或(9.03×1024) 面心立方堆积 铜失去的是全充满的3d10电子,镍失去的是4s1电子 8Fe+2NH3![]() 2Fe4N+3H2 acd abcd
2Fe4N+3H2 acd abcd
【解析】
![]() 丁二酮肟分子中C原子,甲基上碳原子价层电子对个数是4且不含孤电子对,为
丁二酮肟分子中C原子,甲基上碳原子价层电子对个数是4且不含孤电子对,为![]() 杂化,连接甲基的碳原子含有3个价层电子对且不含孤电子对,为
杂化,连接甲基的碳原子含有3个价层电子对且不含孤电子对,为![]() 杂化,丁二酮肟的结构式为
杂化,丁二酮肟的结构式为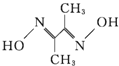 ,分子中含有13个单键,和2个双键,则共含有15个
,分子中含有13个单键,和2个双键,则共含有15个![]() 键,所以1mol丁二酮肟含有
键,所以1mol丁二酮肟含有![]() 键数目为
键数目为![]() 或
或![]()
故答案为:![]() 和
和![]() ;
;![]() 或
或![]() ;
;
![]() 由Cu晶体的晶胞图
由Cu晶体的晶胞图 可知,铜晶体的堆积方式为面心立方最密堆积,单质铜及镍都是金属晶体,都是由金属键形成的晶体,
可知,铜晶体的堆积方式为面心立方最密堆积,单质铜及镍都是金属晶体,都是由金属键形成的晶体,
元素铜与镍的第二电离能分别为![]()
![]() 、
、![]()
![]() ,
,![]() ,考虑到铜失去的是全充满的
,考虑到铜失去的是全充满的![]() 电子,镍失去的是
电子,镍失去的是![]() 电子,后者失去较前者容易,
电子,后者失去较前者容易,
故答案为:面心立方堆积;铜失去的是全充满的![]() 电子,镍失去的是
电子,镍失去的是![]() 电子;
电子;
![]() 该晶胞中铁原子个数
该晶胞中铁原子个数![]() ,氮原子个数是1,所以氮化铁的化学式是
,氮原子个数是1,所以氮化铁的化学式是![]() ,铁和氨气在
,铁和氨气在![]() 可发生置换反应生成氢气和氮化铁,所以该反应方程式为:
可发生置换反应生成氢气和氮化铁,所以该反应方程式为: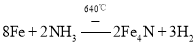 ,
,
故答案为: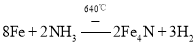 ;
;
![]() 因为
因为![]() 常温下为液态,易溶于
常温下为液态,易溶于![]() 、苯等有机溶剂,根据相似相溶原理知,固态
、苯等有机溶剂,根据相似相溶原理知,固态![]() 属于分子晶体,故a正确;
属于分子晶体,故a正确;
![]() 中阴离子
中阴离子![]() 中S原子的孤电子对数
中S原子的孤电子对数![]() ,价层电子对数
,价层电子对数![]() ,离子空间构型为正四面体,故b错误;
,离子空间构型为正四面体,故b错误;
![]() 影响离子晶体熔点的因素是晶格能,晶格能与离子半径成反比、与电荷数成正比,相同电荷时,离子半径越小,熔点越高,镍离子半径小于亚铁离子半径,所以氧化镍熔点高于氧化亚铁熔点,故c正确;
影响离子晶体熔点的因素是晶格能,晶格能与离子半径成反比、与电荷数成正比,相同电荷时,离子半径越小,熔点越高,镍离子半径小于亚铁离子半径,所以氧化镍熔点高于氧化亚铁熔点,故c正确;
![]() 铁晶胞中铁占据8个顶点和中心,根据均摊法确定其晶胞中的原子数为:
铁晶胞中铁占据8个顶点和中心,根据均摊法确定其晶胞中的原子数为:![]() ,故d正确;
,故d正确;
故答案为:acd;
![]() 根据图可知碳碳间形成非极性共价键、碳氮间为极性共价键,氮镍间为配位键,氧氢间形成氢键,无离子键、金属键,故选abcd,
根据图可知碳碳间形成非极性共价键、碳氮间为极性共价键,氮镍间为配位键,氧氢间形成氢键,无离子键、金属键,故选abcd,
故答案为:abcd。


 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:
【题目】H2O2(l)在有MnO2条件下和无MnO2条件下分解的能量变化如图所示。下列说法正确是

A. 有MnO2条件下的反应曲线是a曲线
B. a曲线变为b曲线,反应的活化分子百分数增大
C. a曲线变为b曲线,平衡时H2O2的转化率增大
D. b曲线的热化学方程式为:H2O2(l) =H2O(l) +1/2O2(g) ΔH= - ( E1 - E2)KJmol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图所示示意图,下列说法不正确的是( )
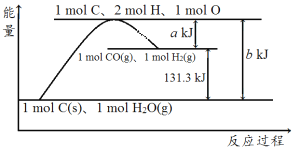
A.反应的热化学方程式可表示为C(s)+H2O(g)=CO(g)+H2(g) ΔH=(b-a) kJ·mol-1
B.该反应过程反应物断键吸收的能量大于生成物成键放出的能量
C.amol C和amol H2O(l)反应生成amol CO和a mol H2吸收的热量一定为131.3a kJ
D.1mol C、2mol H、1mol O转变成1mol CO(g)和1mol H2(g)放出的热量为a kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知0.1mol/L的醋酸溶液中存在电离平衡:CH3COOH![]() CH3COO-+H+要使溶液中
CH3COO-+H+要使溶液中![]() 值增大,可以采取的措施是( )
值增大,可以采取的措施是( )
A.加少量烧碱溶液B.降低温度
C.加少量冰醋酸D.加水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用98%的浓硫酸(其密度为1.84 g·cm-3)配制250 mL0.4 mol·L-1稀硫酸,有以下实验仪器供选:A 10mL量筒 B 托盘天平 C 玻璃棒 D 250 mL容量瓶 E 500 mL容量瓶 F 胶头滴管 G. 烧杯
(1)需量取浓硫酸的体积为___________mL。
(2)实验时不可选用的仪器有(填序号) __________________。
(3)配制过程中,下列情况会使配制结果偏高的是_____(填序号)
①容量瓶使用时未干燥;
②定容时俯视刻度线观察液面;
③将浓硫酸在烧杯中稀释后未经冷却就转移至容量瓶中,并定容;
④定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线。
(4)配置过程中,实验操作步骤为: __________
A.在烧杯中注入蒸馏水(溶液体积少于250mL),沿烧杯壁注入量取的浓硫酸用玻璃棒搅拌,使其混匀。
B.待稀释的硫酸冷却后,沿玻璃棒注入250mL的容量瓶中。
C.用量筒量取密度为1.84g/cm3质量分数为98%的浓硫酸。
D.用蒸馏水洗涤烧杯2~3次,将洗涤液注入容量瓶中。
E.往容量瓶中小心加蒸馏水至液面接近刻度1-2cm处,改用胶头滴管加蒸馏水,使溶液凹液面恰好与刻度线相切。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2H2(g)+O2(g)=2H2O(l) ΔH=-569.6kJ/mol,2H2O(g)=2H2(g)+O2(g) ΔH=+482.1 kJ/mol。现有1g液态H2O,蒸发时吸收的热量是 ( )
A. 2.43 kJ B. 4.86 kJ C. 43.8 kJ D. 87.5 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)由工业合成气(组成为H2、CO和少量的CO2)直接制备二甲醚,涉及以下四个可逆反应:
甲醇合成反应:
(i)CO(g) +2H2(g)==CH3OH(g) △H 1=-90.1kJ·mol-1;
(ii)CO2(g)+3H2(g)== CH3OH(g) +H2O(g) △H2=-49.0kJ·mol-1;
水煤气变换反应:(iii)CO(g)+ H2O(g)==CO2(g)+ H2(g) △H3=-41.1kJ·mol-1;
二甲醚合成反应:(iv)2CH3OH(g) ==CH3OCH3(g)+ H2O(g) △H4=-24.5kJ·mol-1;
①由H2和CO直接制备二甲醚(另一产物为水蒸气)的热化学方程式为____________________________。根据化学反应原理,分析增大压强对直接制备二甲醚反应的影响:___________________________________。
②反应( ii )的平衡常数表达式为K=______________。
(2)现以二甲醚燃料电池,采用电解法来处理酸性含铬废水(主要含有Cr2O72-),实验室利用如图2装置模拟该法:

①M电板(a为CO2)的电极反应式为________________________;电解池阳极的电极反应式为_______________________________________。
②请写出电解池中Cr2O72-转化为Cr3+的离子反应方程式:__________________________。
③已知25 ℃时,Ksp[Cr(OH)3]=6.4×10-31。一般以离子浓度≤1×10-5 mol/L作为该离子除尽的标准。处理废水时,最后Cr3+以Cr(OH)3形式除去,当溶液的pH=6时,c(Cr3+)=______,Cr3+ ___ (填“是”或“否”)被除尽。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据元素周期表和元素周期律,判断下列叙述不正确的是

A. 气态氢化物的稳定性:H2O>NH3>SiH4
B. 氢元素与其他元素可形成共价化合物或离子化合物
C. 上图所示实验可证明元素的非金属性:Cl>C>Si
D. 用中文“![]() ”(ào)命名的第118号元素在周期表中位于第七周期0族
”(ào)命名的第118号元素在周期表中位于第七周期0族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016 年 IUPAC 命名 117 号元素为 Ts,已知 Ts 位于第七周期,其原子核外最外层电子数为 7。下列说法正确的是( )
A.Ts的同位素原子具有不同的核外电子数
B.Ts 元素具有放射性
C.Ts 在同族元素中非金属性最强
D.中子数为 176 的 Ts 核素符号为![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com