
回答下列问题。
(1)如下图,某温度(t℃)时水的图像如下,a点离子积KW= mol2·L-2;该温度下,pH=12的NaOH与pH=2的H2SO4等体积混合,溶液显 性。
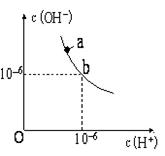
(2)25℃时,向0.1 mol·L-1氨水中加入少量NH4Cl固体,当固体溶解后,测得溶液pH ,NH4+的物质的量浓度 。(填增大、减小或不变)
(3)体积相等的稀NaOH和CH3COOH溶液混合,若溶液中c(Na+)=c(CH3COO-),则该溶液显 (填“酸性”、“碱性”、“中性”),则混合前c(NaOH)
c(CH3COOH)(填“>”、“<”或“=”)。
(4)常温时,Fe(OH)3的Ksp=1×10-38,要使溶液中的Fe3+沉淀完全(残留在溶液中的c(Fe3+)<10-5 mol·L-1),则溶液的pH最小为 。
(5)用可溶性碳酸盐,可以浸取CaSO4固体,则溶浸过程中会发生反应:
CaSO4(s)+CO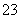 (aq)
(aq)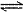 CaCO3(s)+SO
CaCO3(s)+SO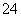 (aq)。
(aq)。
已知298 K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,则此温度下该反应的平衡常数K为 (计算结果保留三位有效数字)。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
通常情况下,微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀。请回答:
(1)用化学符号表示下列4种微粒:
A: B : C: D :
(2)写出A、B、E三种微粒反应的离子方程式:
、
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的数值。下列说法正确的是(用到的相对原子质量:H 1 O16 Al27)
A.18g 2H2O含有10NA个电子
B.1mol苯含有6NA个C-H键
C.常温常压下,22. 4L NH3约含有NA个NH3分子
D.27 g铝片投入足量浓H2SO4中生成1.5NA个SO2分子
查看答案和解析>>
科目:高中化学 来源: 题型:
下列过程或现象与水解无关的是
A.纯碱溶液去油污 B.配制氯化铁溶液时加入少量的盐酸
C.NaHCO3与Al2(SO4)3混合作泡沫灭火剂 D.铁在潮湿的环境下生锈
查看答案和解析>>
科目:高中化学 来源: 题型:
某新型手机采用甲醇-氧气燃料电池,以强碱溶液作为电解质,可连续使用一个月。该电池反应为:2CH3OH+3O2+4OH-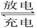 2CO
2CO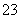 +6H2O,则有关说法正确的是
+6H2O,则有关说法正确的是
A.充电时阴极发生氧化反应
B.放电时负极的电极反应式为CH3OH+8OH--6e-===CO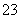 +6H2O
+6H2O
C.通入0.25 mol氧气并完全反应后,有0.5 mol e-转移
D.放电一段时间后,通入氧气的电极附近溶液的pH升高
查看答案和解析>>
科目:高中化学 来源: 题型:
某硫原子的质量是a g,12C原子的质量是b g,若NA只表示阿伏加德罗常数的数值,则下列说法中正确的是
①该硫原子的相对原子质量为aNA
②m g该硫原子的物质的量为m/a mol
③该硫原子的摩尔质量是aNA g·mol-1
④a g该硫原子所含有的电子数为16
A.①②③ B.①②④ C.②③④ D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
硫代硫酸钠可作为脱氯剂,已知25.0 mL 0.100 mol·L-1Na2S2O3溶液恰
好把224 mL(标准状况下)Cl2完全转化为Cl-,则S2O32—将转化为
A.S2- B.S C.SO32— D.SO42—
查看答案和解析>>
科目:高中化学 来源: 题型:
判断存放的FeCl2溶液是否变质。从现象观察看 ;鉴定的方法为加入 试剂,若溶液出现 ;则证明有 存在。实验室为了防止FeCl2溶液变质,在配制时常加入 。向FeSO4溶液中滴加NaOH溶液,并放置一段时间,此过程中观察到的现象 。
查看答案和解析>>
科目:高中化学 来源: 题型:
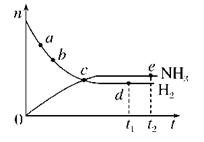 合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g)+3H2(g)
合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g)+3H2(g)  2NH3(g)(正反应为放热反应),673 K、30 MPa下,n(NH3)和n(H2)随时间t变化的关系示意图如图所示。下列叙述中正确的是( )
2NH3(g)(正反应为放热反应),673 K、30 MPa下,n(NH3)和n(H2)随时间t变化的关系示意图如图所示。下列叙述中正确的是( )
A. c点处正反应速率和逆反应速率相等
B. a点处正反应速率比b点处的大
C. d点(t1时刻)和e点(t2时刻)处n(N2)不同
D. t2时刻,正反应速率大于逆反应速率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com