
【题目】电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率变化可以确定滴定反应的终点。在一定温度下,用 0.1 mol·L-1KOH溶液分别滴定体积均为 20 mL、浓度均为 0.1 mol·L-1的盐酸和醋酸溶液,滴定曲线如图所示。下列有关判断正确的是
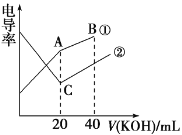
A.①表示的是 KOH溶液滴定盐酸溶液
B.A点的溶液中有c(CH3COO-)+c(OH-)-c(H+)=0.1mol/L
C.C 点水电离的 c(OH-)小于 A 点水电离的 c(OH-)
D.在B点的溶液中有:c(CH3COO-)>c(K+)>c(H+)>c(OH-)
【答案】C
【解析】
溶液电导率与离子浓度成正比,HCl是强电解质,醋酸是弱电解质,因此相同浓度的盐酸和醋酸,盐酸中离子浓度大于醋酸,盐酸的电导率较大,根据图像,推出①是醋酸和KOH的混合,②是HCl和KOH的混合,据此分析;
A、溶液电导率与离子浓度成正比,HCl是强电解质,醋酸是弱电解质,因此相同浓度的盐酸和醋酸,盐酸中离子浓度大于醋酸,盐酸的电导率较大,根据图像,推出①是醋酸和KOH的混合,②是HCl和KOH的混合,故A错误;
B、A点溶液中,醋酸和KOH恰好完全反应,生成CH3COOK,根据电荷守恒,c(CH3COO-)+c(OH-)-c(H+)=c(K+),A点溶液的体积增加一倍,则离子浓度降为原来的一半,即c(CH3COO-)+c(OH-)-c(H+)=c(K+)=0.05mol·L-1,故B错误;
C、C点代表HCl和KOH恰好完全反应,溶质为KCl,对水的电离无影响,A点溶质为CH3COOK,促进水的电离,即C点水电离的c(OH-)小于A点水电离的c(OH-),故C正确;
D、B点溶质为CH3COOK和KOH,且两者物质的量相等,溶液显碱性,CH3COO-水解,但程度非常微弱,因此离子浓度大小顺序是c(K+)>c(OH-)>c(CH3COO-) >c(H+),故D错误;
答案为C。


 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】设![]() 为阿伏加德罗常数的值。下列说法不正确的是
为阿伏加德罗常数的值。下列说法不正确的是![]()
![]()
A.![]() 和
和![]() 于密闭容器中充分反应后,其分子总数为
于密闭容器中充分反应后,其分子总数为![]()
B.标准状况下,![]() 某气体含有的分子数为Y,则
某气体含有的分子数为Y,则![]() 该气体的体积为
该气体的体积为![]()
C.常温下,![]() 质量分数为
质量分数为![]() 的乙炔的苯溶液中,含有碳原子的数目为
的乙炔的苯溶液中,含有碳原子的数目为![]()
D.氢氧燃料电池正极消耗![]() 气体时,负极消耗的气体分子数为
气体时,负极消耗的气体分子数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若NA表示阿伏加德罗常数,下列叙述中正确的是 ( )
A.标准状况下,22.4L SO3含NA个分子
B.含0.4mol HCl的浓盐酸与足量二氧化锰反应转移电子数为0.2NA
C.32gCu与足量硫完全反应,转移的电子数为0.5NA
D.在200mL 5mol·L-1 AlCl3溶液中,Al3+数目为NA,等于Cl-数目的1/3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应2A(g)+2B(g)![]() C(g)+2D(g),在容器均为2L的甲,乙,丙三个恒温(反应温度分别为300℃,T℃,300℃)容器中分别加入物质的量之比为1:1的A和B,测得各容器中n(B)随反应时间t的变化情况如下表所示:
C(g)+2D(g),在容器均为2L的甲,乙,丙三个恒温(反应温度分别为300℃,T℃,300℃)容器中分别加入物质的量之比为1:1的A和B,测得各容器中n(B)随反应时间t的变化情况如下表所示:
0 | 40 | 80 | 120 | 160 | |
甲 | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
乙 | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
丙 | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
根据表中数据,下列说法正确的是
A.乙容器中的反应温度T<300
B.丙容器中,0-40min内用A的浓度变化表示的平均反应速率为为0.05mol/(L·min)
C.若起始时向甲容器中加入0.2、0.2、0.4和1.2,则反应将向正反应方向进行
D.在0-40min内,提高乙容器中的A的转化率的有效途径是使用高效催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钨是熔点最高的金属,是重要的战略物资。自然界中钨主要存在于黑钨矿中,其主要成分是铁和锰的钨酸盐(FeWO4、MnWO4),还含少量Si、As的化合物。由黑钨矿冶炼钨的工艺流程如图1:
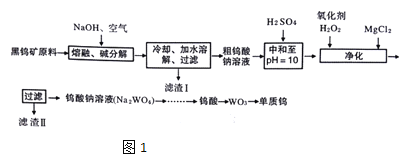
已知:
①滤渣I的主要成份是Fe2O3、MnO2
②上述流程中,钨的化合价只有在最后一步发生改变。
③常温下钨酸难溶于水。
(1)钨酸盐(FeWO4、MnWO4)中钨元素的化合价为___,请写出MnWO4在熔融条件下发生碱分解反应生成Fe2O3的化学方程式___
(2)上述流程中向粗钨酸钠溶液中加硫酸中和至pH=10后,溶液中的杂质阴离子确SiO32-、HAsO32-、HAsO42-等,则“净化”过程中,加入H2O2时发生反应的离子方程式为___,滤渣Ⅱ的主要成分是___
(3)已知氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,两者的溶解度均随温度升高而减小。图2为不同温度下Ca(OH)2、CaWO4的沉淀溶解平衡曲线,则:
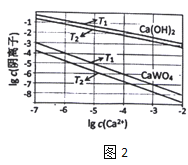
①T1___T2(填“>”或“<”)T1时Ksp(CaWO4)=___
②将钨酸钠溶液加入石灰乳得到大量钨酸钙,发生反应的离子方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:ZnS呈白色,CuS呈黑色;常温下,Ksp(ZnS)=3.0×10-25,Ksp(CuS)=1.0×10-36;pM=-lgc(M2+)。常温下,向10.0mL0.20molL-1ZnCl2溶液中逐滴滴加0.10molL-1Na2S溶液,溶液中pM与加入Na2S溶液的体积(V)的关系如图所示。下列说法不正确的是( )
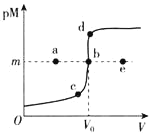
A.V0=20.0mL,m=12.5-![]() lg3
lg3
B.相同实验条件下,若用10.0mL0.20molL-1CuCl2溶液代替上述ZnCl2溶液,则反应终点b向d方向移动
C.若c(ZnCl2)=0.10molL-1,则反应终点可能为e点
D.向b点浊液中加入0.002molCuCl2固体,白色沉淀变黑色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图分别是A、B两种物质的核磁共振氢谱,已知A、B两种物质都是烃类,都含有6个氢原子,试根据两种物质的核磁共振氢谱推测A、B有可能是下面的
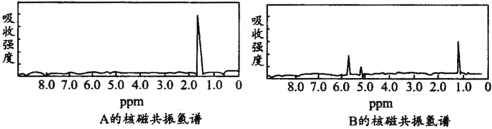
A.C3H6,C6H6B.C2H6,C3H6C.C6H6 ,C2H6D.C3H6,C2H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向10mL0.1mol/L的某一元酸HR溶液中逐滴加入0.1mol/L氨水,所得溶液pH及导电能力变化如图。下列分析不正确的是( )

A. a~b点导电能力增强说明HR为弱酸
B. a、b点所示溶液中水的电离程度不相同
C. b恰好完全中和,pH=7说明NH4R没有水解
D. c 点溶液存在c(NH4+)>c(R-)、c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C 为中学常见单质,其中一种为金属;通常情况下,A 为固体,B 为液体,C 为气体。D、 E、F、G、H、X 均为化合物,其中 X 是一种无氧强酸、E 为黑色固体,H 在常温下为液体。它们之间的 转化关系如图所示(其中某些反应条件和部分反应物已略去)。

(1)写出化学式:A____________、D__________、E__________、X________。
(2) 在反应①~⑦中,不属于氧化还原反应的是__________(填编号)。
(3) 反应⑥的离子方程式为__________。
(4)反应⑦的化学方程式为__________,该反应中每消耗 0.3molA,可转移电子__________mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com