
【题目】微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。下列有关微生物电池的说法错误的是

A. 正极反应中有CO2生成
B. 微生物促进了反应中电子的转移
C. 质子通过交换膜从负极区移向正极区
D. 电池总反应为C6H12O6+6O2=6CO2+6H2O
科目:高中化学 来源: 题型:
【题目】水是最普通、最常见的物质之一。
(1)“水”有很多种。下列“水”属于纯净物的是 ________ (填字母序号)。
A.河水 B.自来水 C.矿泉水 D.蒸馏水
(2)电解水可证明水由氢、氧两种元素组成,该反应的化学方程式为________ 。
(3)水是重要的溶剂和化工原料。氯碱工业以饱和食盐水为原料获得烧碱等化工产品,反应原理为:![]() 。
。
①20℃时,NaCl 的溶解度是36 g。该温度下,饱和食盐水中溶质与溶剂的质量比为______。
②烧碱可用于处理硫酸泄漏,反应的化学方程式为__________。
(4)水在化学实验中具有重要作用。将铁丝放在潮湿的空气中(如下图所示),一段时间后,观察到导管内液面下降,导管口有气泡冒出,关闭 K。请解释导管内液面上升和下降的原因:___________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与科技、社会、生产、生活等关系密切,下列有关说法不正确的是( )
A.部分卤代烃可用作灭火剂
B.福尔马林(甲醛溶液)可用于浸泡生肉及海产品以防腐保鲜
C.提倡人们购物时不用塑料袋,是为了防止白色污染
D.石油分馏是物理变化,可得到汽油、煤油和柴油等产品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于同分异构体数目的叙述不正确的是( )
A. 甲苯苯环上的1个氢原子被含3个碳原子的烷基取代,所得产物有6种
B. 已知丙烷的二氯代物有4种异构体,则其六氯代物的异构体数目也为4种
C. 含有5个碳原子的某饱和链烃,其一氯代物有3种
D. 菲的结构为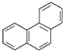 ,它与硝酸反应,可生成5种一硝基取代物
,它与硝酸反应,可生成5种一硝基取代物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,分离提纯的方法不正确的是( )
选项 | 实验 | 分离、提纯方法 |
A | 提纯粗苯甲酸 | 重结晶 |
B | 分离乙醇和丁醇 | 蒸馏 |
C | 除去乙炔中的H2S气体 | 用CuSO4溶液洗气 |
D | 提纯硝基苯 | 碱洗分液-水洗分液-蒸馏 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,许多专家对石灰氮重新进行了深入研究,这也使得石灰氮这一古老的肥料又焕发了新的活力。石灰氮是由Ca、N、C等三种元素组成的盐,其含钙、氮的质量分数分别为50%、35%。石灰氮完全水解后的产物是固体A和气体B,其中B是制取氮肥的主要原料。固体A在高温下分解生成D和气体C。B的催化氧化产物为E和F,F继续氧化后的产物G遇到E生成一种工业强酸。将G和F的混合物溶解在接近零度的水中,即生成亚硝酸的水溶液,该反应可表示如下:G+F+H2O=2HNO2(已配平)。
请回答下列问题:
(1)石灰氮的化学式为_____________。
(2)写出足量B和C与饱和氯化钠溶液反应的化学方程式:__________________。
(3)亚硝酸(HNO2)是一种与醋酸酸性相当的弱酸,很不稳定,通常在室温下立即分解。在酸性条件下,当NaNO2与KI按物质的量1:1恰好完全反应,且I— 被氧化为I2时,含氮产物为_________(填化学式)。要得到稳定HNO2溶液,可以往冷冻的浓NaNO2溶液中加入或通入某种物质,下列物质不适合使用是__________(填序号)。
a. 磷酸 b. 二氧化碳 c. 稀硫酸 d. 二氧化硫 e. 次氯酸
(4)工业废水中的NO2― 可用铝粉除去。已知此反应体系中包含Al、NaAlO2、NaNO2、NaOH、NH3、H2O六种物质。写出上述反应的离子方程式:____________________________。若改用电解法将废水中NO2— 转换为N2除去,N2将在________(填电极名称)生成。
(5)某研究小组学生提出检验火柴头上KClO3实验方案如下:

有关的离子反应方程式为__________________________________________。
(6)在(5)方案基础上,要确定火柴头中含KClO3,还需进行的实验操作为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。现有一定量铝粉和铁粉的混合物与一定体积某浓度的稀硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入5 mol·L-1的NaOH溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量关系如下图所示:
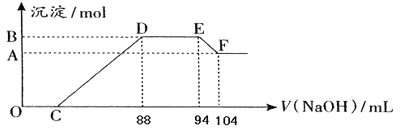
(1)B与A的差值为________mol。
(2)C点对应的溶液体积为________mL。
(3)原硝酸溶液中含硝酸的物质的量为________mol。
(4)铝粉和铁粉的混合物中铝粉与铁粉的物质的量之比为_______________。
(5)写出铝与该浓度硝酸反应的离子方程式_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向X溶液中加入Y试剂,产生沉淀的示意图与下图所示情形吻合的是(注意线段的斜率)
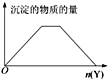
A. 向NaOH和Ca(OH)2的混合溶液中通入CO2
B. 向HCl和AlCl3的混合溶液中滴加NaOH
C. 向NH4Al(SO4)2溶液中滴加NaOH
D. 向NH4Cl和MgCl2的混合溶液中滴加NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
Zn 在现代工业中对于电池制造有不可磨灭的地位,锌还是人体必需的微量元素之一,在人体生长发育、生殖遗传、免疫、内分泌等重要生理过程中起着极其重要的作用。
(l)元素Zn在周期表中的位置为_____,基态Zn原子的电子排布式为_____。
(2)在[Zn(NH3)4]2+中,Zn2+提供4s和4p共四个空轨道,与4个NH3分子形成_____键,Zn2+采取sp3杂化,预测[Zn(NH3)4]2+的空间构型为______。
(3)金属Zn晶体密置层采取…ABAB…方式堆积,其堆积方式名称为:______,配位数为:____。
(4)闪锌矿(ZnS )晶胞如图所示
白球为S2-离子、黑球为Zn2+离子,与Zn2+距离最近的四个S2-所围成的空间构型为_____,若晶胞参数为a,则Zn2+与S2-最近距离为______(用含a的代数式表示)。

(5)具有相似晶胞结构的ZnS和ZnO,ZnS熔点为1830℃,ZnO熔点为1975℃,后者较前者高是由于______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com