
【题目】实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。现有一定量铝粉和铁粉的混合物与一定体积某浓度的稀硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入5 mol·L-1的NaOH溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量关系如下图所示:
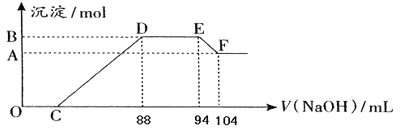
(1)B与A的差值为________mol。
(2)C点对应的溶液体积为________mL。
(3)原硝酸溶液中含硝酸的物质的量为________mol。
(4)铝粉和铁粉的混合物中铝粉与铁粉的物质的量之比为_______________。
(5)写出铝与该浓度硝酸反应的离子方程式_______________________。
【答案】 0.05 40 0.5 5∶3 8Al+3OH++3NO![]() ===8Al3++3NH
===8Al3++3NH![]() +9H2O
+9H2O
【解析】考查化学计算,(1)E→F发生Al(OH)3+OH-=AlO2-+2H2O,B与A的差值为Al(OH)3的物质的量,即物质的量为(104-94)×10-3×5mol=0.05mol;(2)O到C没有沉淀产生,说明HNO3过量,D→E发生NH4++OH-=NH3·H2O,推出n(NH4+)=(94-88)×10-3×5mol=0.03mol,根据得失电子数目守恒,因此有n(Al)×3+n(Fe)×3=n(NH4+)×8,代入数值,解得n(Fe)=0.03mol,C→D发生Al3++3OH-=Al(OH)3↓、Fe3++3OH-=Fe(OH)3↓,此阶段共消耗NaOH的体积为(0.03+0.05)×3×1000/5mL=48mL,因此C点对应的数值为(88-48)mL=40mL;(3)E点溶质为NaNO3,因此n(NO3-)=94×10-3×5mol=0.47mol,根据N元素守恒,因为合金与硝酸反应过程中没有气体产生,因此原硝酸溶液中n(HNO3)=n(NO3-)+n(NH4+)=(0.47+0.04)mol=0.5mol;(4)根据(2)的分析,合金中铝粉和铁粉的物质的量比值为0.05:0.03=5:3;(5)根据上述分析,硝酸被还原成NH4+,因此离子反应方程式为:8Al+3OH++3NO3- =8Al3++3NH4+ +9H2O。


科目:高中化学 来源: 题型:
【题目】下利说法正确的是(NA表示阿伏加德罗常数的值)
①28g氮气所含有的原子数目为NA
②4g金属钙变成钙离子时失去的电子数目为0.1 NA
③在常温常压下,11.2LN2含有含有的分子数为0.5NA
④在标况下,1 molNe含有的原子数为NA
⑤0.5 mol单质铝与足量盐酸反应转移电子数为1.5NA
⑥标准状况下,1 L水所含分子数为1 /22.4NA
⑦17g氨气所含电子数目为10NA
A. ①②⑤⑥⑦ B. ①②④⑤⑥ C. ⑤⑦ D. ④⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸钠在轻工、建材、纺织、国防、医药等工业中有重要的应用。
(1)工业碳酸钠(纯度约为98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO![]() 等杂质,提纯工艺线路如下:
等杂质,提纯工艺线路如下:
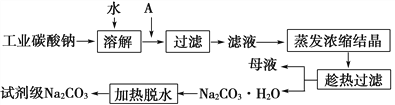
碳酸钠的饱和溶液在不同温度下析出的溶质如图所示:
![]()
请回答下列问题:
①试剂A是________,“母液”中除了含有Na+、CO![]() 、OH-外,还含有________等离子,过滤要“趁热”的目的是____________________________。
、OH-外,还含有________等离子,过滤要“趁热”的目的是____________________________。
②检验试剂级Na2CO3中Cl-和SO![]() 是否除尽,选用的试剂及加入的先后次序是________(填字母)。
是否除尽,选用的试剂及加入的先后次序是________(填字母)。
a.HCl、BaCl2、AgNO3
b.AgNO3、HNO3、Ba(NO3)2
c.HNO3、Ba(NO3)2、AgNO3
d.AgNO3、HCl、BaCl2
(2)“侯氏制碱法”的原理:NaCl+NH3+CO2+H2O===NaHCO3↓+NH4Cl
如图是某兴趣小组在实验室中模拟“侯氏制碱法”制取NaHCO3所用到的主要装置。
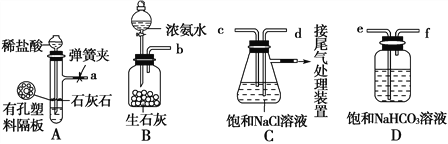
请回答下列问题:
①各仪器口的连接顺序为a接___________________________________接b,实验时先向NaCl溶液中通入较多的NH3,再通入足量的CO2,其原因是________(填字母)。
a.使CO2更易被吸收
b.NH3比CO2更易制取
c.CO2的密度比NH3大
②将生成的NaHCO3晶体从混合物中分离出来需要的玻璃仪器是_______________。
③该兴趣小组用如图装置比较C、N、Si三种元素的非金属性强弱,B中的试剂是________,能说明碳的非金属性比硅强的实验现象是_______________________(H2SiO3是一种不溶于水的白色胶状物)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。下列有关微生物电池的说法错误的是

A. 正极反应中有CO2生成
B. 微生物促进了反应中电子的转移
C. 质子通过交换膜从负极区移向正极区
D. 电池总反应为C6H12O6+6O2=6CO2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.需要加热才能发生的化学反应不一定是吸热反应
B.放热反应在常温下一定很容易发生
C.在一定条件下,某一化学反应是吸热反应还是放热反应,由生成物与反应物的焓值差即焓变(ΔH)决定
D.化学反应除了生成新的物质外,还伴随着能量的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列所得溶液的物质的量浓度等于0.1molL-1的是
A. 将16gCuSO4·5H2O充分溶解,配成1L溶液中
B. 将25gCuSO4·5H2O充分溶解,配成1L溶液
C. 将16gCuSO4充分溶解在1L水中
D. 将25gCuSO4·5H2O充分溶解在1L水中
查看答案和解析>>
科目:高中化学 来源: 题型:
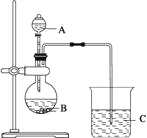
【题目】某研究性学习小组讨论甲、乙、丙、丁四种仪器装置的有关用法,其中不合理的是( )

A. 甲装置:可用来证明碳的非金属性比硅强
B. 乙装置:橡皮管的作用是能使水顺利流下
C. 丙装置:用图示的方法不能检查此装置的气密性
D. 丁装置:先从①口进气集满二氧化碳,再从②口进气,可收集氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A. 将铜丝插入稀硝酸中:Cu+4H++2NO![]() ===Cu2++2NO2↑+H2O
===Cu2++2NO2↑+H2O
B. NaHCO3溶液中加少量Ba(OH)2溶液:HCO![]() +Ba2++OH-===BaCO3↓+H2O
+Ba2++OH-===BaCO3↓+H2O
C. 硫化钠水溶液呈碱性:S2-+2H2O===H2S↑+2OH-
D. 在酸性碘化钾溶液中滴加双氧水:2I-+2H++H2O2===I2+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的氢化物有多种,在科学技术和生产中有重要的应用。根据题意完成下列计算:
(1)某氮的氢化物的相对分子质量为43.0,其中氮原子的质量分数为0.977,确定该氢化物的分子式为____________。该氢化物受撞击则完全分解为氮气和氢气。4.30 g该氢化物受撞击后产生的气体在标准状况下的体积为____________L。
(2)氨的水溶液可用于吸收NO与NO2混合气体,反应方程式为
6NO+4NH3=5N2+6H2O① 6NO2+ 8NH3=7N2+12H2O②
反应①中氧化剂是__________,还原剂与还原产物物质的量之比_______________;如NO与NO2混合气体87g被过量氨水(质量分数0.300)完全吸收,产生50.4L氮气(标准状况下测定),则计算混合气体中NO与NO2的体积比为多少____________?(要求写计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com