
【题目】已知H2A为二元弱酸。室温时,配制一组c(H2A)+c(HA-) +c(A2-)=0. 100mol·L-1的H2A和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如下图所示。下列指定溶液中微粒的物质的量浓度关系不正确的是

A. pH=2 的溶液中:c(H2A)+c(A2-)>c(HA- )
B. E点溶液中:c(Na+)-c(HA-)< 0. 100 mol L-1
C. c(Na+)= 0.100 mol·L-1的溶液中:c(H+) + c(H2A)=c(OH-)+c(A2-)
D. pH=7的溶液中:c(Na+)>2c(A2- )
【答案】A
【解析】A、根据图像,可以得知pH=2时c(HA-)>c(H2A)+c(A2-),故A说法错误;B、E点:c(A2-)=c(HA-), 根据电荷守恒:c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-),此时的溶质为Na2A、NaHA,根据物料守恒,2n(Na+)=3n(A),即2c(Na+)=3c(A2-)+3c(HA-)+3c(H2A),两式合并,得到c(Na+)-c(HA-)=[c(HA-)+3c(H2A)+c(A2-)]/2,即c(Na+)-c(HA-)=0.1+c(H2A),c(Na+)-c(HA-)< 0. 100 mol·L-1,故B说法正确;C、根据物料守恒和电荷守恒分析,当c(Na+)=0.1mol·L-1溶液中:c(H+) + c(H2A)=c(OH-)+c(A2-),故C说法正确;D、根据电荷守恒,c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-),pH=7,说明c(H+)=c(OH-),即c(Na+)=c(HA-)+2c(A2-),因此有c(Na+)>2c(A2- ),故D说法正确。


 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案科目:高中化学 来源: 题型:
【题目】膜技术原理在化工生产中有着广泛的应用。有人设想利用电化学原理制备少量硫酸和绿色硝化剂N2O5,装置图如下。

(1)A装置是__________,B装置是_____________(填“原电池”或“电解池”)。
(2)N2O5在电解池的_____(填“c极”或“d极”)区生成,其电极反应式为______________。
(3)A装置中通入O2的一极是____极,其电极反应式为_________________;通入SO2的一极是_____极,其电极反应式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将浓度均为0.1 mol·L-1、体积分别为Va和Vb的HX溶液与NH3·H2O溶液按不同体积比混合,保持Va+Vb=100mL,Va、Vb与混合液的pH的关系如图所示。下列说法不正确的是
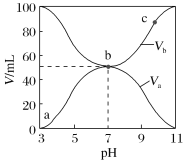
A. Ka(HX)的值与Kb(NH3·H2O)的值相等
B. b点,c(NH4+)+c(HX)=0.05 mol·L-1
C. a→c点过程中,  值不变
值不变
D. a、b、c三点,c点时水电离出的c(H+)最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质得不同。下列事实不能说明上述观点的是( )
A. 甲苯能使酸性KMn04溶液褪色,甲基环己烷不能使酸性KMn04溶液褪色
B. 乙烯能与溴水发生加成反应,而乙烷不能与溴水发生加成反应
C. 苯与浓硝酸反应生成硝基苯,而甲苯与浓硝酸反应生成三硝基甲苯
D. 苯酚( )可以与NaOH反应,而乙醇(CH3CH2OH)不能与NaOH反应
)可以与NaOH反应,而乙醇(CH3CH2OH)不能与NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某另类元素周期表的一部分,下列说法正确的是( )

A. 简单阴离子的半径大小:X>Y>Z
B. 单质的氧化性:X>Y>Z
C. Y的氢化物只有一种
D. X的最高价氧化物对应的水化物为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“低碳经济”已成为全世界科学家研究的重要课题。为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究。
(1)已知:①CO(g)+H2O(g)![]() H2(g)+CO2(g) ΔH=-41 kJ·mol-1
H2(g)+CO2(g) ΔH=-41 kJ·mol-1
②C(s)+2H2(g) ![]() CH4(g) ΔH=-73 kJ·mol-1
CH4(g) ΔH=-73 kJ·mol-1
③2CO(g) ![]() C(s)+CO2(g) ΔH=-171 kJ·mol-1
C(s)+CO2(g) ΔH=-171 kJ·mol-1
写出CO2与H2反应生成CH4和H2O(g)的热化学方程式:____
(2)目前工业上有一种方法是用CO2来生产燃料甲醇。为探究该反应原理,在容积为2 L密闭容器中,充入1 mol CO2和3.25 mol H2在一定条件下发生反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化如图所示:
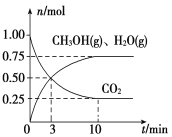
①从反应开始到平衡,氢气的平均反应速率v(H2)=________。
②下列措施一定不能使CO2的平衡转化率增大的是________。
A 在原容器中再充入1 mol CO2
B 在原容器中再充入1 mol H2
C 在原容器中充入1 mol氦气
D 使用更有效的催化剂
E 缩小容器的容积
F 将水蒸气从体系中分离
(3)煤化工通常研究不同条件下CO转化率以解决实际问题。已知在催化剂存在条件下反应:CO(g)+H2O(g) ![]() H2(g)+CO2(g)中CO的平衡转化率随p(H2O)/p(CO)及温度变化关系如图所示:
H2(g)+CO2(g)中CO的平衡转化率随p(H2O)/p(CO)及温度变化关系如图所示:

①上述反应的正反应方向是________反应(填“吸热”或“放热”);
②对于气相反应,用某组分(B)的平衡压强(pB)代替物质的量浓度(cB)也可以表示平衡常数(记作Kp),则该反应的Kp=_____(填表达式,不必代数计算);如果提高p(H2O)/p(CO),则Kp_______(填“变大”“变小”或“不变”)。使用铁镁催化剂的实际工业流程中,一般采用400 ℃左右、p(H2O)/p(CO)=3~5,采用此条件的原因可能是_______
(4)科学家用氮化镓材料与铜组装成如图所示的人工光合系统,利用该装置实现了用CO2和H2O合成CH4。下列关于该电池的叙述错误的是________。

A.该装置能量转化形式仅存在将太阳能转化为电能
B.铜电极为正极,电极反应式为CO2+8e-+8H+===CH4+2H2O
C.电池内部H+透过质子交换膜从左向右移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱性电池具有容量大、放电电流大的特点而得到广泛应用。锌锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:![]() ,下列说法错误的是
,下列说法错误的是
A. 电池工作时,锌失去电子
B. 用该电池电解水时,电子通过外电路流向电解池阳极
C. 电池正极电极反应式![]()
D. 外电路中每通过0.2mol电子,锌的质量理论上减小6.5g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)高铁酸钾![]() 不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。总反应式为
不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。总反应式为![]()
![]()
![]() ,如图是高铁电池的模拟实验装置:
,如图是高铁电池的模拟实验装置:

①该电池盐桥中盛有饱和![]() 溶液,此盐桥中氯离子向______(填“左”或“右”)移动。
溶液,此盐桥中氯离子向______(填“左”或“右”)移动。
②该电池放电时正极的电极反应式为______;充电时每转移0.3mol电子,有______mol![]() 生成,正极附近溶液的碱性______(填“增强”,“不变”或“减弱”)。
生成,正极附近溶液的碱性______(填“增强”,“不变”或“减弱”)。

③上图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有_________________。
(2)“![]() ”电池可将
”电池可将![]() 变废为宝。我国科研人员研制出的可充电“
变废为宝。我国科研人员研制出的可充电“![]() ”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为
”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为![]()
![]()
![]() 。放电时该电池“吸入”
。放电时该电池“吸入”![]() ,其工作原理如图所示:
,其工作原理如图所示:

①充电时,正极的电极反应式为________________________________。
②放电时,若生成的![]() 和
和![]() 全部沉积在电极表面,当转移0.2mol
全部沉积在电极表面,当转移0.2mol![]() 时,两极的质量差为______。
时,两极的质量差为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微型银-锌电池可用作电子仪器的电源,其电极分别是![]() 和
和![]() ,电解质为
,电解质为![]() 溶液,电池总反应为
溶液,电池总反应为![]() ,下列说法正确的是( )
,下列说法正确的是( )
A. 电池工作过程中,![]() 溶液浓度降低
溶液浓度降低
B. 电池工作过程中,电解液中![]() 向负极迁移
向负极迁移
C. 负极发生反应![]()
D. 正极发生反应![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com