
【题目】中国海军航母建设正在有计划、有步骤向前推进,第一艘国产航母目前正在进行海试。建造航母需要大量的新型材料。航母的龙骨要耐冲击,航母的甲板要耐高温,航母的外壳要耐腐蚀。
(1)镍铬钢抗腐蚀性能强,Ni2+基态原子的核外电子排布为_______,铬元素在周期表中______区。
(2)航母甲板涂有一层耐高温的材料聚硅氧烷结构如图所示,其中C原子杂化方式为_______杂化。
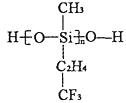
(3)海洋是元素的摇篮,海水中含有大量卤族元素。
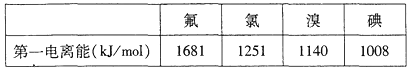
①根据下表数据判断:最有可能生成较稳定的单核阳离子的卤素原子是______填元素符号
②根据价层电子对互斥理论,预测ClO3-的空间构型为______形,写出一个ClO3-的等电子体的化学符号______。
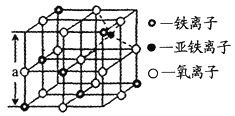
(4)海底金属软泥是在洋海底覆盖着的一层红棕色沉积物,蕴藏着大量的资源,含有硅、铁、锰、锌等。如右图是从铁氧体离子晶体Fe3O4中取出的能体现其晶体结构的一个立方体,则晶体中的离子是否构成了面心立方最密堆积?_____(填“是”或“否”);该立方体是不是Fe3O4的晶胞?______(填“是”或“否”);立方体中铁离子处于氧离子围成的_______(填空间结构)空隙;根据下图计算Fe3O4晶体的密度为________g/cm3。(图中a=0.42nm,计算结果保留两位有效数字)
【答案】1s22s22p63s23p63d8 d sp3 Ⅰ 三角锥 SO32- 是 是 正八面体 5.2
【解析】
(1)Ni处于周期表中第四周期第ⅤⅢ族,是d区金属元素;
(2)聚硅氧烷中C形成4个单键;
(3)①根据第一电离能分析,第一电离能越小,越容易生成较稳定的单核阳离子;
②根据VSEPR理论判断ClO3-的空间构型,价电子对数为VP=BP+LP,等电子体是指原子总数相同,价电子总数也相同的微粒;
(4)根据O2-的坐标分析,根据晶胞粒子的排布,该立方体不是Fe3O4的晶胞,立方体中Fe3+处于O2-围成的正八面体空隙,根据密度公式ρ=![]() 计算。
计算。
(1)Ni处于周期表中第四周期第ⅤⅢ族,Ni2+基态原子的核外电子排布为1s22s22p63s23p63d8,铬元素在周期表中d区;
(2)聚硅氧烷中C形成4个单键,所以C的杂化方式为sp3;
(3)①根据第一电离能分析,第一电离能越小,越容易生成较稳定的单核阳离子,所以有可能生成较稳定的单核阳离子的卤素原子是I原子;
②根据VSEPR理论判断ClO3-的空间构型,价电子对数为VP=BP+LP=3+![]() =4,VSEPR模型为四面体形,由于一对孤电子对占据四面体的一个顶点,所以其空间构型为三角锥形,等电子体是指原子总数相同,价电子总数也相同的微粒,则与ClO3-互为等电子体的是SO32-;
=4,VSEPR模型为四面体形,由于一对孤电子对占据四面体的一个顶点,所以其空间构型为三角锥形,等电子体是指原子总数相同,价电子总数也相同的微粒,则与ClO3-互为等电子体的是SO32-;
(4)晶胞中,O2-的坐标为(![]() ,0,0),(0,
,0,0),(0,![]() ,0),(0,0,
,0),(0,0,![]() ),(
),(![]() ,
,![]() ,
,![]() ),将(
),将(![]() ,
,![]() ,
,![]() )+(
)+(![]() ,
,![]() ,0)=(0,0,
,0)=(0,0,![]() ),将(
),将(![]() ,
,![]() ,
,![]() )+(0,
)+(0,![]() ,
,![]() )=(
)=(![]() ,0,0),将(
,0,0),将(![]() ,
,![]() ,
,![]() )+(
)+(![]() ,0,
,0,![]() )=(0,
)=(0,![]() ,0),刚好与前三个坐标相同,所以O2-作面心立方最密堆积,根据晶胞粒子的排布,该立方体是Fe3O4的晶胞,立方体中Fe3+处于O2-围成的正八面体空隙,以立方体计算,1个立方体中含有Fe3+的个数为4×
,0),刚好与前三个坐标相同,所以O2-作面心立方最密堆积,根据晶胞粒子的排布,该立方体是Fe3O4的晶胞,立方体中Fe3+处于O2-围成的正八面体空隙,以立方体计算,1个立方体中含有Fe3+的个数为4×![]() +
+![]() ×3=2个,含有Fe2+的个数为1个,含有O2-的个数为12×
×3=2个,含有Fe2+的个数为1个,含有O2-的个数为12×![]() +1=4个,假设取1mol这样的立方体,即有NA个这样的立方体,1mol立方体的质量为m=(56×3+16×4)g,1个立方体体积为V=a3nm3=a3(a×10-7)3cm3,则晶体密度为ρ=
+1=4个,假设取1mol这样的立方体,即有NA个这样的立方体,1mol立方体的质量为m=(56×3+16×4)g,1个立方体体积为V=a3nm3=a3(a×10-7)3cm3,则晶体密度为ρ=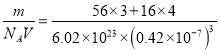 g/cm3=5.2 g/cm3。
g/cm3=5.2 g/cm3。


科目:高中化学 来源: 题型:
【题目】将30g MnO2的质量分数为76.6%的软锰矿石与足量的浓度为12 molL-1的浓盐酸完全反应(杂质不参加反应),试计算:
(1)参加反应的浓盐酸的体积的大小(结果保留3位小数)。____________
(2)在标准状况下,生成Cl2的体积的大小________ (结果保留1位小数,已知软锰矿石与浓盐酸反应的化学方程式为MnO2+4HCl(浓) =MnCl2+Cl2↑+2H2O)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 NA是阿伏加德罗常数的值。下列说法正确的是
A.1L1mol/L葡萄糖水溶液中含H-O键的数目为5 NA
B.标准状况下,2.24LCO2和N2O的混合气体所含质子数为2.2 NA
C.1molCH3COOH和3molCH3CH2OH在浓硫酸催化下反应生成酯基的数目为NA
D.常温下,28g铁片投入足量浓硝酸中,转移电子数为1.5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2一氨-3—氯苯甲酸是白色晶体,其制备流程如下:
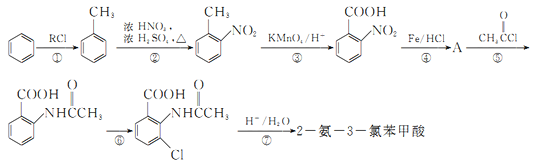
已知: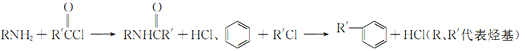
回答下列相关问题
(1)![]() 的名称是__________,2-氨-3-氯苯甲酸中含N官能团的电子式为__________。
的名称是__________,2-氨-3-氯苯甲酸中含N官能团的电子式为__________。
(2)反应①中R代表的是_____________,反应②的反应类型为_____________。
(3)如果反应③中KMnO4的还原产物为MnSO4,请写出该反应的化学方程式_____________。
(4)A的结构简式为_____________,⑥的反应条件为_____________。
(5)符合下列条件的同分异构体的结构简式为_____________。
a.式量比![]() 大42的苯的同系物;
大42的苯的同系物;
b.与酸性KMnO4反应能生成二元羧酸
c.仅有3种等效氢
(6)事实证明上述流程的目标产物的产率很低;据此,研究人员提出将步骤⑥设计为以下三步,产率有了一定提高。
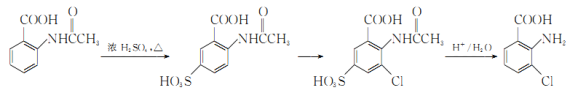
分析产率提高的原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量是高中化学常用的物理量,请完成以下有关计算:
(1)相同质量的CO和CO2,它们所含的原子数之比为___________,标准状况下,含有相同氧原子数的CO和CO2的体积之比为_____________。
(2)若a g某气体中含有的分子数为b,则c g该气体在标准状况下的体积是___________(设NA为阿伏加德罗常数的值)。
(3)标准状况下有①0.112 L水 ②0.5NA个HCl分子 ③25.6 g SO2气体 ④0.2 mol氨气(NH3) ⑤2 mol Ne 所含原子个数从大到小的顺序为___________。
(4)V mL Fe2(SO4)3溶液中,含有Fe 3+ m g,取出![]() mL该溶液稀释至4V mL,则溶液中SO42-的物质的量浓度为___________________。(用含有m、V的式子表示)
mL该溶液稀释至4V mL,则溶液中SO42-的物质的量浓度为___________________。(用含有m、V的式子表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值。下列判断正确的是( )
A.46g的NO2和N2O4的混合物所含原子总数为3NA
B.24g Mg变为Mg2+时失去的电子数目为NA
C.1mol/L CaCl2溶液中含有的Cl-离子数目为2NA
D.含有lmol FeCl3的溶液加热中完全转化为氢氧化铁胶体,其中胶粒的数目为NA个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有NaCl、Na2SO4.和NaNO3的混合物,选择适当的试剂除去杂质,从而得到纯净的NaNO3晶体,相应的实验流程如图所示。
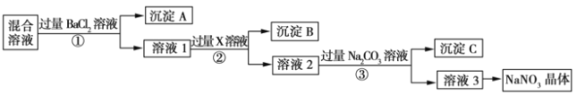
请回答下列问题:
(1)产生沉淀A的离子反应方程式是:________________________;
(2)试剂X是:____________________________________;
(3)上述实验流程中①②③步骤中均要用到的主要玻璃仪器有____________;
(4)上述实验流程中加入过量Na2CO3溶液产生的沉淀C是:________________________。
(5)按此实验方案得到的溶液3中肯定含有杂质,为了解决这个问题,可以向溶液3中加入适量的____________ (填化学式),并写出离子反应方程式:_______________________________________________。
(6)溶液3到硝酸钠晶体需要的操作步骤是:________________________洗涤,干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国最近在太阳能光电催化一化学耦合分解硫化氢研究中获得新进展,相关装置如图所示。下列说法正确的是( )

A.该工艺中光能最终转化为化学能
B.该装置工作时,H+由b极区流向a极区
C.a极上发生的电极反应为Fe3++e-=Fe2+
D.a极区需不断补充含Fe3+和Fe2+的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CoS2催化CO烟气脱硫具有广阔的工业化前景。回答下列问题:
(1)已知:
CoS2(s) +CO(g) ![]() CoS(s) +COS(g) H1
CoS(s) +COS(g) H1
2COS(g) +SO2(g) ![]() 3S(s) +2CO2(g) H2
3S(s) +2CO2(g) H2
S(s) +CoS(S) ![]() CoS2 (s) △H3
CoS2 (s) △H3
则2CO(g)+ SO2(g)![]() 2CO2(g)+S(s) H4=____。 (用H1、 H2、H3表示)
2CO2(g)+S(s) H4=____。 (用H1、 H2、H3表示)
(2)在恒温、恒压的容器中模拟回收硫,加入SO2起始量均为1mol,测得CO2的平衡体积分数随CO和SO2的投料比变化如图:

①当投料比为2时,t min 时测得SO2转化率为50%,则用S的生成速率表示的反应速率v=______g·min-1。
②当投料比为3时,CO2 的平衡体积分数对应的点是______________。
(3)向体积均为1L的恒温、恒客密团容器通入2 mol CO和| mol SO2。反应体系总压强随时间的变化如图:
①相对于I,II改变的外界条件是____________________。
②SO2的平衡转化率为______,平衡常数Kp =________(用平衡分压代替平衡浓度计算)。
(4)利用电解法处理SO2尾气可制备保险粉 (Na2S2O4).电解装置如图,则a____ b (填“>” “=”或“<”),生成S2O42-的电极反应式为____________________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com