
����Ŀ����ͼ��ʾ��װ���У���ͨ��ֱ����5 minʱ��ͭ�缫��������2.16 g��
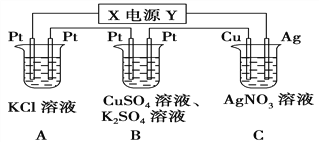
��1����Դ�缫X������Ϊ________��
��2��A�з��������ӷ���ʽΪ_______________________
��3��B�������ĵ缫��ӦʽΪ___________________________
��4��pH�仯��A_______��B_______��C_______��(��������������С������������)
��5��ͨ��5 min��B�й��ռ�224 mL����(��״��)����Һ���Ϊ200 mL����ͨ��ǰCuSO4��Һ�����ʵ���Ũ��Ϊ______________(����ǰ����Һ����ޱ仯)��
��6����A��KCl��Һ�����Ҳ��200 mL��������Һ��pHΪ_______(����ǰ����Һ����ޱ仯)
���𰸡� ���� 2Cl-+2H2O![]() 2OH-+H2��+Cl2�� 4OH--4e-=O2��+2H2O ���� ��С ���� 0.025 mol��L��1 13
2OH-+H2��+Cl2�� 4OH--4e-=O2��+2H2O ���� ��С ���� 0.025 mol��L��1 13
�������������������ͼ����Ϣ��֪��A��B��C����װ�ô�����ͬһ��·�С�����ͭ�缫��������2.16 g�������ж�ͭ�缫Ϊ���������Դ��X�缫Ϊ������Y�缫Ϊ���������ԣ�A��B�ǵ�����C�ǵ��װ�á���·��ͨ���ĵ���Ϊn(e-)=n(Ag)= ![]() .
.
��1����Դ�缫X������Ϊ������
��2��A�з��������ӷ���ʽΪ2Cl-+2H2O![]() 2OH-+H2��+Cl2��.
2OH-+H2��+Cl2��.
��3��B�������ϣ���Һ��ˮ�����OH-���ӷŵ磬�缫��ӦʽΪ4OH--4e-=O2��+2H2O.
��4��A�е��������������أ���pH����B�е����������ᣬ��pH��С��C��һ�����װ�ã���pH���䡣
��5��ͨ��5 min��·��ͨ���ĵ���Ϊn(e-)=![]() ��B���������ռ���O2��n(O2)=
��B���������ռ���O2��n(O2)= ![]() ����ΪB�й��ռ�����״����224 mL���壨0.01mol��������B������һ������������0.005mol���ɴ˸��ݵ���ת���غ㣬����ȷ��B��һ������ͭ0.005mol��������Һ���Ϊ200 mL�����Լ����ͨ��ǰCuSO4��Һ�����ʵ���Ũ��Ϊ
����ΪB�й��ռ�����״����224 mL���壨0.01mol��������B������һ������������0.005mol���ɴ˸��ݵ���ת���غ㣬����ȷ��B��һ������ͭ0.005mol��������Һ���Ϊ200 mL�����Լ����ͨ��ǰCuSO4��Һ�����ʵ���Ũ��Ϊ![]() 0.025 mol��L��1��
0.025 mol��L��1��
��6����A��KCl��Һ�����Ҳ��200 mL��������Һ��n(OH-)=n(e-)=0.02mol����c(OH-)= ![]() ������pHΪ13��
������pHΪ13��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A�ķ���ʽΪC2H2,B�Ǻϳ����ϵĵ��壬C����Է�������Ϊ78,M��һ�־��й���ЧʳƷ�������õ��л���,��AΪԭ�Ϻϳ�B��M��·����ͼ��ʾ��
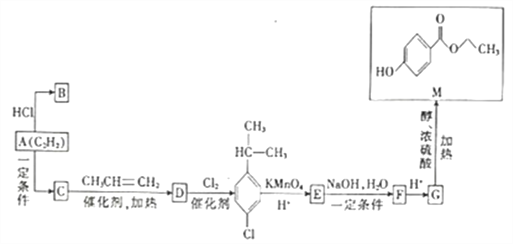
��1��C��D�ķ�Ӧ����Ϊ___________��B�Ľṹ��ʽΪ___________��
��2��д��E��F�Ļ�ѧ����ʽ��_______________________________��
��3��G�еĺ��������ŵ�������_______________,д����G��һ�������·�Ӧ���ɸ߷��ӻ�����Ļ�ѧ��Ӧ����ʽ��_______________________________________��
��4��M��ͬ���칹���ж���,д��������������������ͬ���칹��Ľṹ��ʽ��___________��___________��___________��___________��
���ܷ���������Ӧ
�������ͻ��ұ�����һ��ȡ����������
����FeCl3��Һ������ɫ
��1mol���л������������Ʒ�Ӧ����1mol����(һ��̼ԭ����ͬʱ��������-OH�Ľṹ���ȶ�)
��5���Լ�����![]() ����Ҫ���л������м��壬д������Ȳ����ȲΪԭ��(���Լ���ѡ)�Ʊ��Լ����ӵĺϳ�·�ߣ�_________________________________________________��
����Ҫ���л������м��壬д������Ȳ����ȲΪԭ��(���Լ���ѡ)�Ʊ��Լ����ӵĺϳ�·�ߣ�_________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ��������һδ֪Ũ�ȵ�ϡ���ᣬijͬѧ��ʵ�����н���ʵ��ⶨ�����Ũ�ȡ������������գ�
��1������100mL0.100molL-1 NaOH����Һ��
�� ��Ҫ�������裺������������ܽ��_______����ȴ��ϴ�ӣ�����ϴ��Һ��������ƿ�������ݡ�ҡ�ȡ������ƺõ���Һ�����Լ�ƿ�У����ϱ�ǩ��
�� ����_____g�������ƹ������������У���ƽ�������롢���ӣ���________���ձ����������
��2��ȡ20.00 mL�������������ƿ�У����μ�23�η�̪��ָʾ���������Ƶı�NaOH��Һ���еζ����ظ������ζ�����23�Σ���¼�������£�
ʵ���� | NaOH��Һ��Ũ�ȣ�molL-1�� | ����NaOH��Һ�����(mL) | ������������(mL) |
1 | 0.100 | 22.18 | 20.00 |
2 | 0.100 | 22.22 | 20.00 |
3 | 0.100 | 22.20 | 20.00 |
�ٸ�ʵ��ζ��ﵽ�յ�ı�־��_____________________________��
�ڸ����������ݣ��ɼ�����������Ũ��ԼΪ_________________��������λ��Ч���֣���
��������ʵ���У����в���������������ȷ������ɲⶨ���ƫ�ߵ���_______________��
A.�ζ��յ����ʱ���Ӷ���
B����ʽ�ζ���ʹ��ǰ��ˮϴ��δ�ô���������ϴ
C����ƿˮϴ��δ����
D����ʽ�ζ��ܼ��첿�������ݣ��ζ�����ʧ
E������NaOH����ʱ����������KOH����
����������ʵ�����Ƶ�0.10 molL-1NaOH��Һ�ⶨʳ���������Ũ�ȣ�Ӧ��ѡ�õ�ָʾ��Ϊ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����25 mL 0.1 mol/L��NaOH��Һ����μ���0.2 mol/L������Һ��������ͼ��ʾ���й����ӵ�Ũ�ȹ�ϵ��ȷ����
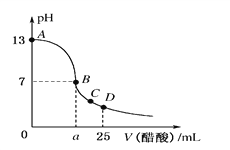
A. ��A��B����һ�㣬��Һ��һ������c(Na��)>c(CH3COO��)> c(H��) >c(OH��)
B. ��B�㣬a>12.5������c(Na��)��c(CH3COO��)��c(OH��)��c(H��)
C. ��C�㣺c(CH3COO��)>c(Na��)> c(OH��) > c(H��)
D. ��D�㣺c(CH3COO��)��c(CH3COOH)��2c(Na��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ���¶Ȳ���ʱ��ij�����ָ���A��B�����֣�A��B֮��ĵ���������������ƶ���B�п��ƶ��Ļ�������A�г���2molSO2��1molO2��ƽ��ʱA�����Ʊ�Ϊԭ�����0.7������B�г���2molSO3��1molN2������ͬ�¶Ⱥ���ǿ�����·�����Ӧ��Ҳ����ƽ�⡣����˵����ȷ����
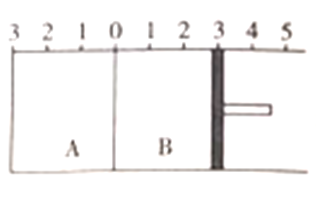
A. ƽ���A��B������������ȴ���2.1:3.1
B. ƽ���B������SO2���������С��2/21
C. ƽ���B������SO3��ת����С��10%
D. ƽ���A��B��������S02�����ʵ���ΪA>B
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ4A��g��+5B��g��![]() 4C��g��+6D��g������5 L���ܱ������н��У�����Ӻ�C�����ʵ���������0.30 mol������������ȷ���ǣ�������
4C��g��+6D��g������5 L���ܱ������н��У�����Ӻ�C�����ʵ���������0.30 mol������������ȷ���ǣ�������
A. A��ƽ����Ӧ������0.010 molL��1s��1
B. �����к�D���ʵ�������Ϊ0.45 mol
C. ������A��B��C��D�����ʵ����ı�һ����4��5��4��6
D. ������A�����ʵ���һ��������0.30 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A.ֻ����һ��Ԫ�ص�����һ���Ǵ�����
B.���й��ۼ��Ļ�����һ���ǹ��ۻ�����
C.ʯīת��Ϊ���ʯΪ��ѧ�仯
D.ˮ���ȶ�����Ϊˮ���Ӽ���ڽ�ǿ�ķ��Ӽ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������AIST������������һ�������������ͳɱ����-ͭ����ȼ�ϵ�ء��õ��ͨ��һ�ָ��ӵ�ͭ��ʴ���������������������зŵ����Ϊ2Li+Cu2O+H2O�T2Cu+2Li++2OH-������˵������ȷ����( )

A. �ŵ�ʱ��Li+������������Cu���ƶ�
B. �ŵ�ʱ�������ĵ缫��ӦʽΪCu2O+H2O+2e-=2Cu+2OH-
C. ͨ����ʱ��ͭ����ʴ���������Cu2O
D. ������Ӧ�����У�ͭ�൱�ڴ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com