
【题目】某课外研究性学习小组拟用粗盐(含有少量杂质包括:泥沙、CaCl2、MgCl2、Na2SO4)经提纯后,配制0.4mol/L 450mL NaCl溶液.他们设计并实施了如下实验,请根据已学过的知识回答下列问题:
(1)取一定量的粗盐置于烧杯中加适量的水溶解。将配制的粗盐悬浊液过滤后取滤液加入过量的除杂试剂,如果除杂试剂可从下列六种溶液中选择①Na2CO3溶液②KOH溶液③AgNO3溶液④NaOH溶液⑤NaHCO3溶液⑥BaCl2溶液,则正确的试剂和加入的顺序应为:__________(填选项)
A.①②③ B.②⑥⑤ C.④⑥① D.①④⑥ E.⑥①④ F.⑥②⑤
(2)将所得的悬浊液经过滤后取滤液加入足量的盐酸,充分反应后对混合溶液进行蒸发、过滤、洗涤、干燥操作,得到纯净的NaCl固体,请描述在蒸发操作过程中玻璃棒的作用:_______________________________________________________
(3)利用(2)中所得的NaCl固体继续配制所需溶液.在托盘天平上称量____g NaCl固体.配制过程中需要使用的玻璃仪器有:烧杯、玻璃棒、_________
和_______________
(4)配制结束后同学们对实验中出现的某些错误操作,对最终配制的溶液浓度的影响进行了分析,则下列错误操作会导致最终配制溶液中NaCl的浓度相比0.4mol/L是偏小的是__________
A.在上述(2)步中没有使用盐酸处理滤液;
B.在上述(3)步中没有对烧杯和玻璃棒进行洗涤;
C.定容时俯视凹液面;
D.上下颠倒摇匀后液面低于刻度线,未及时加水至刻度线。
【答案】CE 搅拌,使溶液受热均匀 11.7g 胶头滴管 500mL容量瓶 AB
【解析】
(1)、根据含有的杂质是CaCl2、MgCl2、Na2SO4,根据既能除去杂质还不能引入新杂质的原则,选择出合适的除杂试剂是:①Na2CO3溶液④NaOH溶液⑥BaCl2溶液,然后根据①Na2CO3溶液的作用是不但要除去CaCl2,还要除去过量的BaCl2,故①Na2CO3溶液的加入一定要在⑥BaCl2溶液之后,得出所加试剂的顺序;
(2)、蒸发操作过程中为防止溶液因局部过热造成飞溅,需要用玻璃棒搅拌,使溶液受热均匀;
(3)、依据配制溶液体积选择合适容量瓶,依据m=cV M计算需要溶质的质量;根据配制步骤选择需要的仪器;
(4)、分析操作对溶质的物质的量和溶液体积的影响,依据![]() 进行误差分析。
进行误差分析。
(1)、除去食盐中的CaCl2用①Na2CO3溶液,除去MgCl2用④NaOH溶液,除去Na2SO4用⑥BaCl2溶液,而①Na2CO3溶液的作用是不但要除去CaCl2,还要除去过量的BaCl2,故①Na2CO3溶液的加入一定要在⑥BaCl2溶液之后,故正确的试剂和加入的顺序应为:⑥①④或⑥④①或④⑥①;
故选CE;
(2)、蒸发操作过程中为防止溶液因局部过热造成飞溅,需要用玻璃棒搅拌,使溶液受热均匀;
故答案为:搅拌,使溶液受热均匀;
(3)、配制0.4mol/ L 450mL NaCl溶液,应择500mL容量瓶,实际配制500mL溶液,需要溶质氯化钠的质量m = 0.4mol/L×58.5g/mol×0.5L= 11.7g ;配制一定物质的量浓度溶液的一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶,用到的仪器为:天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管;所以还需要的仪器为:胶头滴管; 500mL容量瓶;
故答案为:11.7;胶头滴管; 500mL 容量瓶;
(4)A、在上述(2)步中没有使用盐酸处理滤液,则得到的氯化钠中含有杂质,导致称取的氯化钠质量偏小,溶质的物质的量偏小,溶液浓度偏小;
B、在上述(3)步中没有对烧杯和玻璃棒进行洗涤,导致部分溶质未转移到容量瓶,导致浓度偏小;
C、定容时俯视凹液面,导致溶液体积偏小,溶液浓度偏大;
D、上下颠倒摇匀后液面低于刻度线,未及时加水至刻度线,操作正确,溶液浓度准确无影响;
故选AB。


科目:高中化学 来源: 题型:
【题目】如表为某有机物与各种试剂的反应现象,则这种有机物可能是
试剂 | 钠 | 溴水 | NaHCO3溶液 |
现象 | 放出气体 | 褪色 | 放出气体 |
A. CH2═CH﹣CH2﹣OHB. ![]()
C. CH2═CH﹣COOHD. CH3COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钠常作漂白剂、杀菌剂、消毒剂。过氧化钠保存不当容易吸收空气中CO2而变质。
(1)某课外活动小组欲探究某过氧化钠样品是否已经变质,取少量样品,溶解,加入__________溶液,充分振荡后有白色沉淀,证明Na2O2已经变质。
(2)该课外活动小组为了粗略测定过氧化钠的纯度,他们称取a g样品,并设计用下图装置来测定过氧化钠的质量分数。

①A中发生反应离子方程式为_____________________。
②将仪器连接好以后,必须进行的第一步操作是_____________________。
③B装置出来的气体是否需要干燥_________________。(填“是”或“否”)
④写出装置C中发生的所有反应的化学方程式_____________,______________。
⑤D中NaOH溶液的作用_______________________。
⑥实验结束时,读取实验中生成气体的体积时,不合理的是_______________。
a.直接读取气体体积,不需冷却到室温
b.上下移动量筒,使得E、F中液面高度相同
c.视线与凹液面的最低点相平读取量筒中水的体积
⑦读出量筒内水的体积后,折算成标准状况下氧气的体积为V mL,则样品中过氧化钠的质量分数为__________________。
⑧实验完成后E到F之间导管内残留水的体积会使测量结果__________。(填“偏大”、“偏小”或“不影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设阿伏加德罗常数的数值为NA,则下列说法正确的是( )
A. 常温常压下,11.2 L甲烷中含有的氢原子数为2NA
B. 标准状况下,0.3 mol二氧化硫中含有的氧原子数为0.3×6.02×1023
C. 标准状况下,2.7 g Al与足量的盐酸反应,生成H2的体积是22.4L
D. 常温下,1 L 0.1 mol·L-1MgCl2溶液中含Cl-数为0.2moL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示物质相互转换关系:

试回答:
(1)写出B的化学式____________、C溶液是______________。
(2)写出由E转变成F发生反应的化学方程式_______________。
(3)鉴别G溶液中阳离子的操作方法及实验现象:__________________。
(4)向G溶液中加入A的离子方程式____________________。
(5)写出D溶液中加入AgNO3得到白色沉淀的离子方程式__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,从A处通入新制备的Cl2,关闭B阀时,C处的红色布条看不到明显现象;当打开B阀后,C处红色布条逐渐褪色。D瓶中装的是( )

①浓硫酸 ②NaOH溶液 ③H2O ④饱和NaCl溶液
A. ①③ B. ②④ C. ①② D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ca(ClO)2与浓盐酸反应会生成Cl2,该反应的化学方程式为Ca(ClO)2+4HCl(浓)===CaCl2+2Cl2↑+2H2O
(1)浓盐酸在反应中显示出来的性质是_____(填写字母)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)产生0.3 mol Cl2,则转移的电子的物质的量为______mol。
(3)用双线桥法表示该氧化还原反应中电子转移的方向和数目_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组的同学在网上查询资料时得知,干燥的CO2与Na2O2不能反应,只有在水蒸气存在下二者才能发生反应。他们设计了如图所示实验装置,用于验证上述结论。
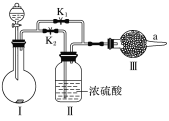
(1)装置Ⅰ中的试剂的最佳组合是________(填字母)。
a.稀盐酸 b.稀硫酸
c.小苏打 d.石灰石
(2)实验时,甲同学认为关闭K1、打开K2,通过观察________判断此时Ⅲ中是否发生了化学反应。
(3)乙同学认为可以分别按“先关闭K1、打开K2,再关闭K2、打开K1”的方式进行操作,并在a处收集所得气体,然后用带火星的木条检验收集到的气体,但他发现两种情况下木条均没有复燃。
①丙同学经过观察分析,建议在Ⅲ后安装一个盛有碱石灰的干燥管,目的是________________
②丁同学认为即使采纳丙同学的建议且最终观察到木条复燃,也不能证明CO2参与了反应,原因是________________________
(4)为进一步达到实验目的,应补充的实验操作是:取最终反应后Ⅲ中所得固体,____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数,下列叙述中正确的是
①106 g Na2CO3晶体中的离子总数大于3NA
②25 ℃、1.01×105 Pa下,14 g氮气所含的氮原子数为NA
③标准状况下,22.4LCCl4中所含的分子数约为6.02×1023
④标准状况下,aL的氧气和氮气的混合物含有的分子数约为![]() ×6.02×1023
×6.02×1023
⑤常温常压下,92 g的NO2和N2O4混合气体含有的原子数为6NA
A.①②④B.②④⑤C.③④⑤D.④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com