
����Ŀ��ʵ��С��ģ�ҵ�Ϻ�ˮ���壬�������ʵ�顣 �ش��������⣺
�� ������ͼ��ʾװ�ø����壺
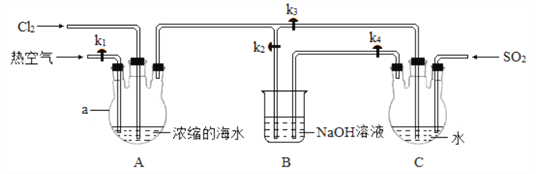
ʵ�鲽�裺
�ٹر� k1��k3����k2����װ��A ��ͨ������Cl2����ַ�Ӧ��
��ֹͣͨCl2���ر�k2���� k1��k3 ��k4�� ��װ��A ��ͨ�������ȿ�����ͬʱ��װ��C��ͨ������SO2����ַ�Ӧ��
��ֹͣͨ���壬�ر�k1��k4��
��1��a ������Ϊ___________��
��2�� ���������Ҫ��Ӧ�����ӷ���ʽΪ_____________��
��3�� �������ͨ���ȿ���������Ϊ_______�� װ�� C ����������ķ�Ӧ�У��������뻹ԭ�������ʵ���֮��Ϊ____________��ʵ�ʲμӷ�Ӧ��SO2 �����ʵ�����������ֵ����Ҫԭ��Ϊ_____________���û�ѧ����ʽ��ʾ����
���Ʊ��壺
������Ĺ��̽���������װ�� C ��ͨ�� Cl2����ַ�Ӧ������
��4����������װ����ȷ����_____����ѡ����ĸ����

��5�� װ�� A �м���V mL �� Br����Ũ��Ϊ c mol��L��1��Ũ����ˮ�����������嵥�ʵ�����Ϊ m g�� ���ʵ�����嵥�ʵIJ���Ϊ__________��
���𰸡� ������ƿ 2Br����Cl2��Br2��2Cl�� �����ɵ� Br2����װ�� C �� 1:1 2SO2��O2��2H2O��2H2SO4 d ![]()
����������1��a������Ϊ������ƿ����2�����������Ҫ��Ӧ���������������ӣ���Ӧ�����ӷ���ʽΪ2Br����Cl2��Br2��2Cl������3�����ӷ�����˲������ͨ���ȿ���������Ϊ�����ɵ� Br2����װ��C�С�װ��C ����������ķ�Ӧ��SO2+Br2+2H2O��H2SO4+2HBr������SO2�ǻ�ԭ���������������������������뻹ԭ�������ʵ���֮��Ϊ1:1������SO2����Һ���ױ���������������ʵ�ʲμӷ�Ӧ��SO2�����ʵ�����������ֵ����Ӧ�Ļ�ѧ����ʽΪ2SO2��O2��2H2O��2H2SO4����4���������¶ȼ�ˮ���������ƿ֧�ܳ��ڴ���Ϊ��ֹҺ��������������У�Ӧ����ֱ�������ܣ���ѡd����5��װ�� A �м���V mL�� Br����Ũ��Ϊ c mol��L��1��Ũ����ˮ�����������嵥�ʵ�����Ϊm g����˸�ʵ�����嵥�ʵIJ���Ϊ![]() ��
��


 ����ʦ���һ��һ��ϵ�д�
����ʦ���һ��һ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��2SO3(g)![]() 2SO2(g)+O2(g)�������仯ͼ����ͼ�ó������������ȷ����( )
2SO2(g)+O2(g)�������仯ͼ����ͼ�ó������������ȷ����( )
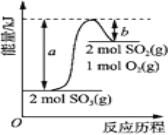
A. �û�ѧ��Ӧ�����м������������������������ͷ�
B. 2SO3(g)![]() 2SO2(g)+O2(g) ��H����(a��b) kJ��mol
2SO2(g)+O2(g) ��H����(a��b) kJ��mol
C. 1 mol SO2��������1 mol SO3��������
D. ��ij��������2 mol SO3��ַ�Ӧ������(a��b) kJ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. 3.0L0.1mol��L-1NaOH��Һ�л���ͨ��CO2����Һ����8.8gʱ����Һ�У�c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
B. �����£���CH3COONa��Һ������������ҺpH=7��c(Na+)>c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)=c(OH-)
C. �����£�pH=6��NaHSO3��Һ�У�c(SO32-)- c(H2SO3)=9.9��10-7mol��L-1
D. Ksp (Fe(OH)3)=1.0��10-38��Ksp (Mg(OH)2)=1.0��10-11����Ũ�Ⱦ�Ϊ0.1 mol��L-1�Ȼ������Ȼ�þ�����Һ������ȥ��Һ�е�Fe3+��Ӧ��pH����3��11��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Һ���ܴ����������ɫ���������ǣ� ��
A.K+��Na+��NO3����MnO4��
B.K+��Na+��Cl����SO42��
C.K+��Na+��Br����Cu2+
D.Na+��Ba2+��OH����SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ҵ������и��ֻ�ѧ����ͼ��ʾ,�����Ҵ��ڸ��ַ�Ӧ�ж��Ѽ���˵������ȷ���� (����)
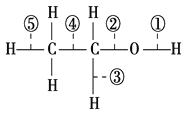
A. �ͽ����Ʒ�Ӧʱ���ٶ���
B. ��ŨH2SO4���ȵ�170 ��ʱ���ں͢ݶ��ѣ���ŨH2SO4���ȵ�140 ��ʱ���٢ڶ���
C. �Ҵ�����������ȫȼ�գ����٢ڶ���
D. ��Ag������O2��Ӧʱ���ٺ͢۶���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ճ�����л��ϳ�����;�㷺��ij�о�С���о������ڸ����������ѽⷴӦ��ԭ������Ӧ�á�
(1)��֪CH4(g)+2O2(g)=CO2(g)+2H2O ��H=- Q1kJ��mol-1
C2H2(g)+O2(g)=2CO2(g)+H2O(l) ��H=- Q2kJ��mol-1
H2(g)+ ![]() O2=(g)=H2O(l) ��H=- Q3kJ��mol-1
O2=(g)=H2O(l) ��H=- Q3kJ��mol-1
����������ѽⷴӦ��2CH4(g)=C2H2(g)+3H2(g)�ġ�H=____________kJ��mol-1
(2)���о�С�����о������еó�������ֽ�ʱ����������ƽ��ʱ��ѹ(Pa)���¶�(��)�Ĺ�ϵ��ͼ��ʾ��
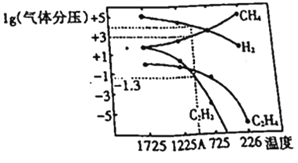
��T1��ʱ����2L�����ܱ������г���0.3molCH4��������Ӧ2CH4(g) ![]() C2H6(g)+2H2 (g)���ﵽƽ��ʱ�����c(C2H4)=c(CH4)���÷�Ӧ�ﵽƽ��ʱ��CH4��ת����Ϊ_________________��
C2H6(g)+2H2 (g)���ﵽƽ��ʱ�����c(C2H4)=c(CH4)���÷�Ӧ�ﵽƽ��ʱ��CH4��ת����Ϊ_________________��
�ڶ�����ƽ��״̬�����ı��¶���T2�棬��10s���ٴδﵽƽ�⣬c(CH4)=2c(C2H4)����10s��C2H4ƽ����Ӧ����r(C2H4) =__________�������仯������T1______T2(�>����<��)���ж�������_________________��
�۶��������з�����2CH4(g)![]() C2H2(g)+3H2(g)����ʽ����÷�Ӧ��ͼ��A���¶�ʱ��ƽ�ⳣ��K_____(��ƽ���ѹ����ƽ��Ũ��)��(��֪1g0.05=-1.3)����ֻ�ı�һ����Ӧ����ʹ�÷�Ӧ��ƽ�ⳣ����Kֵ�����������ǣ�_________(�����)
C2H2(g)+3H2(g)����ʽ����÷�Ӧ��ͼ��A���¶�ʱ��ƽ�ⳣ��K_____(��ƽ���ѹ����ƽ��Ũ��)��(��֪1g0.05=-1.3)����ֻ�ı�һ����Ӧ����ʹ�÷�Ӧ��ƽ�ⳣ����Kֵ�����������ǣ�_________(�����)
A.���ܼ�С��C2H2��Ũ�� B.һ�����������¶�
C.���������˷�Ӧ��ϵ��ѹǿ D.����ʹ���˴���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼװ�ã�ͨ�����Cu��������Һ��ɫ�������˵����ȷ����(����)
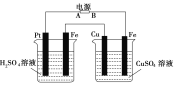
A. A��������Cu����
B. ���ձ���Һ�����ձ���Һ��pH����С
C. ���ձ���ҺŨ�ȱ�����ձ���ҺŨ�Ȳ���
D. ���ձ�Pt�������ձ�Fe���ĵ��������ʵ���֮��Ϊ1:1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Է�Ӧ��aA(g)+bB(g)![]() cC(g)+dD(g) ��H����Ӧ�ص����Ӧ��ͼ���˵���в���ȷ����
cC(g)+dD(g) ��H����Ӧ�ص����Ӧ��ͼ���˵���в���ȷ����
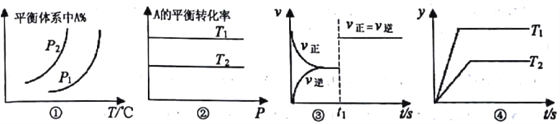
A. ͼ���У���P1>P2����÷�Ӧ�ڽϵ��¶����������Է�����
B. ͼ���У���T2>T1�����H<0 ��a+b=c+d
C. ͼ����t1ʱ�̸ı������һ����ʹ���˴���
D. ͼ���У�����H<0���������겻���ܱ�ʾ���Ƿ�Ӧ���ת����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������6������������������ص��л��
�� ![]() ���ջ���Ʒ���ϣ� ��
���ջ���Ʒ���ϣ� �� ![]() ����������ԭ�ϣ�
����������ԭ�ϣ�
�� ![]() ����������ԭ�ϣ� ��
����������ԭ�ϣ� �� 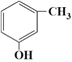 ������ũҩ��ԭ�ϣ�
������ũҩ��ԭ�ϣ�
�� ![]() ��ʳ�����ϣ� ��
��ʳ�����ϣ� �� ![]() ��ʳƷ��������
��ʳƷ��������
��ش�
��1�������������______������ţ���
��2��������Ϊͬϵ�����______������ţ���
��3��������Ϊͬ���칹�����______������ţ���
��4����ϵͳ����������������������Ϊ______��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com