
【题目】甲烷在日常生活及有机合成中用途广泛。某研究小组研究甲烷在高温下气相裂解反应的原理及其应用。
(1)已知CH4(g)+2O2(g)=CO2(g)+2H2O △H=- Q1kJ·mol-1
C2H2(g)+O2(g)=2CO2(g)+H2O(l) △H=- Q2kJ·mol-1
H2(g)+ ![]() O2=(g)=H2O(l) △H=- Q3kJ·mol-1
O2=(g)=H2O(l) △H=- Q3kJ·mol-1
则甲烷气相裂解反应:2CH4(g)=C2H2(g)+3H2(g)的△H=____________kJ·mol-1
(2)该研究小组在研究过程中得出当甲烷分解时,几种气体平衡时分压(Pa)与温度(℃)的关系如图所示。
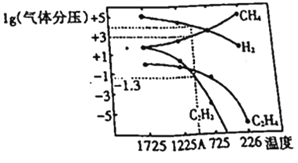
①T1℃时,向2L恒容密闭容器中充入0.3molCH4,发生反应2CH4(g) ![]() C2H6(g)+2H2 (g),达到平衡时,测得c(C2H4)=c(CH4)。该反应达到平衡时,CH4的转化率为_________________。
C2H6(g)+2H2 (g),达到平衡时,测得c(C2H4)=c(CH4)。该反应达到平衡时,CH4的转化率为_________________。
②对上述平衡状态,若改变温度至T2℃,经10s后再次达到平衡,c(CH4)=2c(C2H4),则10s内C2H4平均反应速率r(C2H4) =__________,上述变化过程中T1______T2(填“>”或“<”),判断理由是_________________。
③对于容器中发生的2CH4(g)![]() C2H2(g)+3H2(g),列式计算该反应在图中A点温度时的平衡常数K_____(用平衡分压代替平衡浓度);(已知1g0.05=-1.3)。若只改变一个反应条件使该反应的平衡常数的K值变大。则该条件是:_________(填序号)
C2H2(g)+3H2(g),列式计算该反应在图中A点温度时的平衡常数K_____(用平衡分压代替平衡浓度);(已知1g0.05=-1.3)。若只改变一个反应条件使该反应的平衡常数的K值变大。则该条件是:_________(填序号)
A.可能减小了C2H2的浓度 B.一定是升高了温度
C.可能增大了反应体系的压强 D.可能使用了催化剂
【答案】 (3Q3+Q2-2Q1) 66.7% 0.00125mol·L-1·S-1 > 从图象判断出该反应为吸热反应,对比T1℃到T2℃,CH4浓度增大,说明平衡逆向移动,则T1>T2 5×104 B
【解析】本题主要考查影响化学平衡的外界因素及有关化学平衡的计算。
(1)将已知热化学方程式分别表示为①、②、③,3③+②-2①得甲烷气相裂解反应:2CH4(g)=C2H2(g)+3H2(g)的△H=(3Q3+Q2-2Q1)kJ·mol-1。
(2) ①达到平衡时,由碳元素守恒可得c(C2H4)=c(CH4)=0.1mol,CH4的转化率为0.2mol/0.3mol=66.7%。
②由碳元素守恒可得c(CH4)=2c(C2H4)=0.15mol, r(C2H4)=r(CH4)/2=0.05/2/2/10mol·L-1·S-1=0.00125mol·L-1·S-1,上述变化过程中T1>T2,判断理由是从图象判断出该反应为吸热反应,对比T1℃到T2℃,CH4浓度增大,说明平衡逆向移动,则T1>T2。
③该反应在图中A点温度时CH4(g)、C2H2(g)、H2(g)的平衡分压分别为103、0.05、104,2CH4(g)![]() C2H2(g)+3H2(g),对应的平衡常数K=1012×0.05/106= 5×104。
C2H2(g)+3H2(g),对应的平衡常数K=1012×0.05/106= 5×104。
若只改变一个反应条件使该反应的平衡常数的K值变大。则该条件是:B。理由:A.温度不变,K不变;B. 从图象判断出该反应为吸热反应,升温平衡右移,K增大;C. 温度不变,K不变;D. 温度不变,K不变。故选B。


科目:高中化学 来源: 题型:
【题目】苯甲酸是常用的防腐剂和重要的医药原料。一种药用苯甲酸的制备方法如下:
Ⅰ.在反应罐中加入甲苯、饱和KMnO4溶液、Fe2O3(催化剂),加热、回流数小时,充分反应。
Ⅱ.反应结束后,改为蒸馏装置。加热蒸馏,直至冷凝管壁不再出现油珠。
Ⅲ.将反应罐中的混合物趁热过滤,滤渣用少量热水洗涤。
Ⅳ.向滤液中滴加浓盐酸酸化至pH=2,抽滤,用少量水洗涤,干燥得苯甲酸粗品。
Ⅴ.将粗苯甲酸加入……,结晶、洗涤、过滤,得到药用纯苯甲酸。
已知:相关物质的溶解度(g/mL)
温度(℃) | 25 | 50 | 60 | |
苯甲酸 | 在水中 | 0.0034 | 0.0085 | 0.0095 |
在乙醇中 | 0.4 | 0.7 | 1 | |
氯化钾 | 在乙醇中 | 难溶 | ||
(1)Ⅰ中发生的主要反应为:![]() (未配平),则Ⅳ中发生反应的离子方程式为______。
(未配平),则Ⅳ中发生反应的离子方程式为______。
(2)Ⅱ中蒸馏的目的是______。
(3)Ⅲ中趁热过滤的目的是______。
(4)将Ⅴ中操作补充完整:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于容量瓶的使用,下列操作不正确的是( )
A.容量瓶是不能作为反应容器或长期贮存溶液的容器
B.用蒸馏水洗涤后不需要将容量瓶烘干
C.为了便于操作,浓溶液稀释或固体溶解可直接在容量瓶中进行
D.为了使所配溶液浓度均匀,定容结束后,要摇匀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以铬铁矿(主要成分为FeOCr2O3)、碳酸钠、氧气、和硫酸为原料生产重铬酸钠(Na2Cr2O72H2O),其主要反应为:
(1)4FeOCr2O3+8Na2CO3+7O2![]() 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2
(2)2Na2CrO4+H2SO4![]() Na2SO4+Na2Cr2O7+H2O
Na2SO4+Na2Cr2O7+H2O
下列说法正确的是( )
A. 反应(1)和(2)均为氧化还原反应
B. 反应(1)的氧化剂是O2,还原剂是FeOCr2O3
C. 高温下,O2的氧化性强于Fe2O3,弱于Na2CrO4
D. 反应(1)中每生成1molNa2CrO4时电子转移3mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验小组模拟工业上海水提溴,设计如下实验。 回答下列问题:
Ⅰ. 利用如图所示装置富集溴:
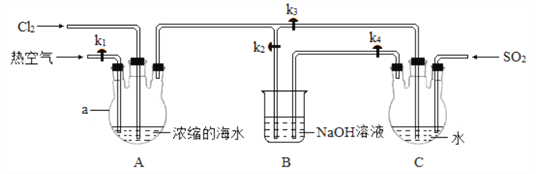
实验步骤:
①关闭 k1、k3,打开k2,向装置A 中通入足量Cl2,充分反应;
②停止通Cl2,关闭k2,打开 k1、k3 和k4, 向装置A 中通入足量热空气,同时向装置C中通入足量SO2,充分反应;
③停止通气体,关闭k1、k4。
(1)a 的名称为___________。
(2) 步骤①中主要反应的离子方程式为_____________。
(3) 步骤②中通入热空气的作用为_______。 装置 C 发生富集溴的反应中,氧化剂与还原剂的物质的量之比为____________;实际参加反应的SO2 的物质的量大于理论值,主要原因为_____________(用化学方程式表示)。
Ⅱ.制备溴:
富集溴的过程结束后,继续向装置 C 中通入 Cl2,充分反应后蒸馏。
(4)下列蒸馏装置正确的是_____(填选项字母)。

(5) 装置 A 中加入V mL 含 Br-的浓度为 c mol·L-1的浓缩海水,蒸馏所得溴单质的质量为 m g, 则该实验中溴单质的产率为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆周中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示。导致该现象的主要原因是液滴之下氧气含量比边缘少。下列说法正确的是( )

A. 液滴中的Cl―由a区向b区迁移
B. 液滴边缘是正极区,发生的电极反应为:O2+2H2O+4e-=4OH-
C. 液滴下的Fe因发生还原反应而被腐蚀,生成的Fe2+由a区向b区迁移,与b区的OH―形成Fe(OH)2,进一步氧化、脱水形成铁锈
D. 若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,则负极发生的电极反应为:Cu-2e-=Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是碳酸钙(CaCO3)在25 ℃和100 ℃两种情况下,在水中的溶解平衡曲线。下列有关说法正确的是
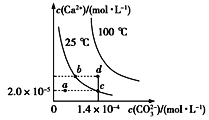
A. CaCO3(s)![]() Ca2+(aq)+ CO32-(aq) ΔH<0
Ca2+(aq)+ CO32-(aq) ΔH<0
B. a、b、c、d四点对应的溶度积Ksp相等
C. 温度不变,蒸发水,可使溶液由a点变到c点
D. 25 ℃时,CaCO3的Ksp=2.8×10-9
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com