
【题目】化学与社会、生产、生活密切相关。下列说法正确的是( )
A. 明矾、漂白粉、臭氧的净水原理相同
B. 硅胶可用作干燥剂
C. 煤的干馏和石油的分馏都属于物理变化
D. 亚硝酸钠是一种食品防腐剂,使用时其用量可以不加限制
科目:高中化学 来源: 题型:
【题目】已知:25℃,H2A的电离常数Kl=6.0×10-2,K2=6.0×10-5。此温度下,将1 mL浓度为0.1mol/L, 的H2A溶液加水稀释到1000mL。下列说法正确的是
A. 上述稀释过程中,H2A分子及所有离子浓度均减小
B. 上稀释过程中,![]() 的变化趋势保持增大
的变化趋势保持增大
C. 上述溶液稀释前后均存在:c(H+)=c(OH-)+2c(A2-)
D. 根据H2A的电离常数,可推知0.1mol/L NaHA溶液的pH值大于7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把0.1molNaCl固体溶于水,配成1L 溶液,溶液中NaCl的物质的量浓度是
A. 2 mol/L B. 0.2 mol/L C. 1 mol/L D. 0.1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁、铝合金粉末10.2g溶于500mL 4mol·L-1盐酸中恰好完全反应。若加入2mol·L-1的氢氧化钠溶液,使得沉淀达到最大量,则需加入氢氧化钠溶液的体积为
A. 100mL B. 500mL C. 1000mL D. 1500mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元
素的含量。实验步骤如下:
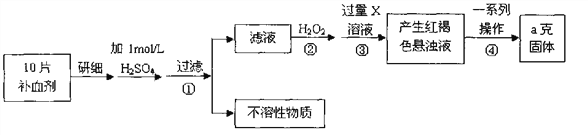
请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法________________________________,该
过程的现象为:______________________________
(2)步骤②加入过量H2O2的目的(用离子方程式表示):_______________。
(3)步骤③中反应的离子方程式:_______________________________________。
(4)实际上向滤液中直接滴加X溶液最终也会生成红褐色浊液,此过程中发生的
氧化还原反应为(用化学方程式表达)_________________________。
(5)步骤④中最终得到a克红棕色粉末,则一系列处理的操作步骤:_________、
洗涤、_________、冷却、称量。
(6)若实验无损耗,则每片补血剂含铁元素的质量__________g。
(7)正常人每天应补充14mg左右的铁,如果全部通过服用含FeSO4·7H2O的片剂
来补充铁,则正常人每天服需用含______________mgFeSO4·7H2O的片剂。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在FeCl3、CuCl2和HCl的混合溶液中加入铁粉,待反应结束后,将剩余的固体滤出,发现固体能被磁铁吸引,则反应后溶液中大量存在的阳离子是
A.Fe2+ B.H+ C.Cu2+和Fe2+ D.Fe3+和Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 可将气态废弃物中的硫化氢转化为可利用的硫,自身还原为
可将气态废弃物中的硫化氢转化为可利用的硫,自身还原为![]() 。工业上常采用如图所示的电解装置,通电电解,然后通入
。工业上常采用如图所示的电解装置,通电电解,然后通入![]() 加以处理。下列说法不正确的是 ( )
加以处理。下列说法不正确的是 ( )

A. 电解时阳极反应式为![]() ]
]
B. 电解时阴极反应式为![]()
C. 当电解过程中有标准状况下 22. 4L 的![]() 生成时,溶液中有 32g S析出(溶解忽略不计)
生成时,溶液中有 32g S析出(溶解忽略不计)
D. 整个过程中需要不断补充![]() 与
与![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子中,能在强酸溶液里大量共存,并且溶液呈无色透明的是( )
A. MnO4-,K+,Na+,SO42- B. Na+,K+,HCO3-,Cl-
C. Mg2+,NH4+,Cl-,NO3- D. Ba2+,K+,S2-,SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com