
����Ŀ���мס�����λͬѧ��������ԭ��ط�Ӧ�������Ļ��˳�����˾�ʹ��þƬ����Ƭ���缫������ͬѧ���缫����6mol L-1��H2SO4��Һ�У���ͬѧ���缫����6mol L-1NaOH����Һ�У���ͼ��ʾ��
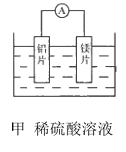
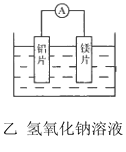
��1��д������������ĵ缫��Ӧʽ��________.
��2��д���ҵ�����ܷ�Ӧ�����ӷ���ʽ��_________.
��3�����������ͬѧ����Ϊ������ԭ��صĵ缫����������ǽ������ɸ������ϵĽ���Ӧ�ȹ����������ϵĽ������á�������жϳ�______(��дԪ�ط���,��ͬ)�Ľ�����Ը�ǿ,���һ��жϳ�___�Ľ�����Ը�ǿ��
��4���ɴ�ʵ�飬�ɵõ�������Щ��ȷ������______��
A������ԭ��ط�Ӧ�жϽ������˳��ʱӦע��ѡ����ʵĽ���
B��þ�Ľ�����Բ�һ�������Ľ������ǿ
C����ʵ��˵���������˳���ѹ�ʱ����û��ʹ�ü�ֵ
D����ʵ��˵����ѧ�о������ӣ���Ӧ������Ӱ��ϴ����Ӧ��������������
��5����5.1gþ���Ͻ�����60 mL5.0 mol L-1H2SO4��Һ��,��ȫ�ܽ���ټ���65mL10.0mol L-1��NaOH��Һ���õ���������Ϊ9.7g�������μ�NaOH��Һʱ��������١�
�ٵ�����____mLNaOH��Һʱ����ʹ�ܽ��������е�Mg2+��Al3+ǡ����ȫ������
�ڼ���Ͻ���������ʱ�������������ڱ�״����Ϊ_____L
���𰸡�2H+ + 2e- = H2�� 2Al + 2OH- + 2H2O = 2AlO2- + 3H2�� Mg Al AD 60 5.6
��������
��1������ܷ�ӦΪMg + 2H+ = Mg2+ + H2�����������ϼ���֪������Al�缫��Al�缫�����H+�õ��ӻ�ԭ��H2���缫��ӦʽΪ2H+ + 2e- = H2����
��2��Mg��Ȼ��Al���ã���Mg����NaOH��Һ��Ӧ����Al���Ժ�NaOH��Ӧ����H2������ҵ���ܷ�Ӧ�����ӷ���ʽΪ2Al + 2OH- + 2H2O = 2AlO2- + 3H2����
��3������������ط�Ӧ��֪���ж�Mg���������������ΪMg�Ƚϻ��ã����һ�۲쵽Al�缫�ܽ⣬��Alʧ���ӣ�Al������������һ���ΪAl�Ƚϻ��á�
��4��A.��Ȼ���ҵ�صĵ缫������ȫ��ͬ�������Һ��ͬ����������������ת���������ԭ��ط�Ӧ�жϽ������˳��ʱӦע��ѡ����ʵĽ��ʣ���ȷ��
B.������������ָ�����Խ�ǿ�Ľ��������ܴӽ�����������Һ���û��������Խϲ�Ľ������ʣ�������ʵ��Mgһ����Al���ã�����
C.�������������жϽ�����ѧ���ʵ���Ի��Ե���Ҫ�ֶΣ�����
D.�����þ���Ļ�ѧ����ʱ����Ӧ�̰���ǿ�н��Ͳ�ͬ�����µ��������⣬Ӧ�����������Դ����Ӷ����ջ�ѧ����ı��ʣ���ȷ��
�ʴ�ѡAD��
��5����n(H2SO4)=0.06L��5mol/L=0.3mol���������е�Mg��Alǡ����ȫ����ʱ����Һ�ɷ�ΪNa2SO4����ʱn(NaOH)=2n(H2SO4)=2��0.3mol=0.6mol������V(NaOH)=0.6mol/10mol/L=0.06L=60mL��
�ڵ�����60mL NaOH��Һʱ��þ��ǡ�ó�����������n(NaOH)=0.065L��10mol/L=0.65molʱ��NaOH���������ʵ���Ϊ��0.65mol-0.6mol=0.05mol��������ӦΪ��Al(OH)3+NaOH=NaAlO2+2H2O�����ܽ��n[Al(OH)3]=0.05mol��m[Al(OH)3]=0.05mol��78g/mol=3.9g�����������е�Mg��Alǡ����ȫ����������ӦΪ��3.9g+9.7g=13.6g���������к���xmolMg��ymolAl����24x+27y=5.1��58x+78y=13.6����ã�x=0.1��y=0.1��
Mg + H2SO4 = MgSO4 + H2��
0.1mol 0.1mol
2Al + 3H2SO4 = Al2(SO4)3 + 3H2��
0.1mol 0.15mol
n(H2)=0.1mol+0.15mol=0.25mol�������������ڱ�״���µ����Ϊ��V(H2)=0.25mol��22.4L/mol=5.6L��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ�������ж���ȷ����
A. ��״���£�2.24L���к���̼̼˫����Ϊ0.3NA
B. 6.4gS2��S4��S8�Ļ������������ԭ����Ϊ0.2NA
C. 1L0.1mol��L-1��������к��⻯�������Ϊ0.1NA
D. 60g�����������Ҵ�����������Ӧʱ���ѵ�C-O����ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Դ�ı��⣬����ʮ�־�Ŀ���DZ������ҵ�ϴӺ�ˮ��ȡ����þ���������£�
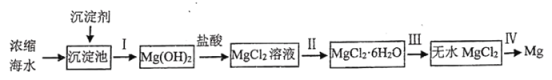
�ش��������⣺
��1����������________________���ѧʽ������ѡ��ͬ����������ʵ�������_______________��
��2������ѡ���У��漰�IJ����������������___________��
A ʵ���Ҵ���ˮ����ȡ�嵥��
B ��ȥ![]() �����е�����NaCl
���������NaCl
C ��![]() �ֽ�����л��
�ֽ�����л��![]()
D �ù�ҵ�ƾ�����ˮ�Ҵ�
��3���ڽ��в����ʱ�����û�м������ᣬ���ܲ�����������______________���ѧʽ����
��4��һ��ģ�ҵ��![]() ����ˮ
����ˮ![]() ��ʵ����������£�
��ʵ����������£�
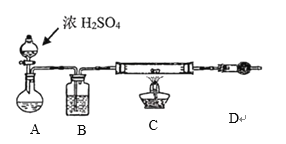
װ��A��ʢ��Һ����______________��װ��D��������____________________________��
��5�������������Ӧ�Ļ�ѧ����ʽ��___________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������A��B��C����Ԫ�أ���֪Bԭ����������A��A��B������֮��Ϊ27��������֮��Ϊ5��0.9gC������������������ �ų���̬��1.12 L������ͬʱ����C�����Ȼ���ش��������⣺
��1��C��Ԫ�ط�����________________��
��2��A��ԭ�ӽṹʾ��ͼ________��
��3��B���⻯��ĵ���ʽ____________��
��4���ų�����Ԫ������������Ӧ��ˮ�����������ǿ������˳��_____��
��5��A��C����Ԫ������������Ӧ��ˮ���ﷴӦ�����ӷ���ʽ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС��Ϊ̽��ͭ��Ũ����ķ�Ӧ������ͼ��ʾװ�ý����й�ʵ�顣��ش�

��1��д��ͭ��Ũ���ᷴӦ�Ļ�ѧ����ʽ:_____________��
��2��װ��D���Թܿڷ��õ����н���NaOH��Һ����������______��
��3��װ��B�������������������塣��D�������Ե�����ر�����K����ȥ�ƾ��ƣ����������ȵ����ã�A�����������������ʱB�е�������__��B��Ӧ���õ�Һ����____(�����)��
A��ˮ B������KMnO4��Һ C��Ũ��ˮ D������NaHSO3��Һ
��4��ȡһ��������ͭƬ��һ�����Ũ��Ϊ18.4 mol��L��1��Ũ�������Բ����ƿ�й��ȣ�ֱ����Ӧ��ϣ�������ƿ��ͭ�����ᶼ��ʣ�ࡣ����ʹ��ƿ��ʣ���ͭƬ�ܽ⣬������ƿ�м��������Լ��е�____������ţ���
A��HNO3 B��NaNO3 C��NaHCO3 D��Na2CO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ߺ������˷ɴ������ҹ��������Ƶ�������һ��D�����ػ�����û������Ҫȼ����ƫ������(��R��ʾ)���������������ڻ������ʱ�����߾��ҷ�Ӧ�����������岢�ͷų��������ȣ��÷�Ӧ�Ļ�ѧ����ʽΪ:R+2N2O4=3N2+4H2O+2CO2����������������ǣ� ��
A.�˷�Ӧ��������ԭ��ӦB.�÷�Ӧ�����Ϊ�ǵ����
C.R�ķ���ʽΪ![]() D.��Ӧ˲����������������壬�ƶ��������
D.��Ӧ˲����������������壬�ƶ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ӻ�������ۺͼ۵��ӶԻ���ģ���жϣ����з��ӻ������ӵ�����ԭ���ӻ���ʽ���ռ乹����ȷ���ǣ� ��
ѡ�� | ���ӻ����� | ����ԭ���ӻ���ʽ | �۵��ӶԻ���ģ�� | ���ӻ����ӵ����幹�� |
A�� | SO2 | sp | ֱ���� | ֱ���� |
B�� | HCHO | sp2 | ƽ�������� | ������ |
C�� | NF3 | sp2 | �������� | ƽ�������� |
D�� |
| sp3 | ���������� | ���������� |
A. AB. BC. CD. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ƹ���������Һ�Ĺ���:��ȡ10.0 g�������ƹ��壬���ձ��м�ˮ�����ܽ������ͼ��ʾ������ƿ����������������Һ���ش��������⣺
(1)______(������������������)���ܽ���������������ת�Ƶ�����ƿ�С�
(2)�����Ƶ�����������Һ�����ʵ���Ũ����_______molL-1.
(3)ȡ�������Ƶ���Һ10 mL����ˮϡ����500 mL��ϡ�ͺ���Һ���ʵ����ʵ���Ũ����_______mol L-1.
(4)��CO2ͨ������������Һ(�������У�д��������Ӧ�Ļ�ѧ����ʽ:__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�������ܶ�Ϊ1.18 g/mL����������Ϊ36.5%Ũ��������250 mL 0.1 mol/L��������Һ����ղ���ش��������⣺
(1)����250 mL 0.1 mol/L��������Һ����Ҫ��ȡŨ����������_____mL(��ȷ��0.1)��
(2)����ʱ������ȷ�IJ���˳����(��ĸ��ʾ��ÿ����ĸֻ����һ��)____________��
A.��30 mLˮϴ���ձ�2��3�Σ�ϴ��Һ��ע������ƿ����
B.����Ͳȷ��ȡ�����Ũ���ᣬ�ز����������ձ��У��ټ�������ˮ(Լ30 mL)���ò���������������ʹ���Ͼ���
C.������ȴ�������ز�����ע��250 mL������ƿ��
D.������ƿ�ǽ�����ҡ��
E.���ý�ͷ�ιܼ�ˮ��ʹ��Һ����ǡ����̶�����
F.����������ƿ��С�ļ�ˮ��ֱ��Һ��ӽ��̶�1��2 cm��
(3)����A�У���ϴ��Һ����������ƿ����Ŀ����_________����Һע������ƿǰ��ָ������£�������Ϊ__________��
(4)�����������������������ҺŨ�Ƚ��к�Ӱ�죨����ƫ��������ƫ����������Ӱ������?��û�н���A����________����������ˮʱ���������˿̶�________��������ʱ���ӿ̶���________��
(5)��ʵ������г������������δ�����
������ˮʱ���������˿̶�____________��
������ƿ��ת����Һʱ(ʵ�鲽���)������Һ�ε�������ƿ����_________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com