
【题目】现有A、B、C三种元素,已知B原子序数大于A,A与B质子数之和为27,质子数之差为5,0.9gC单质与足量盐酸作用 放出标态下1.12 L氢气,同时生成C的三氯化物,回答下列问题:
(1)C的元素符号是________________。
(2)A的原子结构示意图________。
(3)B的氢化物的电子式____________。
(4)排出三种元素最高价氧化物对应的水化物酸碱性由强到弱的顺序_____。
(5)A和C两种元素最高价氧化物对应的水化物反应的离子方程式_______。
【答案】Al 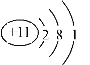
![]() NaOH、Al(OH)3、H2SO4; Al(OH)3+OH-=AlO2-+2H2O
NaOH、Al(OH)3、H2SO4; Al(OH)3+OH-=AlO2-+2H2O
【解析】
设A、B的质子数分别为a、b,则:a+b=27,b-a=5。解得:a=11,b=16,故A为Na元素,B为S元素。据题意:C应为三价金属元素,则有反应通式为:
2C+6H+=2C3++3H2↑
2M(C) 3×22.4L
0.9g 1.12L
解得 M(C)=27,故C为铝元素。
(1)C的元素符号是Al。
(2)A为Na元素,A的原子结构示意图为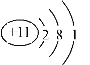 ;
;
(3)B的氢化物为H2S,其电子式为![]() ;
;
(4)三种元素最高价氧化物对应的水化物分别为:NaOH、Al(OH)3、H2SO4,酸碱性由强到弱的顺序为:NaOH、Al(OH)3、H2SO4;
(5)A和C两种元素最高价氧化物对应的水化物反应的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O。
故答案为:(1)Al;(2)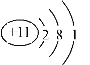 ;(3)
;(3) ![]() ;(4)NaOH、Al(OH)3、H2SO4;(5)Al(OH)3+OH-=AlO2-+2H2O;
;(4)NaOH、Al(OH)3、H2SO4;(5)Al(OH)3+OH-=AlO2-+2H2O;


科目:高中化学 来源: 题型:
【题目】下列对有机物![]() 的叙述中,不正确的是( )
的叙述中,不正确的是( )
A. 它不能使溴水褪色,也不能使酸性KMnO4溶液褪色
B. 在FeBr3作催化剂时与Br2发生取代反应可生成三种一溴代物
C. 在一定条件下可发生加成反应
D. 一定条件下可以和浓硝酸、浓硫酸的混合物发生硝化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明矾石的主要成分是K2SO4·Al2(SO4)3·2Al 2O3·6H2O,还含有少量Fe2O3杂质。利用明矾石制备氢氧化铝的流程如下:
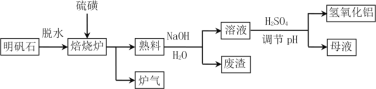
(1)焙烧炉中发生反应的化学方程式为2Al2(SO4)3+3S ![]() 2Al 2O3 +9SO2,该反应的氧化剂是______________,若生成1molAl2O3,则转移的电子数为____________________。
2Al 2O3 +9SO2,该反应的氧化剂是______________,若生成1molAl2O3,则转移的电子数为____________________。
(2)将标况下1.12L炉气通入100mL 0.5mol·L-1 NaOH溶液中,得到一种酸性溶液,则该溶液中各种离子浓度由大到小的排列顺序为___________________________________。
(3)熟料溶解时反应的离子方程式为_________________________。
(4)母液中溶质主要成分的化学式为____________、_____________,溶液调节pH后经过滤、洗涤可得Al(OH)3沉淀,证明沉淀已洗涤干净的实验操作和现象是 ________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素周期表中短周期的一部分,四种元素均不是稀有气体元素。下列关于这四种元素及其化合物的说法中正确的是( )

A. 原子半径:W>Z
B. 气态氢化物的稳定性:W>X
C. W的最高正化合价与负化合价的绝对值可能相等
D. Z的最高价氧化物的水化物可能为强碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将物质的量之比为1:1的Fe、Cu的混合粉末逐渐加入到含1mol![]() 的稀硝酸中充分反应(还原产物全部是NO),则能使硝酸完全反应的金属粉末的最小质量为
的稀硝酸中充分反应(还原产物全部是NO),则能使硝酸完全反应的金属粉末的最小质量为
A.14gB.15gC.18gD.22.5g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不同元素的原子在分子内吸引电子的能力大小可用一定数值x来表示,若x越大,其原子吸引电子的能力越强,在所形成的分子中成为负电荷一方。
下面是某些短周期元素的x值:
元素符号 | Li | Be | B | C | O | F | Na | Al | Si | P | S | Cl |
x值 | 0.98 | 1.57 | 2.04 | 2.55 | 3.44 | 3.98 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
(1)通过分析x值变化规律,确定Mg的x值范围:____<x(Mg)< _____。
(2)推测x值与原子半径的关系是____;根据短周期元素的x值变化特点,体现了元素性质的________变化规律。
(3)某有机化合物结构式为![]() ,其中S—N中,你认为共用电子对偏向谁?__(写原子名称)。
,其中S—N中,你认为共用电子对偏向谁?__(写原子名称)。
(4)经验规律告诉我们:当成键的两原子相应元素的差值(Δx),当Δx>1.7时,一般为离子键,当Δx<1.7时,一般为共价键,试推断AlBr3中化学键类型是______。
(5)预测元素周期表中,x值最小的元素位置:_________
查看答案和解析>>
科目:高中化学 来源: 题型:
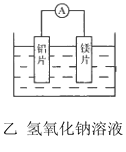
【题目】有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均使用镁片与铝片作电极,但甲同学将电极放入6mol L-1的H2SO4溶液中,乙同学将电极放入6mol L-1NaOH的溶液中,如图所示。
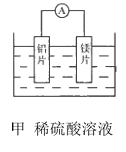
(1)写出甲电池中正极的电极反应式:________.
(2)写出乙电池中总反应的离子方程式:_________.
(3)如果甲与乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出______(填写元素符号,下同)的金属活动性更强,而乙会判断出___的金属活动性更强。
(4)由此实验,可得到如下哪些正确结论(______)
A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
B.镁的金属活动性不一定比铝的金属活动性强
C.该实验说明金属活动性顺序已过时,已没有使用价值
D.该实验说明化学研究对象复杂,反应受条件影响较大,因此应具体问题具体分析
(5)将5.1g镁铝合金溶于60 mL5.0 mol L-1H2SO4溶液中,完全溶解后再加入65mL10.0mol L-1的NaOH溶液,得到沉淀质量为9.7g,继续滴加NaOH溶液时沉淀会减少。
①当加入____mLNaOH溶液时,可使溶解在硫酸中的Mg2+和Al3+恰好完全沉淀。
②计算合金溶于硫酸时所产生的氢气在标准状况下为_____L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从溴乙烷制取1, 2-二溴乙烷,下列转化方案中最好的是
A. CH3CH2Br![]() CH3CH2OH
CH3CH2OH![]() CH2=CH2
CH2=CH2![]() CH2BrCH2Br
CH2BrCH2Br
B. CH3CH2Br![]() CH2BrCH2Br
CH2BrCH2Br
C. CH3CH2Br![]() CH2=CH2
CH2=CH2![]() CH2BrCH3
CH2BrCH3![]() CH2BrCH2Br
CH2BrCH2Br
D. CH3CH2Br![]() CH2=CH2
CH2=CH2![]() CH2BrCH2Br
CH2BrCH2Br
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据vt图分析外界条件改变对可逆反应A(g)+3B(g) ![]() 2C(g) ΔH<0的影响。该反应的速率与时间的关系如图所示:
2C(g) ΔH<0的影响。该反应的速率与时间的关系如图所示:

可见在t1、t3、t5、t7时反应都达到平衡,如果t2、t4、t6、t8时都只改变了一个反应条件,则下列对t2、t4、t6、t8时改变条件的判断正确的是
A. 使用了催化剂、增大压强、减小反应物浓度、降低温度
B. 升高温度、减小压强、减小反应物浓度、使用了催化剂
C. 增大反应物浓度、使用了催化剂、减小压强、升高温度
D. 升高温度、减小压强、增大反应物浓度、使用了催化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com