
【题目】钛被称为继铁、铝之后的第三金属,其单质及化合物在航天、军事、航海、医疗等领域都有着重要的应用。请回答下列问题:
(1)基态Ti 原子的价层电子排布图为________________________。
(2)在TiO、TiN、TiS2、TiCl4等化合物中,S、Cl的电负性大小:S________Cl (填“>”、“<”或“=”)。O、N 的第一电离能大小为O < N,原因是___________________________。
(3)TiCl4的熔点是-23℃,沸点是136℃,可溶于CCl4,该晶体是_______ 晶体。TiCl4中加入大量水,同时加热,可制得二氧化钛的水合物(TiO2·xH2O),再经焙烧可得TiO2,写出生
成二氧化钛水合物(TiO2·xH2O)的化学方程式_________________________________。
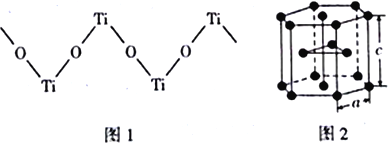
(4)TiO2能溶于浓硫酸并析出一种离子晶体,已知其中阳离子是以链状聚合物形式存在的钛酰阳离子,其结构如下图1所示,其化学式为_____________。阴离子SO42-中硫原子的杂化方式为______________,写出一种与SO42-互为等电子体的分子_____________。
(5)下图2是钛晶体在空间的一种堆积方式,此堆积方式叫______________,钛原子的配位数为____________。已知:a=0.295 nm,c=0.469nm,则该钛晶体的密度为_________g·cm-3(NA表示阿伏加德罗常数的值,列出计算式即可)。
【答案】 ![]() < N原子的2P轨道为半充满状态,具有较高的稳定性,故不易失去一个电子 分子 TiCl4+ (x+2)H2O
< N原子的2P轨道为半充满状态,具有较高的稳定性,故不易失去一个电子 分子 TiCl4+ (x+2)H2O![]() TiO2·xH2O↓+4HCl (TiO)n2n+(或TiO2+) sp3 CCl4(SiCl4等) 六方最密堆积 12
TiO2·xH2O↓+4HCl (TiO)n2n+(或TiO2+) sp3 CCl4(SiCl4等) 六方最密堆积 12 ![]()
【解析】(1). Ti是22号元素,价层电子排布式为3d24s2,所以价层电子排布图为:![]() ,故答案为:
,故答案为:![]() ;
;
(2). Cl元素的非金属性比S强,所以Cl的电负性大于S,N元素的价层电子排布式为2s22p3,是一种半充满的稳定结构,具有较高的稳定性,不易失去一个电子,所以第一电离能O < N,故答案为:<;N原子的2P轨道为半充满状态,具有较高的稳定性,故不易失去一个电子;
(3). 由题中信息可知,TiCl4的熔点和沸点较低,可溶于有机溶剂,说明TiCl4是分子晶体,TiCl4中加入大量水的同时加热,发生水解反应生成TiO2·xH2O,反应的化学方程式为:TiCl4+ (x+2)H2O![]() TiO2·xH2O↓+4HCl,故答案为:分子;TiCl4+ (x+2)H2O
TiO2·xH2O↓+4HCl,故答案为:分子;TiCl4+ (x+2)H2O![]() TiO2·xH2O↓+4HCl;
TiO2·xH2O↓+4HCl;
(4). 由图1可知,每个Ti原子连接2个O原子,每个O原子连接2个Ti原子,说明Ti与O原子的个数比为1:1,则该阳离子的化学式为(TiO)n2n+(或TiO2+),SO42-中硫原子的价层电子对数为:4+![]() =4+0=4,所以硫原子的杂化方式为sp3,SO42-的原子数为5、价层电子数为32,根据等电子体原理,与SO42-互为等电子体的分子有:CCl4、SiCl4等,故答案为:(TiO)n2n+(或TiO2+);sp3;CCl4(SiCl4等);
=4+0=4,所以硫原子的杂化方式为sp3,SO42-的原子数为5、价层电子数为32,根据等电子体原理,与SO42-互为等电子体的分子有:CCl4、SiCl4等,故答案为:(TiO)n2n+(或TiO2+);sp3;CCl4(SiCl4等);
(5). 由图2可知,此堆积方式为六方最密堆积,与Ti原子最近且等距离的Ti原子有12个,所以钛原子的配位数为12,该六棱柱含有的钛原子数为6个,质量为![]() g,六棱柱的体积为
g,六棱柱的体积为![]() cm3,则该钛晶体的密度为
cm3,则该钛晶体的密度为![]() g·cm-3,故答案为:六方最密堆积;12;
g·cm-3,故答案为:六方最密堆积;12;![]() 。
。


科目:高中化学 来源: 题型:
【题目】关于反应2KI+O3+H2O ==2KOH+I2+O2,下列说法正确的是
A.当有2 molKI被氧化时,2 mol氧原子被还原
B.O2是还原产物
C.若消耗2.24 L O3,则转移0.2 mol电子
D.氧化剂与还原产物的物质的量之比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】指甲花中存在的β-紫罗蓝酮属于一种萜类化合物,可作为合成维生素A的原料。下列有关β-紫罗蓝酮的说法正确的是
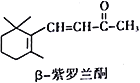
A. β-紫罗蓝酮的分子式为C10H14O
B. 分子中所有碳原子可能处于同一平面
C. 与足量的H2反应后,分子中官能团的种类减少一种
D. 和酸性KMnO4溶液、溴的四氯化碳溶液发生的反应类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正在研发的锂空气电池能量密度高、成本低,可作为未来电动汽车的动力源,其工作原理如图。下列有关该电池的说法正确的是
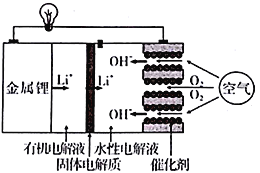
A. 有机电解液可以换成水性电解液
B. 放电时,外电路通过2 mol 电子,消耗氧气11.2 L
C. 放电和充电时,Li+迁移方向相同
D. 电池充电时,在正极上发生的反应为4OH--4e-= O2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】仔细分析下列实验:
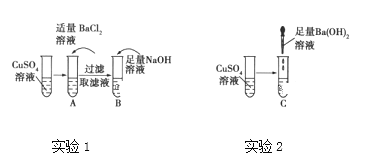
A、B、C试管中的现象如表所示:
试管 | A | B | C |
现象 | 产生白色沉淀, 溶液仍为蓝色 | 产生蓝色沉淀, 溶液变为无色 | 产生蓝色沉淀, 溶液变为无色 |
写出A、B、C试管中所发生反应的离子方程式。
(1)A:______________________________________________。
(2)B:______________________________________________。
(3)C:______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的铁粉加入100mL稀硫酸中,为中和过量硫酸,且使Fe2+完全转化为Fe(OH)2,共消耗掉2mol·L-1NaOH溶液150mL。原硫酸溶液的浓度是
A. 0.5mol·L-1 B. 1mol·L-1 C. 1.5mol·L-1 D. 2mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】既可用来鉴别甲烷与乙烯,又可除去甲烷中混有乙烯的最佳方法是 ( )
A.通入酸性高锰酸钾溶液中B.通入足量溴水中
C.一定条件下通入H2D.通入水中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com