
【题目】含绒量是决定羽绒服质量优劣最重要的指标,按照我国实施的羽绒服新国标,羽绒服的含绒量要在50%以上,一些不法厂家填充“飞丝”或“人造羊毛来假冒羽绒,严重损害消费者的利益。“飞丝”由鸭毛、鹅毛甚至鸡毛经粉碎而成,人造羊毛的主要成分是聚丙烯腈纤维。请回答下列问题:
Ⅰ.鸭绒、蚕丝、人造羊毛都是高分子化合物,下列说法正确的是________(填序号)。
A.通过灼烧的方法可鉴别羽绒服中填充的是鸭绒还是飞丝
B.将人造羊毛和棉花进行混纺可提高纤维的性能
C.鸭绒、蚕丝、人造羊毛都有固定的熔沸点
D.鸭绒、蚕丝、人造羊毛燃烧过程中不会产生有毒气体
Ⅱ.合成聚丙烯腈纤维的方法很多,如以乙炔为原料,其合成过程如下:
CH≡CH+HCN![]() CH2=CHCN
CH2=CHCN![]() 聚丙烯腈
聚丙烯腈
(1)反应①的反应类型为__________。
(2)写出反应②的化学方程式:__________________,其反应类型为_________。
(3)CH2=CHCN在一定条件下可与苯乙烯(![]() )反应得到一种优良的塑料,该塑料的结构简式为__________。
)反应得到一种优良的塑料,该塑料的结构简式为__________。
【答案】B 加成反应 nCH2=CHCN![]()
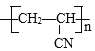 加聚反应
加聚反应 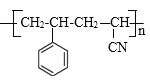 (或
(或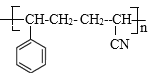 )
)
【解析】
I.根据物质的组成成分、元素组成、物质的性质分析解答;
II.乙炔与HCN发生加成反应产生CH2=CHCN,CH2=CHCN发生加聚反应产生聚丙烯腈。CH2=CHCN与苯乙烯(![]() )在一定条件下可发生加聚反应产生高聚物
)在一定条件下可发生加聚反应产生高聚物 、
、 。
。
Ⅰ.A.鸭绒和飞丝的主要成分都属于蛋白质,在灼烧过程中都有烧焦羽毛的气味,故不能用灼烧的方法鉴别,A错误;
B.人造羊毛属于合成纤维,优点在于强度高、弹性好、耐磨、耐化学腐蚀、不发霉、不怕虫蛀、不缩水等,其缺点在于不透气、不吸汗等,棉花则具有吸汗、透气性强的优点,但又有不耐磨、不耐腐蚀的缺点,若把它和棉花混纺,这样制成的混纺织物兼有两类纤维的优点,B正确;
C.高分子化合物都属于混合物,混合物没有固定的熔、沸点,C错误;
D.鸭绒飞丝、人造羊毛组成成分是蛋白质,含有C、H、O、N元素,有的蛋白质还含有S元素,在燃烧过程中会释放出如SO2、CO、氮氧化物等有毒气体,D错误;
故合理选项是B;
Ⅱ.(1) CH≡CH 与HCN发生加成反应生成CH2=CHCN,故①反应的反应类型为加成反应;
(2)CH2=CHCN在引发剂作用下发生加聚反应生成聚丙烯腈,反应方程式为:nCH2=CHCN![]()
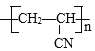 ;
;
(3)CH2=CHCN在一定条件下可与苯乙烯(![]() )在一定条件下发生加聚反应产生高聚物
)在一定条件下发生加聚反应产生高聚物 或
或 。
。


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
【题目】核黄素又称为维生素B2,可促进发育和细胞再生,有利于增进视力,减轻眼睛疲劳。核黄素分子的结构为:

已知:
有关核黄素的下列说法中,不正确的是:
A.该化合物的分子式为C17H22N4O6
B.酸性条件下加热水解,有CO2生成
C.酸性条件下加热水解,所得溶液加碱后有NH3生成
D.能发生酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从环己烷可制备1,4-环己二醇,下列有关7步反应(其中无机产物都已略去),其中有3步属于加成反应。(提示:路线⑤的反应可利用1,3-环己二烯与Br2的1,4-加成反应)请回答下列问题:
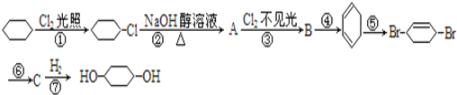
(1)分别写出B、C的结构简式:B_________________、C_________________。
(2)写出反应类型④_________________,⑤_________________,⑥_________________。
(3)写出反应①的化学方程式________________________________________________。(有机物写结构简式,并注明反应条件)
(4)写出反应②的化学方程式________________________________________________(有机物写结构简式,并注明反应条件)
(5)写出反应⑥的化学方程式________________________________________________(有机物写结构简式,并注明反应条件)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中科院某课题组将二氧化锰和生物质置于一个由滤纸制成的折纸通道内形成电池(如图所示),该电池可将可乐(pH=2.5)中的葡萄糖作为燃料获得能量。下列说法中正确的是( )
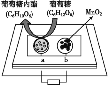
A. a极为正极
B. 随着反应不断进行,负极区的pH不断增大
C. b极电极反应式为MnO2+2H2O+2e-=Mn2++4OH-
D. 消耗0.01mol葡萄糖,电路中转移0.02mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M是表面分子、药物的中间体,N是一种高分子化合物。实验室由A、B两种烃制备M和N一种合成路线如下: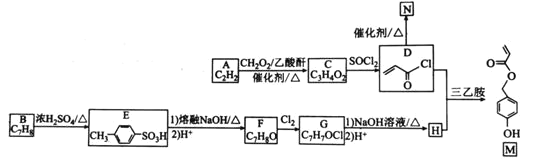
已知:![]()
回答下列问题:
(1)B的化学名称为________。N的结构简式为_____________________。
(2)由A生成C的反应类型为____。G中官能团的名称为______________。
(3)由F转化为G的条件为________________________________。
(4)由D和H生成M的化学方程式为_________________________。
(5)![]() 是M的同分异构体,同时满足下列条件的X的结构有_________种。
是M的同分异构体,同时满足下列条件的X的结构有_________种。
①能与![]() 溶液发生显色反应
溶液发生显色反应
②能发生银镜反应,且![]() 最多生成
最多生成![]()
③核磁共振氢谱中有5组吸收峰
(6)参照上述合成路线和信息,设计以苯和甲醛为原料制备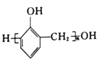 的合成路线
的合成路线![]() 无机试剂任选
无机试剂任选![]() :________________________________。
:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组在网上收集到如下信息:以贫软锰矿和有色金属冶炼厂的![]() 废气为原料制备高纯碳酸锰.已知,贫软锰矿的主要成分为
废气为原料制备高纯碳酸锰.已知,贫软锰矿的主要成分为![]() 和少量
和少量![]() 、
、![]() 、
、![]() 等杂质.工艺流程如图1:
等杂质.工艺流程如图1:

已知:有关氢氧化物沉淀pH对应表
物质 | 开始沉淀时的pH | 完全沉淀时的pH |
氢氧化铁 |
|
|
氢氧化铝 |
|
|
氢氧化亚铁 |
|
|
请回答:
![]() 在浸出液除杂过程中需通入适量空气并调节溶液的pH到
在浸出液除杂过程中需通入适量空气并调节溶液的pH到![]() ,沉淀部分杂质离子,此时滤渣I中主要含有 ______
,沉淀部分杂质离子,此时滤渣I中主要含有 ______ ![]() 填化学式
填化学式![]() .
.
![]() 影响浸锰率的操作因素有多种,其中温度选择不合理时会产生杂质
影响浸锰率的操作因素有多种,其中温度选择不合理时会产生杂质![]() 造成锰损失.温度对浸锰率的影响见图2、图3.
造成锰损失.温度对浸锰率的影响见图2、图3.
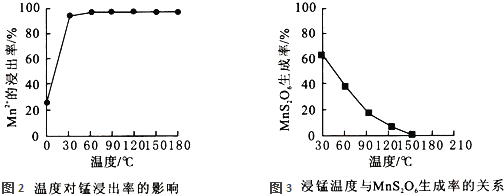
为了提高锰的浸出率,请选择合适的条件 ______ ![]() 填序号
填序号![]()
![]() 以上
以上
![]() 在滤液中加入
在滤液中加入![]() 生成
生成![]() 的同时还可以获得一种作为肥料的副产物,写出该过程的化学反应方程式 ______ ,从废液中分离出该副产物的操作是蒸发浓缩、 ______
的同时还可以获得一种作为肥料的副产物,写出该过程的化学反应方程式 ______ ,从废液中分离出该副产物的操作是蒸发浓缩、 ______ ![]() 若该分离过程在实验室进行,其中除了需要酒精灯、蒸发皿、玻璃棒外,还需要 ______ .
若该分离过程在实验室进行,其中除了需要酒精灯、蒸发皿、玻璃棒外,还需要 ______ .
![]() 现有含锰质量分数为
现有含锰质量分数为![]() 的贫锰矿1吨,若按照上述工艺锰的产率为
的贫锰矿1吨,若按照上述工艺锰的产率为![]() ,最终获得碳酸锰的质量 ______ .
,最终获得碳酸锰的质量 ______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于该物质,下列说法正确的是()
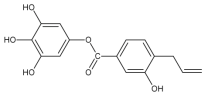
A.1mol该物质最多与8mol H2发生加成反应
B.1mol该物质最多与5mol Br2反应
C.1mol该物质最多与6mol NaOH发生反应
D.可以用酸性高锰酸钾溶液检验该物质中含有碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研小组公司开发了Li-SO2Cl2军用电池,其示意图如下图所示,已知电池反应为:2Li+SO2Cl2═2LiCl+SO2↑;下列叙述中错误的是( )
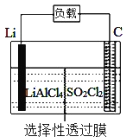
A.电池工作时负极材料是Li,发生氧化反应
B.将电解质溶液改为LiCl的水溶液,电池性能会更好
C.电池工作时电子流向:锂电极→导线→负载→导线→碳棒
D.电池工作过程中,石墨电极反应式为SO2Cl2+2e-═2Cl-+SO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌的化合物在工农业生产中有广泛的应用。请回答下列问题:
(1)基态锌原子中,核外电子占据的最高能级的符号是_________。锌的熔点比铝的熔点低,原因是______________。
(2)锌冶炼过程中会产生污染性气体二氧化硫,已知液态二氧化硫可以发生类似于水的自身电离2SO2(l)![]() SO2++
SO2++![]() ,S和O两种元素中电负性较强的是_______,与SO2+互为等电子体的单质分子为_______(填化学式),SO2+中的σ键和π键数目比为______________。
,S和O两种元素中电负性较强的是_______,与SO2+互为等电子体的单质分子为_______(填化学式),SO2+中的σ键和π键数目比为______________。
(3) [Zn(CN)4]2在水溶液中与HCHO发生如下反应:4HCHO+[Zn(CN)4]2+4H++4H2O![]() [Zn(H2O)4]2++4HOCH2CN,HOCH2CN分子中碳原子轨道的杂化类型是_________,HCHO的立体构型为_______________,[Zn(CN)4]2中Zn2+与CN中的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2的结构可用示意图表示为__________________。
[Zn(H2O)4]2++4HOCH2CN,HOCH2CN分子中碳原子轨道的杂化类型是_________,HCHO的立体构型为_______________,[Zn(CN)4]2中Zn2+与CN中的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2的结构可用示意图表示为__________________。
(4)硒化锌是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为_________。若该晶胞密度为ρ g·cm3,硒化锌的摩尔质量为M g/mol,NA代表阿伏加德罗常数,则晶胞参数a为__________cm。
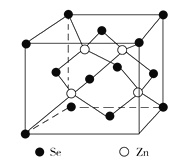
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com