
【题目】核黄素又称为维生素B2,可促进发育和细胞再生,有利于增进视力,减轻眼睛疲劳。核黄素分子的结构为:

已知:
有关核黄素的下列说法中,不正确的是:
A.该化合物的分子式为C17H22N4O6
B.酸性条件下加热水解,有CO2生成
C.酸性条件下加热水解,所得溶液加碱后有NH3生成
D.能发生酯化反应
 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:
【题目】氯化铁是常见的水处理剂。某氯化铁(FeCl36H2O)样品含有少量FeCl2杂质。现要测定其中FeCl36H2O的质量分数,实验按以下步骤进行:
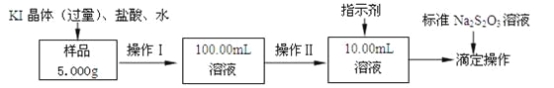
已知有关离子方程式为:2Fe3++2I-═2Fe2++I2,I2+2S2O32-═2I-+S4O62-
(1)取少量氯化铁样品滴入50mL沸水中,加热片刻,液体呈现红褐色,反应的离子方程式为:________________________。
(2)操作I所用到的玻璃仪器除烧杯、玻璃棒外,还必须有________、_________(填仪器名称)。
(3)操作II必须用到的仪器是________(选填编号);
a.50mL烧杯 b.10mL量筒 c.20mL量筒 d.25mL滴定管
指示剂是淀粉溶液,则达到滴定终点的现象是__________________________。
(4)滴定时,消耗浓度为0.1000mol/L的标准Na2S2O3溶液18.00mL。该样品中FeCl36H2O(式量为270.5)的质量分数为_____________。
(5)要把样品氯化铁中的少量FeCl2杂质除去,可用的试剂是________(选填编号)。
a.铁粉 b.氯水 c.溴水 d.双氧水
(6)如果采用以下步骤测定氯化铁样品元素的含量,完成下列填空。
①称量样品 ②加水溶解 ③加足量氨水,沉淀 ④过滤 ⑤灼烧 ⑥称量并进行恒重操作。
还缺少的一步操作是________;在过滤前,需要检验是否沉淀完全,其操作___________________;判断是否恒重的标准是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A为烃类化合物,质谱图表明其相对分子质量为70,其相关反应如图所示,其中B、D、E的结构中均含有2个![]() ,它们的核磁共振氢谱中均出现4个峰.
,它们的核磁共振氢谱中均出现4个峰.
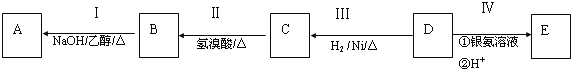
请回答:
![]() 中所含官能团的名称为______;D的分子式为______;
中所含官能团的名称为______;D的分子式为______;
![]() Ⅲ的反应类型为______
Ⅲ的反应类型为______![]() 填字母序号
填字母序号![]() ;
;
![]() 还原反应
还原反应![]() 加成反应
加成反应![]() 氧化反应
氧化反应![]() 消去反应
消去反应
![]() 写出下列反应的化学方程式:
写出下列反应的化学方程式:
Ⅰ:______;
Ⅱ:______;
![]() 和E可在一定条件下反应生成F,F为有香味的有机化合物,该反应的化学方程式为______;
和E可在一定条件下反应生成F,F为有香味的有机化合物,该反应的化学方程式为______;
![]() 的同分异构体中有一对互为顺反异构,且结构中有2个
的同分异构体中有一对互为顺反异构,且结构中有2个![]() ,它们的结构简式为______和______;
,它们的结构简式为______和______;
![]() 的另一种同分异构体能发生银镜反应,能与足量金属钠生成氢气,不能发生消去反应,其结构简式为______。
的另一种同分异构体能发生银镜反应,能与足量金属钠生成氢气,不能发生消去反应,其结构简式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用含锂废渣(主要金属元素的含量:Li 3.50% Ni 6.55% Ca 6.41% Mg 13.24%)制备Li2CO3,并用其制备锂电池的正极材料LiFePO4。部分工艺流程如下:
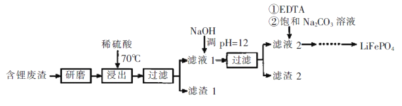
资料:i滤液1、滤液2中部分例子浓度(g·L-1)
Li+ | Ni2+ | Ca2+ | Mg2+ | |
滤液1 | 22.72 | 20.68 | 0.36 | 60.18 |
滤液2 | 21.94 | 7.7×10-3 | 0.08 | 0.78×10-3 |
ii.EDTA能和某些二价金属离子形成稳定的水溶性络合物
iii.某些物质的溶解度(S)
T/℃ | 20 | 40 | 60 | 80 | 100 |
S(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 |
S(Li2SO4)/g | 34.7 | 33.6 | 32.7 | 31.7 | 30.9 |
I.制备Li2CO3粗品
(1)上述流程中为加快化学反应速率而采取的措施是____。
(2)滤渣2的主要成分有____。
(3)向滤液2中先加入EDTA,再加入饱和Na2C03溶液,90℃充分反应后,分离出固体 Li2CO3粗品的操作是_______。
(4)处理lkg含锂3.50%的废渣,锂的浸出率为a,Li+转化为Li2CO3的转化率为b,则粗品中含Li2CO3的质量是________g。(摩尔质量:Li2CO3 74 g.mol4)
II.纯化Li2CO3粗品
(5)将Li2CO3转化为LiHCO3后,用隔膜法电解LiHCO31溶液制备高纯度的LiOH,再转化得电池级Li2CO3。电解原理如图所示,阳极的电极反应式是____,该池使用了_________(填“阳”或“阴”)离子交换膜。
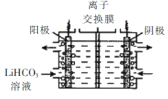
Ⅲ.制备 LiFePO4
(6)将电池级Li2CO3和C、FePO4高温下反应,生成LiFePO4和一种可燃性气体,该反应的化学方程式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列溶液的有关计算。
(1)某H2SO4溶液的浓度是0.005molL-1;
①此溶液的pH=___;
②该溶液中由水电离的c(H+)为___。
③用水稀释到原来体积的100倍,pH=___。
(2)0.001mol/L的NaOH溶液, pH=___;
(3)0.015mol/L的H2SO4与0.01mol/L的NaOH等体积混合,混合液pH=___。
(4)把pH=3的H2SO4溶液和pH=10的NaOH溶液混合,两者恰好中和,则两种溶液的体积比应是___。
A.10∶1 B.1∶10 C.1∶100 D.1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等子中子数。
(1)在CB3分子中C元素原子的原子轨道发生的是____杂化,CB3分子的空间构型为____。
(2)C的氢化物极易溶于水的原因是____。
(3)D元素与同周期相邻元素的第一电离能由大到小的关系是:____(用元素符号表示);
(4)氧原子的价层电子的轨道表示式为____。
(5)X与Y所形成化合物晶体的晶胞如图所示。
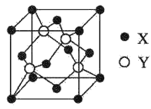
①在一个晶胞中,X离子的数目为____;
②若该化合物的密度为ag·cm-3,则晶胞的体积是____cm3(只要求列出计算式,阿伏加德罗常数用NA表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是应用广泛的金属。以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料制备铝的一种工艺流程如下:

注:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时生成偏铝酸钠的离子方程式为_____________________。
(2)向“过滤Ⅰ”所得滤液中加入NaHCO3溶液,溶液的pH_________ (填“增大”、“不变”或“减小”)。
(3)“电解Ⅰ”是电解熔融Al2O3,电解过程中作阳极的石墨易消耗,原因是___________。
(4)“电解Ⅱ”是电解Na2CO3溶液,原理如图所示。阳极的电极反应式为_____________________,阴极产生的物质A的化学式为____________。
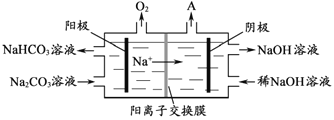
(5)铝粉在1000℃时可与N2反应制备AlN。在铝粉中添加少量NH4Cl固体并充分混合,有利于AlN的制备,其主要原因是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列8种与人们生产生活相关的有机物:① HCHO(防腐剂)② CH3CH2CHO(化工原料)③CH3CH2CH2CH3(打火机燃料)④ ![]() (冷冻剂)⑤
(冷冻剂)⑤ ![]() (汽车防冻液)⑥
(汽车防冻液)⑥ ![]() (杀菌剂)⑦
(杀菌剂)⑦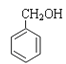 (定香剂)⑧
(定香剂)⑧ ![]() (汽油添加剂)请回答:
(汽油添加剂)请回答:
(1)属于醇的是____(填序号,下同)。
(2)互为同系物的是_____。
(3)互为同分异构体的是__。
(4)用系统命名法给④命名,其名称为_____。
(5)写出②与银氨溶液发生银镜反应的化学方程式__。
(6)写出⑧与浓硝酸反应生成TNT的化学方程式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含绒量是决定羽绒服质量优劣最重要的指标,按照我国实施的羽绒服新国标,羽绒服的含绒量要在50%以上,一些不法厂家填充“飞丝”或“人造羊毛来假冒羽绒,严重损害消费者的利益。“飞丝”由鸭毛、鹅毛甚至鸡毛经粉碎而成,人造羊毛的主要成分是聚丙烯腈纤维。请回答下列问题:
Ⅰ.鸭绒、蚕丝、人造羊毛都是高分子化合物,下列说法正确的是________(填序号)。
A.通过灼烧的方法可鉴别羽绒服中填充的是鸭绒还是飞丝
B.将人造羊毛和棉花进行混纺可提高纤维的性能
C.鸭绒、蚕丝、人造羊毛都有固定的熔沸点
D.鸭绒、蚕丝、人造羊毛燃烧过程中不会产生有毒气体
Ⅱ.合成聚丙烯腈纤维的方法很多,如以乙炔为原料,其合成过程如下:
CH≡CH+HCN![]() CH2=CHCN
CH2=CHCN![]() 聚丙烯腈
聚丙烯腈
(1)反应①的反应类型为__________。
(2)写出反应②的化学方程式:__________________,其反应类型为_________。
(3)CH2=CHCN在一定条件下可与苯乙烯(![]() )反应得到一种优良的塑料,该塑料的结构简式为__________。
)反应得到一种优良的塑料,该塑料的结构简式为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com