
����Ŀ��������X���ȷֽ⣬�ɵ�A��B��D��E��F��ˮ���ֲ������A��B��D������ѧ��ѧ�г��������������E�ǵ���F����Ԫ�ص��⻯�
��1��A������ǿ�ᡢǿ�д��A��ǿ����Һ��Ӧ�����ӷ���ʽ ��
��2��B��D�������������������Ԫ����ͬ��D����ˮ��ǿ�ᣬ��B��D�����г���Ԫ����������һ��Ԫ�������ڱ��е�λ���� ��
��3��E��ʹʪ��ĺ�ɫʯ����ֽ������ʵ������ȡE����Ļ�ѧ����ʽΪ �� �Ƶõ����������ͼ��ʾװ���ռ���������Ӧ�����A����B����ͨ�룮
��4���ɸ��ֽ��������ʵ���֮���Ʋ�X��������������������仯ѧʽΪ �� ����X��Ũ��Һ�еμ�ŨNaOH��Һ����������������Ϊ���� ��
��5��ȡһ������X����ֽ⣬������F 1mol�����ͬʱ��������mol�� 
���𰸡�
��1��Al2O3+2OH��=2AlO2��+H2O
��2���������ڡ���A��
��3��2NH4Cl+Ca��OH��2 ![]() CaCl2+2NH3��+2H2O��B
CaCl2+2NH3��+2H2O��B
��4��NH4Al��SO4��2?12H2O�����ɰ�ɫ���������ɴ̼�����ζ�����壻��ɫ�������ܽ�
��5��SO2��3
���������⣺��1����������ǿ����������ǿ��ij���������AΪAl2O3 �� ��ǿ����Һ��Ӧ�����ӷ���ʽΪ��Al2O3+2OH��=2AlO2��+H2O���ʴ�Ϊ��Al2O3+2OH��=2AlO2��+H2O����2����B��D�������������������Ԫ����ͬ��B��D�����г�����������һ��Ԫ�������ֻ������е����������ֱ�Ϊ50%��40%����֪B��D�ֱ�ΪSO3��SO2 �� ��Ԫ�������ڱ��е������ǵ������ڵڢ�A�壬
�ʴ�Ϊ���������ڡ���A�壻��3��E��ʹʪ��ĺ�ɫʯ����ֽ��������EΪNH3 �� ʵ�����Ʊ������ķ���ʽΪ��2NH4Cl+Ca��OH��2 ![]() CaCl2+2NH3��+2H2O�����ڰ������ܶȱȿ���С��Ӧ�������ſ������ռ�����Ӧ��B��ͨ�������ռ���
CaCl2+2NH3��+2H2O�����ڰ������ܶȱȿ���С��Ӧ�������ſ������ռ�����Ӧ��B��ͨ�������ռ���
�ʴ�Ϊ��2NH4Cl+Ca��OH��2 ![]() CaCl2+2NH3��+2H2O��B����4���������Ϸ�����֪��X�к��������ӡ�笠����ӡ���������ӣ��ٽ��X�������������������֪�仯ѧʽΪ��NH4Al��SO4��212H2O��NH4Al��SO4��212H2O����Һ�к���笠����Ӻ������ӣ���������������Һ���������������������ӷ�Ӧ��������������ɫ�����������ӷ�Ӧ��ȫ��笠����������������ӷ�Ӧ���ɰ���������ɫ�����������������ܽ⣬
CaCl2+2NH3��+2H2O��B����4���������Ϸ�����֪��X�к��������ӡ�笠����ӡ���������ӣ��ٽ��X�������������������֪�仯ѧʽΪ��NH4Al��SO4��212H2O��NH4Al��SO4��212H2O����Һ�к���笠����Ӻ������ӣ���������������Һ���������������������ӷ�Ӧ��������������ɫ�����������ӷ�Ӧ��ȫ��笠����������������ӷ�Ӧ���ɰ���������ɫ�����������������ܽ⣬
�ʴ�Ϊ��NH4Al��SO4��212H2O�����ɰ�ɫ���������ɴ̼�����ζ�����壻��ɫ���������ܽ⣻��5������1molN2ת��6 mol���ӣ����ݵ����غ��غ㣬����SO2�����ʵ���Ϊ�� ![]() =3mol��
=3mol��
�ʴ�Ϊ��SO2��3��
��1����������ǿ����������ǿ��ij���������AΪAl2O3����2����B��D�������������������Ԫ����ͬ��B��D�����г�����������һ��Ԫ�������ֻ������е����������ֱ�Ϊ50%��40%����֪B��D�ֱ�ΪSO3��SO2����3��E��ʹʪ��ĺ�ɫʯ����ֽ��������EΪNH3�����ݰ������ܶȴ�Сѡ���ռ���������4��X�����������������������Ϸ���д������X�Ļ�ѧʽ��NH4Al��SO4��212H2O��Һ�к���笠����ӡ������ӣ���������������Һ�������ɰ�ɫ������Ȼ���������������ɫ�����ܽ⣬�ݴ˽��н�𣻣�5������1molN2ת��6 mol���ӣ����ݵ����غ��������SO2�����ʵ�����


 ��ĩ���ƾ�ϵ�д�
��ĩ���ƾ�ϵ�д� ���ɿ��ñ���ϵ�д�
���ɿ��ñ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�������ȷ�Ӧ���ǣ� ��
A.̿ȼ������һ����̼
B.�кͷ�Ӧ
C.п����ϡ���ᷴӦ��ȡH2
D.Ba��OH��28H2O��NH4Cl��
Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��������þ���������Ͷ�뵽1mol��L��1�������У���������ȫ�ܽ������Һ�м���1mol��L��1������������Һ�����ɳ������������������������Һ�������ϵ����ͼ��ʾ����
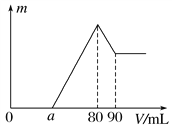
��1��������������Ϊ________��
��2��a��ȡֵ��Χ��________________��
��3��![]() �����ֵ��________��
�����ֵ��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У��ܹ����������ڵ���ʵ��ǣ� ��
A.CuB.Һ̬�Ȼ���C.����D.Һ̬�Ȼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ж�Ӧ��ϵ��ȷ����
ѡ�� | �������ʵ | ���ͻ���� |
A | CuSO4+H2S===CuS��+H2SO4 | �÷�Ӧ���ܷ�������Ϊ����H2SO4>H2S |
B | ���Ȼ�����Һ��ͨ��CO2��δ���ְ�ɫ���� | CO2����������̼����� |
C | �ü�����������������Һ�е��뼸��ϡ���ᣬ�ж�������� | �����˹��ὺ�� |
D | ��ij��Һ���ȵμ���ˮ�ٵμ�KSCN����Һ��� | ��Һ�к���Fe2+ |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£��ڹ̶��ݻ������Ϊ2L���ܱ������г���1mol N2��3mol H2������Ӧ������Ӧ���е�10sĩʱ��Ӧ�ﵽƽ�⣬��ʱ������c��NH3��=0.1molL��1 �� �����й��жϴ�����ǣ� ��
A.��Ӧ��ƽ��ʱN2��ת����Ϊ10%
B.��Ӧ���е�10 sĩʱ��H2��ƽ����Ӧ������0.03 mol��Ls����1
C.�÷�Ӧ�ﵽƽ��ʱ��N2��ƽ��Ũ��Ϊ0.45 mol/L
D.�÷�Ӧ�ﵽƽ��ʱ��ѹǿ����ʼʱѹǿ��0.95��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼװ�ã��Թ���ʢ��ˮ������a��ʢ�и����Na2O2������U�ι���ע��dz��ɫ��ˮ������������Ƥ��������Թܿڣ�ʵ��ʱ�������е�Na2O2���䵽�Թ�b��ˮ�У���������������
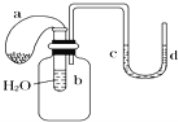
A. U�ι��ں�ɫ��ȥ
B. �Թ�����Һ���
C. ����a���
D. U�ι�ˮλd��c
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б�ʾ��Ӧ��ѧ��Ӧ�����ӷ���ʽ��ȷ���ǣ� ��
A.��KIO3����������Һ�е�KI��5I��+IO3��+3H2O�T3I2+6OH��
B.������SO2ͨ���䰱ˮ�У�SO2+NH3H2O�THSO3��+NH4+
C.��NH4HCO3��Һ�мӹ�����NaOH��Һ�����ȣ�NH4++OH���TNH3��+H2O
D.��ϡ����ϴ���Թ��ڱڵ�������Ag+2H++NO3���TAg++NO��+H2O
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com