
【题目】将等物质的量的A、B混合于2L的密闭容器中,发生反应3A(g)+B(g)xC(g)+2D(g),经5s后,测得D的浓度为0.5mol/L,c(A):c(B)=3:5,v(C)为0.1mol/(L·s)
求:(1)x的值;___________
(2)以B表示的该反应的平均反应速率;___________
(3)此时A的浓度及反应开始前放入容器中的A、B的物质的量。___________
【答案】2 0.05mol/(L·s) 0.75mol/L,3mol,3mol
【解析】
根据C、D物质的化学反应速率之比等于化学计量数之比可以得到x的值;根据B和D的速率之比等于计量数之比计算;根据“三段式”找出A的浓度及反应开始前放入容器中的A、B的物质的量。
(1)v(C)为0.1mol/(L·s),v(D)=![]() =
=![]() = 0.1mol/(L·s), v(C):v(D)=2:x=1:1,x=2;
= 0.1mol/(L·s), v(C):v(D)=2:x=1:1,x=2;
(2)根据化学方程式,3A(g)+B(g)xC(g)+2D(g),v(B):v(D)=1:2,v(D)=![]() =
=![]() = 0.1mol/(L·s),v(B)= 0.05mol/(L·s);
= 0.1mol/(L·s),v(B)= 0.05mol/(L·s);
(3)设A、B的初始物质的量为n,
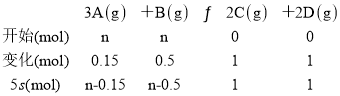
在相同的容器中,c(A):c(B)=3:5,故A和C的物质的量之比也为3:5,(n-1.5):(n-0.5)=3:5,n=3mol,5min后,A的浓度为=![]() =0.75mol/L,开始前放入容器中的A、B的物质的量都为3mol。
=0.75mol/L,开始前放入容器中的A、B的物质的量都为3mol。


科目:高中化学 来源: 题型:
【题目】(1)Co、Cu、Zn都是过渡元素,可作为中心原子形成多种配合物,下列不能作为配合物配位体的是______;
A.H2O B.NH3 C.CH4 D.Cl﹣
(2)用氢键表示式写出氨水中NH3分子与水分子间可能存在的氢键____;
(3)Cu元素可形成[Cu(NH3)4]SO4,其中存在的化学键类型有______(填序号);
①配位键 ②氢键 ③极性共价键 ④非极性共价键 ⑤离子键
(4)甲烷晶体的晶胞结构如下图,下列有关说法正确的是_______。
A.甲烷在常温下呈气态,说明甲烷晶体属于分子晶体
B.晶体中1个CH4分子有12个紧邻的甲烷分子
C.CH4晶体熔化时需克服共价键

(5)下图表示的是SiO2的晶胞结构(白圈代表硅原子,黑点代表氧原子),判断在30g二氧化硅晶体中含______mol Si-O键。如果该立方体的边长为a cm,用NA 表示阿伏加德罗常数,则SiO2晶体的密度表达式为__________________g/cm3 。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有:H、C、O、S、Cl、Fe六种元素,则回答下列有关其性质:
![]() 原子价电子的排布为 ______ ;Cl位于周期表中位置: ______ ;C原子核外有 ______ 个能级。
原子价电子的排布为 ______ ;Cl位于周期表中位置: ______ ;C原子核外有 ______ 个能级。
![]() 用“
用“![]() ”或“
”或“![]() ”填空:还原性:HCl ______
”填空:还原性:HCl ______ ![]() ,半径:C ______ O
,半径:C ______ O
![]() 在NaOH溶液中用Fe作阳极,通过电解制取
在NaOH溶液中用Fe作阳极,通过电解制取![]() 的电极反应式为: ______
的电极反应式为: ______
![]() 已知1molS完全燃烧生成
已知1molS完全燃烧生成![]() 放出akJ热量;又知
放出akJ热量;又知![]() ;
;![]() ;则请写出1mol固体S生成气体
;则请写出1mol固体S生成气体![]() 的热化学方程式为 ______
的热化学方程式为 ______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,对于①![]()
![]() 溶液②
溶液②![]() 的HCl溶液③
的HCl溶液③![]() 的NaOH溶液④
的NaOH溶液④![]()
![]() 溶液,下列说法正确的是
溶液,下列说法正确的是![]()
A.①和②分别稀释100倍后的pH:②<①
B.水电离出的![]() :④>③>②>①
:④>③>②>①
C.①和③混合后溶液呈中性: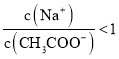
D.①和④混合后溶液呈酸性: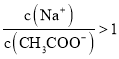
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢能源是一种重要的清洁能源。现有两种可产生H2的化合物甲和乙。将6.00g甲加热至完全分解,只得到一种短周期元素的金属单质和6.72LH2(已折算成标准状况),甲与水反应也能产生H2,同时还产生一种白色沉淀物,该白色沉淀可溶于NaOH溶液。化合物乙在催化剂存在下可分解得到H2和另一种单质气体丙,丙在标准状态下的密度为1.25g/L。请回答下列问题:
(1)甲的化学式是__________;乙的电子式是__________。
(2)甲与水反应的化学方程式是__________。
(3)气体丙与金属镁反应的产物是__________(用化学式表示)。
(4)乙在加热条件下与CuO反应可生成Cu和气体丙,写出该反应的化学方程式__________。有人提出产物Cu中可能还含有Cu2O,请设计实验方案验证之__________(已知Cu2O+2H+=Cu+Cu2++H2O)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以N2和H2为反应物,盐酸酸化的NH4Cl溶液为电解质的原电池,工作原理如图所示,下列说法不正确的是

A.b电极为负极
B.反应过程中,溶液中的H+向a电极移动
C.a电极的电极反应式为N2+6e-+8H+=2NH![]()
D.放电一段时间之后,溶液的酸性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】尿素[CO(NH2)2]是首个由无机物人工合成的有机物。工业上合成尿素的反应如下:2NH3(g)+CO2(g) ![]() CO(NH2)2(l)+H2O(l) △H<0。回答下列问题:
CO(NH2)2(l)+H2O(l) △H<0。回答下列问题:
(1)已知工业上合成尿素分两步进行,相关反应如下:
反应Ⅰ:2NH3(g)+CO2(g) ![]() NH2COONH4(s) △H1<0
NH2COONH4(s) △H1<0
反应Ⅱ:NH2COONH4(s) ![]() CO(NH2)2(l)+H2O(l) △H2>0
CO(NH2)2(l)+H2O(l) △H2>0
①△H=________________(用△H1、△H2表示)
②下列示意图中[a表示2NH3(g)+CO2(g),b表示NH2COONH4(s),c表示CO(NH2)2(l)+H2O(l)],能正确表示尿素合成过程中能量变化曲线是(填编号)______。
(2)某实验小组模拟工业上合成尿素的条件,在恒定温度下,将氨气和二氧化碳按2:1的物质的量之比充入一体积为10L的密闭容器中(假设容器体积不变,生成物的体积忽略不计),经20min达到平衡,各物质浓度的变化曲线如下图所示。

①可以判断该化合反应已经达到化学平衡的是_________。(填编号)
A.![]() B.密闭容器中总压强不变
B.密闭容器中总压强不变
C.密闭容器中氨气的体积分数不变 D.密闭容器中混合气体的密度不变
②在上述条件下,从反应开始至20min时,二氧化碳的平均反应速率为____________。
③该反应的平衡常数表达式K=____________。
(3)人工肾脏可采用间接电化学方法除去代谢产物中的尿素,原理如下图所示。

阳极室中发生的反应依次为_____________________、____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚苯乙烯(PS)和聚对苯二甲酸乙二醇酯(PET)材料具有高韧性、质轻、耐酸碱等性能,在生产生活中应用广泛。这两种聚合物可按下图路线合成,请回答下列问题:

(1)A的分子式为______,其核磁共振氢谱有______组(个)吸收峰。
(2)含有苯环的B的同分异构体有______种。
(3)D为苯乙烯,其结构简式为______,官能团为______。
(4)F的名称为______,由E→G的反应类型是______(填“缩聚”或“加聚”)反应。
(5)已知:
![]()
![]()
![]()
![]()
![]()
写出由BrCH2CH2Br制备HOOC-CH2CH2-COOH的合成路线:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值。下列说法正确的是
A.标准状况下,0.1mol Cl2溶于水,转移的电子数目为0.1NA
B.标准状况下,2.24L NO和2.24L O2混合后气体分子数为0.15 NA
C.0.1mol Na2O2与足量的潮湿的二氧化碳反应转移的电子数为0.1NA
D.加热条件下,1mol Fe投入足量的浓硫酸中,生成NA个SO2分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com