
【题目】关于下列各图的叙述,正确的是( )

A.甲表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6Kjmol﹣1
B.乙表示恒温恒容条件下发生的可逆反应2NO2![]() N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
C.丙表示A、B两物质的溶解度随温度变化情况,将A、B饱和溶液分别由t1℃升温至t2℃时,溶质的质量分数B>A
D.丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB溶液
【答案】D
【解析】
试题分析:A、在101kPa时,1mol可燃物完全燃烧生成稳定氧化物时所放出的热量,使用燃烧热时要注意两个关键点:①反应物用量:可燃物为1mol;②产物要求:充分燃烧成稳定氧化物(如H→H2O),本题生成的水为气体,不是燃烧热,A错误;B、乙表示恒温恒容条件下发生的可逆反应2NO2![]() N2O4(g)中,各物质的浓度与其消耗速率之间的关系,横坐标向右表示浓度增大,纵坐标向上表示物质消耗速率快,如果达到平衡状态,则二者消耗速率之比等于化学计量数之比即应该等于2:1,B错误;C、将A、B饱和溶液分别由T1℃升温至T2℃时两溶液中溶质和溶剂的量都不会改变,而二者T1℃溶解度相同,即浓度相同,所以T2℃时溶质的质量分数相等,C错误;D、常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化可知酸性HA大于HB,NaB溶液中B水解程度大,产生OH-浓度大,pH大,故D正确;答案选DS。
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,横坐标向右表示浓度增大,纵坐标向上表示物质消耗速率快,如果达到平衡状态,则二者消耗速率之比等于化学计量数之比即应该等于2:1,B错误;C、将A、B饱和溶液分别由T1℃升温至T2℃时两溶液中溶质和溶剂的量都不会改变,而二者T1℃溶解度相同,即浓度相同,所以T2℃时溶质的质量分数相等,C错误;D、常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化可知酸性HA大于HB,NaB溶液中B水解程度大,产生OH-浓度大,pH大,故D正确;答案选DS。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列关于苯的说法中,不正确的是( )
A.苯是一种重要的化工原料
B.苯有毒且易挥发,是一种无色无味的液体
C.溴在苯中的溶解度大且与水互不相溶,可以用苯萃取溴水中的溴
D.苯是一种易挥发、易燃的物质,放置苯的仓库要禁止烟火
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.核外电子排布完全相同的两种粒子,其化学性质一定相同
B.难失电子的原子,一定具有强氧化性
C.离子化合物和共价化合物中都可能含有非极性键
D.共价化合物溶水电离过程中,共价键未被破坏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中科大陈乾旺教授等人发明![]() 合成金刚石的新方法,化学原理为:①
合成金刚石的新方法,化学原理为:①![]() (未配平)该方法比1955年人工首次制得金刚石的旧方法容易得多。②
(未配平)该方法比1955年人工首次制得金刚石的旧方法容易得多。②![]() 。以下表述正确的是( )
。以下表述正确的是( )
A. 反应①中既有旧化学键的断裂又有新化学键的形成
B. 新方法利用的是物理变化,旧方法利用的是化学变化
C. 在反应①中每生成![]() 金刚石需要消耗
金刚石需要消耗![]() 金属钠
金属钠
D. 反应①和反应②中所得的金刚石都是还原产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某密闭容器中充入1 mol CO和2 mol H2O(g),发生反应:CO+H2O(g)![]() CO2+H2。当反应达到平衡时,CO的体积分数为x。若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是( )
CO2+H2。当反应达到平衡时,CO的体积分数为x。若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是( )
A. 0.5 mol CO+2 mol H2O(g)+1 mol CO2+1 mol H2
B. 1 mol CO+1 mol H2O(g)+1 mol CO2+1 mol H2
C. 0.5 mol CO+1.5 mol H2O(g)+0.4 mol CO2+0.4 mol H2
D. 0.5 mol CO+1.5 mol H2O(g)+0.5 mol CO2+0.5 mol H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下HF的电离常数Ka=3.3×10-4 ,CaF2的溶度积常数Ksp=1.46×10-10。在该温度下取浓度为0.31 mol·L-1的HF与浓度为0.002 mol·L-1的CaCl2溶液等体积混合。下列说法正确的是
A. 该温度下,0.31 mol·L-1的HF溶液的pH=2
B. 升高温度或增大浓度,HF的电离平衡常数都将增大
C. 两溶液混合不会产生沉淀
D. 向饱和的CaF2溶液中加入少量CaCl2固体后,溶度积常数Ksp一定比之前减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.已知某纯碱试样中含有杂质NaCl,为了确定试样中纯碱的质量分数,可测定其在化学反应中生成CO2的质量,实验装置如下(铁架台及夹持仪器均已省略)。
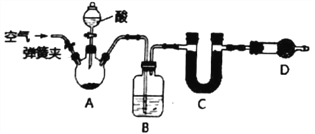
完成下列填空:
(1)B装置中的试剂是_____________,作用是_____________________________。
(2)D装置的作用是___________________________________。
II.测定试样中纯碱质量分数的某次实验步骤如下:①将10.000g纯碱试样放入A中 ②称量C(U型管+碱石灰,下同),质量为l05.160g ③使用分液漏斗滴加足量的酸,使充分反应 ④打开A的弹簧夹,缓缓鼓入一定量的空气 ⑤再次称量C ⑥重复步骤④和⑤,最后得到C的质量为109.l66g。
(3)步骤③中,滴加的酸最好选用________。
a、浓硝酸 b、稀盐酸 c、浓硫酸 d、稀硫酸
当看到____________________现象时即可进行第④步操作。
(4)步骤⑥的目的是_______________________________________________。
(5)由实验数据可知,试样中纯碱的质量分数为_________________(保留3位小数)。
(6)甲同学用上述装置测定某试样中纯碱的质量分数,结果偏高,请帮助他找出造成实验误差的原因。_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一个1L的密闭容器中,加入2molA和1molB进行如下反应:2A(g)+2B(g)![]() 3C(?)+D(?)。反应一段时间后达到平衡,测得生成0.6molC,且反应前后压强之比为15∶11(相同温度下测量),则下列说法正确的是( )
3C(?)+D(?)。反应一段时间后达到平衡,测得生成0.6molC,且反应前后压强之比为15∶11(相同温度下测量),则下列说法正确的是( )
A. 该反应的化学平衡常数K约为0.043
B. 增加C的物质的量,B的平衡转化率不变
C. 增大该体系的压强,平衡正向移动,化学平衡常数增大
D. A的平衡转化率是40%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com