
【题目】写出下列反应的热化学方程式:
(1)N2(g)与H2(g)反应生成1molNH3(g),放出46.1kJ热量。_________________
(2)1molC2H5OH(l)完全燃烧生成CO2(g)和H2O(l),放出1366.8kJ热量。_________________
(3)2molC2H2(g)在O2(g)中完全燃烧生成CO2和H2O(l),放出2598.8kJ热量。_________________。
(4)1molC(石墨)与适量的H2O(g)反应生成CO(g)和H2(g),吸收131.3kJ热量_________________。
(5)2gH2和足量的O2充分燃烧生成液态水,放出热量为285.8kJ,则H2和O2燃烧的热化学方程式:_________________
【答案】N2(g)+3H2(g)=2NH3(g) △H=92.2kJ/mol C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) △H=1366.8kJ/mol 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H=2598.8kJ/mol C(石墨)+H2O(g)=CO(g)+H2(g) △H=131.3kJ/mol H2(g)+![]() O2(g)=H2O(l) △H=285.8kJ/mol
O2(g)=H2O(l) △H=285.8kJ/mol
【解析】
书写热化学方程式时要注明各种反应物、生成物的存在状态,并把与反应的物质的多少对应反应热写在方程式后面,标出反应热的符号、数值及单位。
(1)N2(g)与H2(g)反应生成1mol NH3(g),放出46.1kJ热量,则 N2(g)与H2(g)反应生成2mol NH3(g),放出92.2kJ热量,该反应的热化学方程式为N2(g)+3H2(g)![]() 2NH3(g) △H=92.2kJ/mol;
2NH3(g) △H=92.2kJ/mol;
(2)1mol C2H5OH(l)完全燃烧生成CO2(g)和H2O(l),放出1366.8kJ热量,则该反应的热化学方程式为:C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) △H=1366.8kJ/mol;
(3)2molC2H2(g)在O2(g)中完全燃烧生成CO2和H2O(l),放出2598.8kJ热量,则其相应的热化学方程式为:2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H=-2598.8kJ/mol。
(4)1molC(石墨)与适量的H2O(g)反应生成CO(g)和H2(g),吸收131.3kJ热量,其相应的热化学方程式为:C(石墨)+H2O(g)=CO(g)+H2(g) △H=+131.3kJ/mol 。
(5)2g H2和足量的O2充分燃烧生成液态水,放出热量为285.8kJ,则H2和O2燃烧的热化学方程式:H2(g)+![]() O2(g)=H2O(l) △H=285.8kJ/mol。
O2(g)=H2O(l) △H=285.8kJ/mol。


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
【题目】H2和I2在一定条件下能发生反应:H2(g)+I2(g)2HI(g)△H=-akJ/mol,已知: (a、b、c均大于零)
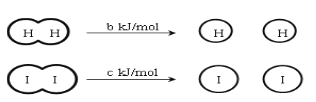
下列说法正确的是
A.碰撞理论认为,反应速率的大小与单位时间内反应物微粒间碰撞次数成正比,只要有足够的能量就可以发生有效碰撞
B.断开2molHI分子中的化学键所需能量约为(c+b+a)kJ
C.相同条件下,1molH2(g)和1molI2(g)总能量小于2molHI(g)的总能量
D.向密闭容器中加入2molH2(g)和2molI2(g),充分反应后放出的热量为2akJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1g氢气在氧气中燃烧生成液态水,放出142.9kJ的热量,表示该反应的热化学方程式是()
A.H2(g)+![]() O2 (g)=H2O(l) △H=-285.8kJ·mol-1
O2 (g)=H2O(l) △H=-285.8kJ·mol-1
B.H2(g)+![]() O2 (g)=H2O(g) △H=-285.8kJ·mol-1
O2 (g)=H2O(g) △H=-285.8kJ·mol-1
C.2H2(g)+O2(g)=2H2O(l) △H=-285.8kJ
D.H2+![]() O2=H2O △H=-285.8kJ·mol-1
O2=H2O △H=-285.8kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业生产中常常需要对混合气体中的NOx含量进行测定,其中一种方法的操作如下:①将200L气样通入酸化的H2O2溶液中,使NOx完全被氧化为NO![]() ,加水稀释至100.00mL;②微微加热,除去过量的H2O2;③量取20.00mL该溶液,加入20mL8.000×10-2mol·L-1FeSO4溶液(过量),充分反应;④用5.000×10-3mol·L-1K2Cr2O7溶液滴定剩余的Fe2+,终点时消耗20.00mL。
,加水稀释至100.00mL;②微微加热,除去过量的H2O2;③量取20.00mL该溶液,加入20mL8.000×10-2mol·L-1FeSO4溶液(过量),充分反应;④用5.000×10-3mol·L-1K2Cr2O7溶液滴定剩余的Fe2+,终点时消耗20.00mL。
(1)能使气样中的NOx更好地被H2O2溶液氧化的操作是___。
(2)NO被H2O2氧化为NO3-的离子方程式是___。
(3)若缺少步骤②,对混合气体中NOx含量的测定结果将___(填“偏大”或“偏小”或“无影响”)。
(4)滴定过程中发生下列反应(未配平):
Fe2++NO![]() +H+——NO↑+Fe3++H2O
+H+——NO↑+Fe3++H2O
Cr2O![]() +Fe2++H+——Cr3++Fe3++H2O
+Fe2++H+——Cr3++Fe3++H2O
则气样中NOx折合成NO2的含量为___mg·m-3。(保留4位有效数字)(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有三种金属单质A、B、C,其中A的焰色反应为黄色,B、C是常见金属。三种金属单质A、B、C与气体甲、乙、丙及物质D、E、F、G、H之间发生如下转化关系(图中有些反应的产物和反应的条件没有标出)。
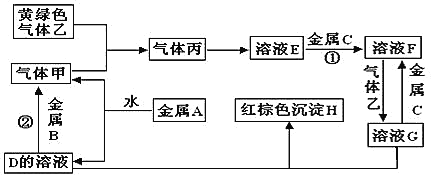
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A__________; G___________。
(2) 写出反应①的化学方程式:__________;写出反应②的离子方程式:_________。
(3)说出黄绿色气体乙的一种用途__________________。
(4)区别E、F两种溶液最简单的方法是______,实验室检验G中所含的金属离子时,常在G的溶液中加入_____溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是分离混合物时常用的仪器,可以进行的混合物分离操作分别是()
![]()
A.蒸馏、过滤、萃取、蒸发B.蒸馏、蒸发、萃取、过滤
C.萃取、过滤、蒸馏、蒸发D.过滤、蒸发、萃取、蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的数值,下列说法正确的是( )
A. 将含1molFeCl3的溶液滴入沸水中,所制得的Fe(OH)3胶体粒子为NA
B. 常温常压下,1 mol甲基(-CH3)所含电子数为10NA
C. 常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA
D. 标准状况下,11.2L三氯甲烷中含有的极性共价键数目为1.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】JohnB.Goodenough等三位科学家因为在锂离子电池研究领域的突出贡献获得2019年诺贝尔化学奖。碳酸锂是一种常见的锂离子电池原料,一种以锂辉石为原料制取碳酸锂的工艺如图:(锂辉石:LiAl(SiO3)2,也表示为Li2O·Al2O3·4SiO2,还含微量的钠、钙、镁等元素)
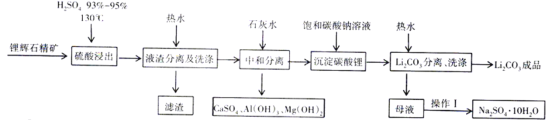
[查阅资料]:Li2CO3为无色单斜晶系结晶体,熔点618℃,溶于硫酸,微溶于水,在冷水中的溶解度比热水中大。
(1)在“硫酸浸出”流程,将硫酸加热到130℃的目的是___________________________。
(2)工业上高温煅烧FePO4、Li2CO3和草酸晶体(H2C2O4·2H2O)的混合物制取电池材料磷酸亚铁锂(LiFePO4),反应的化学方程式为__________________________________。
(3)LiFePO4含有Fe、Li两种金属元素,它们的焰色反应的颜色分别是___________
A.黄色、紫红色B.绿色、黄色C.无焰色反应、紫红色D.黄色、无焰色反应
(4)在“Li2CO3分离、洗涤”流程,用热水洗涤的原因是___________________________。
(5)某浓差电池的原理示意如图所示,可用该电池从浓缩海水中提取LiCl溶液。
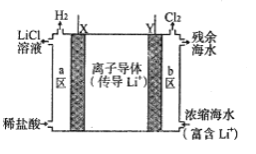
电池中的Y电极为________(填“正极”或“负极”或“阳极”或“阴极”)。X极的电极反应方程式为:________________________________________________。Y极每生成标况下22.4LCl2,有_________molLi+经过离子导体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2O俗名为“笑气”,也是一种温室气体。结合所学知识,回答下列问题:
(1)锌与极稀硝酸反应可生成N2O,该反应的化学方程式为___________,其中作氧化剂的硝酸与参与反应的硝酸的物质的量之比为___________。
(2)已知几种物质的相对能量如下:
物质 | N2O(g) | CO(g) | N2(g) | CO2(g) |
相对能量/kJmol-1 | 475.5 | 283.0 | 393.5 | 0 |
①N2O(g)和CO(g)反应生成N2(g)和CO2(g)的热化学方程式为____________。
②若其他条件不变,加入高效催化剂,该反应的焓变将_______(填“增大”、“减小”或“不变”)。
(3)碘蒸气能催化N2O的分解,反应历程(步骤)如下:
i.I2(g)2I(g)
ii.I(g)+N2O(g)=N2(g)+IO(g)
iii.2IO(g)+2N2O(g)=2N2(g)+2O2(g)+I2(g)
实验表明,在反应过程c(I)始终大于c(IO),由此推测,反应速率ii_________iii(填“>”、“<”或“=”)。
(4)一定温度下,向恒容密闭容器中充入2 mol N2O(g)和3 mol NO(g),发生反应:N2O(g)+NO(g)N2(g)+NO2(g) △H。测得N2体积分数与温度、时间的关系如图所示。
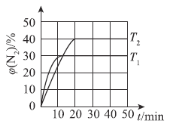
①△H___________0(填“>”、“<”或“=”)。
②下列情况表明该反应达到平衡状态的是___________(填字母)。
A.混合气体的密度不再改变 B.相对分子质量不再改变
C.NO和NO2的消耗速率相等 D.N2O的体积分数不再改变
③T1时,该反应的平衡常数K=___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com