
【题目】A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族。B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物。
请回答下列问题:
(1)C、D、E三种原子对应的离子半径由大到小的顺序是___________(填具体离子符号);由A、B、C三种元素按 4:2:3组成的化合物所含的化学键类型属于_____________________。
(2)用某种废弃的金属易拉罐与 A、C、D组成的化合物溶液反应,该反应的离子方程式为:______________________________________________________。
(3)A、C两元素的单质与熔融K2CO3,组成的燃料电池,其负极反应式为_______________________,
用该电池电解1L1mol/LNaCl溶液,当消耗标准状况下1.12LA2时, NaCl溶液的pH=_____(假设电解过程中溶液的体积不变) 。
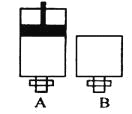
(4)可逆反应2EC2(气)+C2(气)![]() 2EC3(气)在两个密闭容器中进行, A容器中有一个可上下移动的活塞, B 容器可保持恒容 (如图所示) ,若在 A 、B 中分别充入lmolC2和2molEC2,使V (A ) =V( B ) ,在相同温度下反应,则:达平衡所需时间:t(A )______t ( B )(填>、<、二,或:无法确定,下同)。平衡时 EC2的转化率:a( A )_______ a( B )。
2EC3(气)在两个密闭容器中进行, A容器中有一个可上下移动的活塞, B 容器可保持恒容 (如图所示) ,若在 A 、B 中分别充入lmolC2和2molEC2,使V (A ) =V( B ) ,在相同温度下反应,则:达平衡所需时间:t(A )______t ( B )(填>、<、二,或:无法确定,下同)。平衡时 EC2的转化率:a( A )_______ a( B )。
(5)欲比较C和E两元素的非金属性相对强弱,可采取的措施有_____________(填“序号”)。
a.比较这两种元素的气态氢化物的沸点
b.比较这两种元素的单质在常温下的状态
c.比较这两种元素的气态氢化物的稳定性
d.比较这两种元素的单质与氢气化合的难易
【答案】S2->O2->Na+ 共价键和离子键 2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑ H2-2e-+CO32-=CO2+H2O 13 < > c、d
【解析】
A和C可形成两种常见的液态化合物,因此A是氢元素,C是氧元素,两种液态化合物分别是水和双氧水。C、E同主族,E的原子序数大于C,所以在短周期中E是S元素。A和D最外层电子数相同,且D的原子序数大于氧元素的,小于S元素的,所以D应该是钠元素。B、C和E在周期表中相邻,B、C的最外层电子数之和等于D的原子核外电子数,且B的原子序数小于氧元素的,因此B是氮元素。
(1)同主族自上而下离子半径逐渐增大,则微粒半径是S2->O2-。核外电子排布相同的微粒,其微粒半径随原子序数的增大而减小,所以微粒半径是O2->Na+。所以C、D、E三种原子对应的离子半径由大到小的顺序是S2->O2->Na+;由H、N、O三种元素按4:2:3组成的化合物是NH4NO3,所含的化学键类型是离子键和共价键。
(2)A、C、D组成的化合物溶液是氢氧化钠溶液,易拉罐中含有金属铝,和氢氧化钠溶液反应的离子方程式是2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑。
(3)原电池中负极失去电子,发生氧化反应。所以氢气在负极通入。由于电解质是熔融的碳酸钾,所以负极电极反应式是H2-2e-+CO32-=CO2+H2O。消耗氢气的物质的量是1.12L÷22.4L/mol=0.05mol,反应中失去0.05mol×2=0.1mol电子。则根据电子得失守恒可知,生成氢氧化钠的物质的量是0.1mol,因此氢氧化钠溶液的浓度是0.1mol÷1L=0.1mol/L,所以pH=13。
(4)根据装置图可知,A容器保持恒温恒压,B保持恒温恒容。由于反应2SO2+O2![]() 2SO3是体积减小的可逆反应,在反应过程中压强是减小的。这说明在反应过程中A中的压强大于B中的压强,压强大反应速率快,到达平衡的时间少,所以达平衡所需时间:t(A ) < t ( B );压强大有利于平衡向正反应方向移动,所以反应物的转化率高,即平衡时 EC2的转化率:a( A ) >a( B )。
2SO3是体积减小的可逆反应,在反应过程中压强是减小的。这说明在反应过程中A中的压强大于B中的压强,压强大反应速率快,到达平衡的时间少,所以达平衡所需时间:t(A ) < t ( B );压强大有利于平衡向正反应方向移动,所以反应物的转化率高,即平衡时 EC2的转化率:a( A ) >a( B )。
(5)a、非金属性强弱与气态氢化物的沸点没有关系,a不正确;
b、非金属强弱与非金属单质的状态没有关系,b不正确;
c、非金属性越强,气态氢化物的稳定性越强,所以选项c正确;d、非金属性越强,越容易与氢气化合,所以选项d可以说明,答案选cd。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某温度时,在2L密闭容器中X、Y、Z三种气态物质的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据
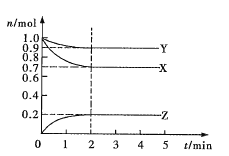
(1)该反应的化学方程式为______________。
(2)反应开始至2min,用Z表示的平均反应速率为_________。
(3)下列叙述能说明上述反应达到化学平衡状态的是________(填序号)
A.混合气体的总物质的量不随时间的变化而变化
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗![]() X,同时生成
X,同时生成![]() Z
Z
D.混合气体的总质量不随时间的变化而变化
E.混合气体的密度不再发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向a L密闭容器中加入1mol X气体和2mol Y气体,发生如下反应:X(g)+2Y(g)![]() 2Z(g),此反应达到平衡的标志是( )
2Z(g),此反应达到平衡的标志是( )
A. 容器内密度不随时间变化B. 容器内各物质的浓度不随时间变化
C. 容器内X、Y、Z的浓度之比为1∶2∶2D. 单位时间消耗0.1mol X同时生成0.2mol Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.有一学生在实验室测某溶液的pH,实验时,他先用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测。
(1)该学生的操作___(填“正确”或“错误”),其理由是___________;
(2)该操作是否一定有误差?______________________;
(3)若用此方法分别测定c(OH-)相等的氢氧化钠溶液和氨水的pH,误差较大的是____,原因是___;
(4)只从下列试剂中选择实验所需的试剂,你能否区分0.1mol·L-1硫酸溶液和0.01mol·L-1硫酸溶液?____,简述操作过程:____________________________。
试剂:A.紫色石蕊溶液 B.酚酞溶液 C.甲基橙溶液 D.蒸馏水 E.氯化钡溶液 F.pH试纸
Ⅱ.pH=2的A、B两种酸溶液各1mL,分别加水稀释到1000mL,其pH与溶液体积的关系如图所示。
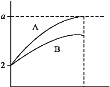
回答下列问题:
(1)若a=5,则A为___酸,B为___酸(填“强”或“弱”),若再稀释100倍,则A的pH___7(填“<”“>”或“=”)。
(2)若A、B都是弱酸,则a的范围是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用脱脂棉包住约0.2gNa2O2粉末,置于石棉网上,往脱脂棉上滴水(如图1),可观察到脱脂棉剧烈燃烧起来。
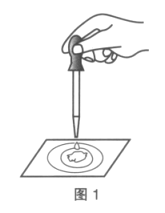
(1)由实验现象所得出的有关Na2O2和H2O反应的结论如下,请补充完整:
a.有___生成;b.反应放热;
Na2O2与水反应的化学方程式是__。
(2)某研究性学习小组拟用图2装置进行实验,以证明上述结论。
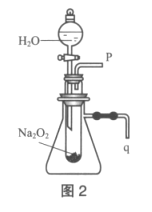
①用以验证结论a的实验方法:打开分液漏斗活塞,__。
②用以验证结论b的实验方法:反应前将q导管口连接一橡胶管浸入盛有水的水槽中,滴入水后,观察到___,证明反应是放热的。
(3)实验(2)往试管中加水至固体完全溶解且不再有气泡生成后,取出试管,向试管中滴入酚酞溶液,发现溶液变红,振荡后,红色褪去。针对褪色现象,查阅资料发现原因之一是反应后溶液中有H2O2,使酚酞氧化漂白。同学们向反应后溶液中加入FeSO4溶液,可观察到__色沉淀生成,该反应的离子方程式是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,2﹣二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度是2.18g/cm3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验中可以用如图所示装置制备1,2﹣二溴乙烷。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液。试管d中装有浓溴水(表面覆盖少量水)。
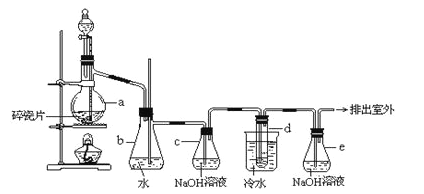
请填写下列空白:
(1)烧瓶a中发生的是乙醇的脱水反应,即消去反应,反应温度是170℃,并且该反应要求温度迅速升高到170℃,否则容易发生副反应.请写出乙醇发生消去反应的方程式 。
(2)写出制备1,2﹣二溴乙烷的化学方程式: 。
(3)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞.请回答发生堵塞时瓶b中的现象: 。
(4)容器c中NaOH溶液的作用是: 。
(5)判断该制备反应已经结束的最简单方法是___________________________;
(6)若产物中有少量副产物乙醚,可用__________的方法除去;
(7)反应过程中应用冷水冷却装置d,其主要目的是___________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C、N、S是重要的非金属元素,按要求回答下列问题:
(1)烟道气中含有的CO和SO2是重要的污染物,可在催化剂作用下将它们转化为S(s)和CO2,此反应的热化学方程式为______________________________________________________。
已知:CO(g)+1/2O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
S(s)+O2(g)=SO2(g) ΔH=-296.0 kJ·mol-1。
(2)向甲、乙两个均为1 L的密闭容器中,分别充入5 mol SO2和3 mol O2,发生反应:2SO2(g)+
O2(g)![]() 2SO3(g) ΔH<0。甲容器在温度为T1的条件下反应,达到平衡时SO3的物质的量为4.5 mol;乙容器在温度为T2的条件下反应,达到平衡时SO3的物质的量为4.6 mol。则T1___T2(填“>”、“<”),甲容器中反应的平衡常数K=_____________________。
2SO3(g) ΔH<0。甲容器在温度为T1的条件下反应,达到平衡时SO3的物质的量为4.5 mol;乙容器在温度为T2的条件下反应,达到平衡时SO3的物质的量为4.6 mol。则T1___T2(填“>”、“<”),甲容器中反应的平衡常数K=_____________________。
(3)如图所示,A是恒容的密闭容器,B是一个体积可变的充气气囊。保持恒温,关闭K2,分别将1 mol N2和3 mol H2通过K1、K3充入A、B中,发生的反应为:N2(g)+3H2(g) ![]() 2NH3(g),起始时A、B的体积相同均为a L。
2NH3(g),起始时A、B的体积相同均为a L。

①下列示意图既能说明A容器中反应达到平衡状态,又能说明B容器中反应达到平衡状态的是______。

②容器A中反应到达平衡时所需时间t s,达到平衡后容器的压强变为原来的5/6,则平均反应速率υ(H2)=___________________________。
(4)将0.1 mol氨气分别通入1 L pH=1的盐酸、硫酸和醋酸溶液中,完全反应后三溶液中NH4+离子浓度分别为c1、c2、c3,则三者浓度大小的关系为____________(用“c1、c2、c3和>、<、=”表示)。已知醋酸铵溶液呈中性,常温下CH3COOH的Ka=1×10-5 mol·L-1,求该温度下NH4Cl的水解常数K h 为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作对应的现象不符合事实的是
选项 | 实验操作 | 现象 |
A | 向盛有 | 溶液逐渐变为黄色,滴加KSCN后溶液变血红色 |
B | 向盛有 | 溶液逐渐褪色,静置后观察到溶液有分层现象 |
C | 向 | 先产生白色沉淀,后沉淀消失 |
D | 向盛有 | 有刺激性气味气体产生,溶液变浑浊 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硫是大气的主要污染物之一。催化还原SO2不仅可以消除SO2的污染,还可以得到工业原料S。燃煤烟气中硫的回收反应为:2CO(g)+SO2(g) ![]() 2CO2(g)+S(l) △H。
2CO2(g)+S(l) △H。
(1)已知:2CO(g)+O2(g)===2CO2(g) △H1=-566.0kJ·mol-1
S(l)+O2(g)===SO2(g) △H2=-296.8 kJ·mol-1
则硫的回收反应的△H=___________ kJ·mol-1。
(2)其他条件相同、催化剂不同时,硫的回收反应中SO2的转化率随反应温度的变化如图所示。260℃时,___________(填“La2O3”、“NiO”或“TiO2”)的催化效率最高。La2O3和NiO作催化剂均可能使SO2的转化率达到很高,不考虑价格因素,选择La2O3的主要优点是___________。

(3)一定条件下,若在恒压密闭容器中发生硫的回收反应,SO2的平衡转化率与温度、压强的关系如图所示,则P1、P2、P3、P4由大到小的顺序为___________;某温度下,若在恒容密闭容器中,初始时c(CO)=2 a mol·L-1,c(SO2)= a mol·L-1,SO2的平衡转化率为80%,则该温度下反应的化学平衡常数为___________。
(4)某实验小组为探究烟气流速、温度对该反应的影响,用La2O3作催化剂,分别在两种不同烟气流量、不同温度下进行实验。实验结果显示:在260℃时,SO2的转化率随烟气流量增大而减小,其原因是___________;在380℃时,SO2的转化率随烟气流量增大而增大,其原因是___________。
(5)工业上常用Na2SO3溶液吸收烟气中的SO2,将烟气通入1.0 mol·L-1的N2SO3溶液,当溶液pH约为6时,吸收SO2的能力显著下降此时溶液中c(HSO3-)c︰(SO32-)=___________。(已知H2SO3的Ka1=1.5×10-2、Ka2=1.0×10-7)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com