
| 2×9+2-8 |
| 2 |
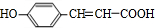 ,E的结构简式为
,E的结构简式为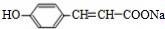 ,E与氢氧化钠反应生成F为
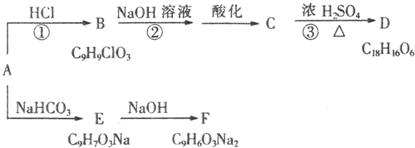
,E与氢氧化钠反应生成F为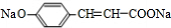 .A与HCl发生加成反应生成B,B发生水解反应、酸化得到C,C转化得到D,D分子中除含2个苯环外还含有1个六元环,结合D的分子式可知,应是2分子C发生酯化反应反应生成环酯,则C中侧链中羧基与-OH连接在同一碳原子上,故B为
.A与HCl发生加成反应生成B,B发生水解反应、酸化得到C,C转化得到D,D分子中除含2个苯环外还含有1个六元环,结合D的分子式可知,应是2分子C发生酯化反应反应生成环酯,则C中侧链中羧基与-OH连接在同一碳原子上,故B为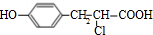 ,则C为
,则C为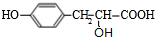 ,D为
,D为 ,据此解答.
,据此解答.| 2×9+2-8 |
| 2 |
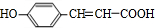 ,E的结构简式为
,E的结构简式为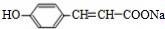 ,E与氢氧化钠反应生成F为
,E与氢氧化钠反应生成F为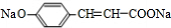 .A与HCl发生加成反应生成B,B发生水解反应、酸化得到C,C转化得到D,D分子中除含2个苯环外还含有1个六元环,结合D的分子式可知,应是2分子C发生酯化反应反应生成环酯,则C中侧链中羧基与-OH连接在同一碳原子上,故B为
.A与HCl发生加成反应生成B,B发生水解反应、酸化得到C,C转化得到D,D分子中除含2个苯环外还含有1个六元环,结合D的分子式可知,应是2分子C发生酯化反应反应生成环酯,则C中侧链中羧基与-OH连接在同一碳原子上,故B为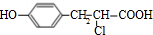 ,则C为
,则C为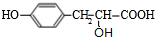 ,D为
,D为 ,
,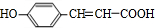 ,所含官能团的名称是:羧基、羟基、碳碳双键,故答案为:羧基、羟基、碳碳双键;
,所含官能团的名称是:羧基、羟基、碳碳双键,故答案为:羧基、羟基、碳碳双键;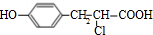 ,D的结构简式为:
,D的结构简式为: ,
,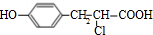 ;
; ;
;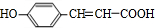 +NaHCO3→
+NaHCO3→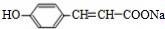 +H2O+CO2↑,
+H2O+CO2↑,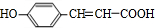 +NaHCO3→
+NaHCO3→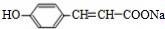 +H2O+CO2↑;
+H2O+CO2↑;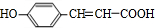 )的同分异构体符合下列条件:
)的同分异构体符合下列条件:

 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源: 题型:
| O | 2- 3 |
| O | 2- 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
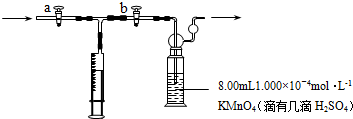
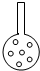
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||

查看答案和解析>>
科目:高中化学 来源: 题型:
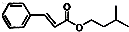 )的路线如下:
)的路线如下: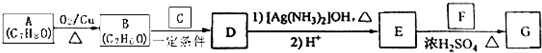
| 一定条件 |
 +H2O.
+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:
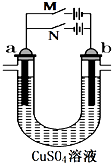 第一阶段:合上M断开N,a极上产224mL(标准状况,下同)气体,b极上有金属析出;
第一阶段:合上M断开N,a极上产224mL(标准状况,下同)气体,b极上有金属析出;查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用加热法可除去Na2CO3中的NaHCO3 |
| B、Na2CO3的热稳定性大于NaHCO3 |
| C、可用石灰水区分Na2CO3与NaHCO3溶液 |
| D、小苏打可中和胃酸、热纯碱可除去油污 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com