
【题目】直接甲醇燃料电池(DMFC)有望取代传统电池,它主要由阴极极板、阳极极板和膜电极构成,其中膜电极包括质子膜、催化剂层和气体扩散层(如图).下列关于DMFC工作原理的叙述正确的是( ) 
A.通入O2的电极反应式为:O2+4e﹣+2H2O═4OH﹣
B.电池内部H+由正极渗过交换膜向负极移动
C.甲醇在正极发生反应,电流经过外电路流向负极
D.注入CH3OH的电极反应式为:CH3OH+H2O﹣6e﹣═CO2+6H+
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列实验操作均要用玻璃棒,其中玻璃棒的作用及其目的相同的是( )
①过滤 ②蒸发 ③溶解 ④向容量瓶转移液体.
A. ①和② B. ①和③ C. ①和④ D. ③和④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铍原子比铝原子少1个电子层,最外层电子数也比铝原子少1,在周期表中铍和铝的位置关系存在有“对角线”关系的元素性质存在相似性。下列关于铍的判断不正确的是( )
A. Be能在空气中燃烧 B. BeO熔点较低
C. BeCl2是共价化合物 D. Be(OH)2具有两性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种元素都是短周期元素。A元素的离子具有黄色的焰色反应。B元素的离子结构和Ne具有相同的电子层排布;5.8gB的氢氧化物恰好能与100mL2mol/L盐酸完全反应;B原子核中质子数和中子数相等。H2在C单质中燃烧产生苍白色火焰。D元素原子的电子层结构里,最外层电子数是次外层电子数的3倍。根据上述条件,回答:
(1)元素C位于第_______周期________族,它的最高价氧化物的化学式为____________。
(2)B是________元素。
(3)写出B 和 D组成化合物的形成过程______________________________________。
(4)A与D形成稳定的化合物的化学式为______________,将该化合物加入含有酚酞的水作用实验现象是____________________________________________________________。
(5)C元素的单质有毒,可用A 的最高价氧化物对应的水化物的溶液吸收,其离子方程式为_________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种短周期元素,对应原子的质子数之和为16,对应单质爱常温下均为气体。三种单质两两化合,可发生如图转化:已知1个B分子中含有的Z原子数比C分子中少1,B、C分子中均含有10个电子。下列说法正确的是
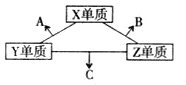
A. 原子半径:X>Y>Z
B. 非金属性:Y>X>Z
C. 沸点:A>B>C
D. B与C分子中所含的化学键完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①⑩种元素,填写下列空白(涉及具体元素对应化学符号表示):

(1)在这些元素中,化学性质最不活泼的是_______(填元素符号)元素⑩在周期表中的位置______。形成化合物最多的元素______(填序号)
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是______,碱性最强的化合物的电子式是:______。
(3)用电子式表示元素④与⑥的化合物的形成过程:_________________.
(4)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是________。
(5)元素③的氢化物的结构式为_____;该氢化物在一定条件下可以生成另一种③的氢化物和③的单质。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一容积不变的密闭容器中充入0.1mol/LCO2和0.1mol/LCH4 , 在一定条件下发生反应:CH4(g)+CO2(g)2CO(g)+2H2(g).测得平衡时CH4的转化率与温度、压强的关系如图.下列有关说法正确的是( ) 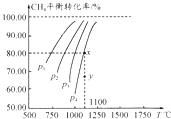
A.上述反应的△H<0
B.压强P1>P2>P3>P4
C.1100℃时该反应的平衡常数约为1.64
D.压强为P4时,y点的v正<v逆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铝合金中含有元素铝、铁、铜、硅。为了测定该合金中铝的含量,设计了如下实验,请回答有关问题:
(1)称取样品ag(精确到0.1g),称量时通常使用的主要仪器的名称是_______。
(2)将样品溶解于足量的稀盐酸,过滤并洗涤滤渣。溶解、过滤用到的玻璃仪器有_______。(3)向滤液中加过量的氢氧化钠溶液,过滤并洗涤滤渣。
(4)向步骤(3)的滤液中通入足量的二氧化碳气体,过滤并洗涤滤渣,生成沉淀的离子方程式是___________。
(5)将步骤(4)的滤渣烘干并灼烧至恒重、冷却后称重,其质量为bg。有关反应的化学方程式是_______________,原样品中铝的质量分数是_______。(用含a、b的代数式表示)
(6)若步骤(5)的滤渣灼烧不充分,则实验结果______(填“偏高”、“偏低”或“不影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有浓度均为0.1molL﹣1的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸氢铵、⑦氨水,请回答下列问题:
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号) .
(2)④、⑤、⑥、⑦四种溶液中NH4+浓度由大到小的顺序是(填序号) .
(3)已知t℃时,Kw=1×10﹣12 , 则t℃(填“>”“<”或“=”)25℃;在t℃时溶液呈中性的pH= .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com