
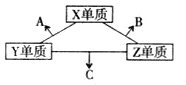
����Ŀ��X��Y��Z���ֶ�����Ԫ�أ���Ӧԭ�ӵ�������֮��Ϊ16����Ӧ���ʰ������¾�Ϊ���塣���ֵ����������ϣ��ɷ�����ͼת������֪1��B�����к��е�Zԭ������C��������1��B��C�����о�����10�����ӡ�����˵����ȷ����
A. ԭ�Ӱ뾶��X>Y>Z
B. �ǽ����ԣ�Y>X>Z
C. �е㣺A>B>C
D. B��C�����������Ļ�ѧ����ȫ��ͬ
���𰸡�D
�����������������Ϣ�����Եó�X��Y��Z�ֱ�ΪO��N��H��A��B��C�ֱ�ΪNO��H2O��NH3��ͬһ���ڣ������ң�ԭ�Ӱ뾶��С��ͬһ���壬���ϵ��£�ԭ�Ӱ뾶�����ɴ˿��Եó���ԭ�Ӱ뾶N>O>H������ͬһ��������������Ԫ�صķǽ�������ǿ��Ԫ�صķǽ�����O>N>H��B����ˮ���������Ӽ����������ˮ���Ӽ�����ϴ��������ֻ�����е�H2O>NH3>NO��C����H2O��NH3�����ж�ֻ���м��Թ��ۼ���D��ȷ����ȷѡ��D��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25�� ��101kpaʱ�����顢��Ȳ�ͱ�ϩ��ɵĻ����32mL�����������ϲ���ȫȼ�գ���ȥˮ�������ָ���ԭ�����¶Ⱥ�ѹǿ��������������С��72mL��ԭ���������Ȳ���������Ϊ�� ��
A.12.5%
B.25%
C.50%
D.75%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���ԭ�ӽṹ��Ԫ�����ʵ�˵����ȷ����(����)
A. ijԪ�ص�������Ϊ�����ԭ��������ֵ��ȡ��
B. ��A�����Ԫ����ͬ�����н�������ǿ��Ԫ��
C. ͬ��Ԫ�ص�ԭ�Ӿ�����ͬ����������������
D. ��A��Ԫ�ص������ӻ�ԭ��Խǿ��������������Ӧˮ���������Խǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼװ�ÿ�����֤�ǽ����Եı仯���ɡ�

��1������A������Ϊ_____________________�������D��������______________________��
��2��ʵ����������ҩƷNa2S��KMnO4��Ũ���ᡢMnO2����ѡ�����ҩƷ���ʵ����֤�ȵķǽ����Դ�����װ��A��B��C����װҩƷ�ֱ�Ϊ________��_______��_______��װ��C�е�ʵ������Ϊ�е���ɫ�������ɣ����ӷ���ʽΪ__________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D���ֶ�����Ԫ����ԭ�Ӱ뾶��С��A��C�ĺ˵����֮��Ϊ3: 4���ֱܷ���A��B��C�γɵ���������ȵķ���X��Y��Z������������ȷ����
A. X��Y��Z���ȶ�������
B. X��Y��Z���ֻ�������۷е�����
C. A��B��C��Dֻ���γ�5�ֵ���
D. ��A��B��C��D����Ԫ����ɵĻ������кܶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ֱ�Ӽ״�ȼ�ϵ�أ�DMFC������ȡ����ͳ��أ�����Ҫ���������塢���������Ĥ�缫���ɣ�����Ĥ�缫��������Ĥ���������������ɢ�㣨��ͼ�������й���DMFC����ԭ����������ȷ���ǣ� �� 
A.ͨ��O2�ĵ缫��ӦʽΪ��O2+4e��+2H2O�T4OH��
B.����ڲ�H+��������������Ĥ���ƶ�
C.�״�������������Ӧ�������������·����
D.ע��CH3OH�ĵ缫��ӦʽΪ��CH3OH+H2O��6e���TCO2+6H+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵����ȷ���ǣ� ��
A.5.6 g ����������ˮ������Ӧ��ʧȥ�ĵ�����Ϊ0.3NA
B.��ȡ��״����22.4 L Cl2 �� ��ת�Ƶĵ�����Ϊ2NA
C.2.3 g Na�ڿ�������ȫȼ�գ�ʧȥ�ĵ�����Ϊ0.1NA
D.��״����3.36 L HF�ﺬ�е�ԭ������Ϊ0.3NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����( )
A. ���ݷ�ɢ�����ӵĴ�С,�ɽ���ɢϵ��Ϊ��Һ���������Һ
B. �����з�ɢ�����ӵ�ֱ��ͨ������100nm
C. ��Һһ���Ǿ�һ���ȶ��Ļ����
D. ����ڵ�����ˮ����μ�������FeCl3������Һ, ���������Һ��ʺ��ɫ,���Ƶ�Fe(OH)3����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����ʢ��ϡ������ձ��з����õ������ӵĵ缫X��Y,���·�е���������ͼ��ʾ�����й��ڸ�װ�õ�˵����ȷ����

A. ���·�ĵ�������ΪX![]() ���·
���·![]() Y
Y
B. �����缫�ֱ�ΪFe��̼������X Ϊ̼����Y ΪFe
C. X ���Ϸ������ǻ�ԭ��Ӧ��Y ���Ϸ�������������Ӧ
D. �����缫���ǽ����������ǵĻ�����˳��ΪX>Y
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com