
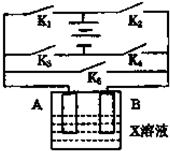
 某课外活动小组准备用如图所示的装置进行实验,现有甲、乙、丙三位同学分别选择了如下电极材料和电解质溶液
某课外活动小组准备用如图所示的装置进行实验,现有甲、乙、丙三位同学分别选择了如下电极材料和电解质溶液| A电极 | B电极 | X溶液 | |
| 甲 | Cu | Zn | H2SO4 |
| 乙 | Pt | Pt | CuCl2 |
| 丙 | Fe | Cu | ? |
| A、甲同学在实验中将开关K5闭合,Zn电极上产生气泡 |
| B、乙同学打算闭合K3、K4做电解CuCl2溶液的实验 |
| C、乙同学用淀粉碘化钾试纸检验电解产生的氯气 |
| D、丙同学准备在Fe上镀Cu,选择了一种铜盐来配制电镀液,闭合的开关的组合是K2、K3 |
| ||


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、0.1mol?L-1稀硫酸100mL中含有硫酸根离子个数为0.1NA |
| B、常温常压下,氧气和臭氧的混合物16g中含有NA个氧原子 |
| C、7.8 g Na2O2含有的阴离子数目为0.2 NA |
| D、NO2与足量的水完全反应,若有1molNO生成,则转移电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加热时生成的气体在标况下3.36L |
| B、NaHCO3和Na2CO3混合物质量为17.9g |
| C、加热时若用浓硫酸吸收气体则浓硫酸增重3.3g |
| D、HCl溶液的浓度为0.6mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C(石墨,s)═C(金钢石,s)△H>0,说明石墨比金刚石稳定 | ||
B、NH3+H3O+?N
| ||
| C、2HCl+CaCO3═CaCl2+CO2↑+H2O,说明盐酸是强酸 | ||
| D、CH3COO-+H2O?CH3COOH+OH-,说明CH3COOH是弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、100mL 1mol/L NaHCO3溶液含有0.1NA个HCO3- |
| B、常温常压下,1mol氦气含有2NA个原子 |
| C、7.8g Na2S和Na2O2的混合物中含有的阴离子数等于0.1NA |
| D、加热条件下,1molCl2与足量Fe粉充分反应,转移的电子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、FeBr2溶液与Cl2 |
| B、Ba(OH)2溶液与H2SO4溶液 |
| C、盐酸与Na2CO3溶液 |
| D、Ca(HCO3)2溶液与NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学键 | C-H | C=C | C-C | H-H |
| 键能(kJ/mol) | 615.3 | 414.4 | 347.4 | 435.3 |
| A、已知则可以计算CH3-CH3(g)→CH2=CH2(g)+H2(g)△H=+125.6 kJ/mol |
| B、容量瓶、量筒和滴定管上都要标明使用温度,容量瓶无“0”刻度,量筒、滴定管都有“0”刻度;使用时量筒和滴定管水洗后还需润洗,但容量瓶水洗后不用润洗 |
| C、氯化镁溶液与氨水反应:Mg2++2NH3?H2O=Mg(OH)2↓+2NH4+ |
| D、使石蕊呈紫色的溶液中,下列离子可以大量共存:Na+、AlO2-、NO3-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:1 | B、4:1 |
| C、5:1 | D、1:4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com