
【题目】SO2、NOx的含量是衡量大气污染的一个重要指标。工业上常采用催化还原法或吸收法处理SO2,催化还原SO2不仅可以消除SO2污染,而且可以得到有价值的中单质硫,采取氨水吸收NOx的方法去除NOx的污染,生成硝酸按。
(1)已知CH4和S的燃烧热分别为a kJ/mol和bkJ/mol。在复合组分催化剂作用下,甲烷可使SO2转化为S,同时生成CO2和液态水,该反应的热化方程式为___________。
(2)用H2还原SO2生成S的反应分两步完成,如图甲所示,该过程中相关物质的物质的量浓度随时间的变化关系如图乙所示:
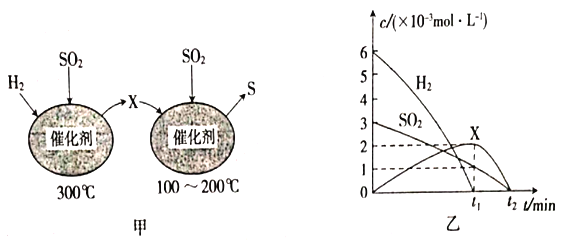
分析可知X为____________(写化学式);0-t1时间段的反应温度为____________,0-t1时间段用SO2表示的化学反应速率为______________________。
(3)焦炭催化还原SO2生成S2的化学方程式为 2C(s)+2SO2 (g)=S2(g)+2CO2(g)。在恒容容器中,浓度为1mol/L的SO2与足量焦炭反应,SO2的转化率随温度的变化如图丙所示。700℃时该反应的平衡常数为____________。
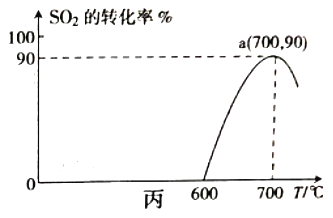
(4)25℃时,用1mol/L的Na2SO3溶液吸收SO2,当溶液的pH=7时,溶液中各离子浓度的大小关系为_____________。(已知:H2SO3的电离常数Ka1=1.3×10-2,Ka2=6.2×10-8)
(5)利用双离子交换膜电解法可以从含硝酸铵的工业废水里生产硝酸和氨。阳极室得到的物质是______,写出阳极反应方程式_______________________;阴极室得到的物质是_____________,写出阴极反应及获得相应物质的方程式______________、________________。
【答案】CH4(g)+2SO2(g)=CO2(g)+2S(s)+2H2O(l) △H=+(2b-a)kJ/mol H2S 300℃ ![]() mol/(L·min) 36.45 c(Na+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-) 硝酸 2H2O-4e-=4H++O2↑或4OH--4e-=2H2O+O2↑ 氨 2H2O+2e-=H2↑+2OH-或 2H++2e-=H2↑ NH4++OH-=NH3+H2O或 NH4++OH-=NH3·H2O
mol/(L·min) 36.45 c(Na+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-) 硝酸 2H2O-4e-=4H++O2↑或4OH--4e-=2H2O+O2↑ 氨 2H2O+2e-=H2↑+2OH-或 2H++2e-=H2↑ NH4++OH-=NH3+H2O或 NH4++OH-=NH3·H2O
【解析】
(1)先写出CH4和S的燃烧热的热化学方程式,然后将两个热化学方程式叠加,可得需求的热化学方程式。
(2)根据氧化还原反应原理分析;0-t1时间段,X的浓度达到最大,应是图1左侧反应,方程式为3H2+SO2=H2S+2H2O,温度为300℃;根据v=![]() 计算;
计算;
(3)a点为700℃时SO2的转化率为90%,根据平衡常数的含义计算。
(4)当吸收液呈中性时溶质为亚硫酸钠和亚硫酸氢钠,根据电离水解能力和电荷守恒分析;
(5)从含硝酸铵的工业废水里生产硝酸和氨,则为硝酸铵中NO3-与H+结合生成硝酸,NH4+与OH-结合生成氨,实际在电解水,阳极为水电离产生的OH-失去电子发生氧化反应,阴极为水电离产生的H+得到电子发生还原反应,据此可得。
(1)已知CH4和S的燃烧热分别为akJ/mol和bkJ/mol,可知热化学方程式:
①CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=akJ/mol
②S(s)+O2(g)=SO2(g) △H=bkJ/mol
由盖斯定律①-②×2可得CH4(g)+2SO2(g)=CO2(g)+2S(s)+2H2O(l) △H=+(2b-a)kJ/mol;
(2)图1右图SO2→S,S元素的化合价降低,根据氧化还原反应特点,化合价有升高,必然有降低,因此推出X为H2S;0-t1时间段,X的浓度达到最大,应是图1左侧反应,方程式为3H2+SO2=H2S+2H2O,温度为300℃;根据化学反应速率的表达式,v(SO2)=![]() =
=![]() mol/(L·min);
mol/(L·min);
(3)由图可知,a点为700℃时SO2的转化率为90%,则根据方程式2C(s)+2SO2(g)=S2(g)+2CO2(g)中物质的转化关系可知平衡时各种物质的浓度c(SO2)=0.1mol/L,c(S2)=0.45mol/L,c(CO2)=0.9mol/L,所以700℃时该反应的平衡常数K=![]() =36.45 mol/L;
=36.45 mol/L;
(4)已知:H2SO3的电离常数Ka1=1.![]() =
=![]() ,亚硫酸氢钠的电离常数为6.2×10-8,小于亚硫酸钠的水解平衡常数,当吸收液呈中性时溶质为亚硫酸钠和亚硫酸氢钠,电离与水解的程度相等,呈中性时,亚硫酸氢根离子浓度大于亚硫酸根离子浓度,溶液中氢离子浓度等于氢氧根离子浓度,溶液中阴阳离子所带电荷相等,则c(Na+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-);
,亚硫酸氢钠的电离常数为6.2×10-8,小于亚硫酸钠的水解平衡常数,当吸收液呈中性时溶质为亚硫酸钠和亚硫酸氢钠,电离与水解的程度相等,呈中性时,亚硫酸氢根离子浓度大于亚硫酸根离子浓度,溶液中氢离子浓度等于氢氧根离子浓度,溶液中阴阳离子所带电荷相等,则c(Na+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-);
(5)从含NH4NO3的工业废水里生产硝酸和氨,则为硝酸铵中NO3-与H+结合生成硝酸,NH4+与OH-结合生成氨,实际在电解水,则阳极为水失去电子发生氧化反应为:2H2O-4e-=4H++O2↑或4OH--4e-=2H2O+O2↑,NO3-与H+结合生成硝酸;阴极为水得到电子发生还原反应:2H2O+2e-=H2↑+2OH-或 2H++2e-=H2↑,NH4+与OH-结合生成氨。


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:
【题目】在由Cu片、Zn片和200 mL稀H2SO4组成的原电池中,当Cu片上放出2.24 L(标准状况下)H2时,H2SO4恰好用完。问:
(1)此时在导线上有________摩尔电子通过?
(2)Zn片溶解的质量是________?
(3)原稀H2SO4的物质的量浓度是________?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z在元素周期表中的相对位置如表所示,这四种元素的原子最外层电子数之和为21。下列说法不正确的是
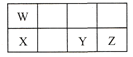
A.原子半径大小:X > Y > Z
B.W、Y两种元素都能与氧元素形成化合物WO2、YO2
C.氧化物对应水化物的酸性: Z > Y > W
D.Y能形成H2Y、H2YO4的化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图示为一种天然产物,具有一定的除草功效。下列有关该化合物的说法错误的是( )

A.分子中含有三种含氧官能团
B.1 mol该化合物最多能与6molNaOH反应
C.既可以发生取代反应,又能够发生加成反应
D.既能与FeC13发生显色反应,也能和Na2CO3反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分)化合物X是一种香料,可采用乙烯与甲苯为主要原料,按下列路线合成:
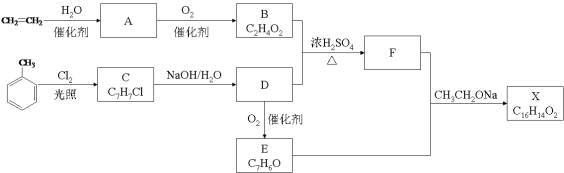
已知:RX![]() ROH;RCHO+CH3COOR’
ROH;RCHO+CH3COOR’![]() RCH=CHCOOR’
RCH=CHCOOR’
请回答:
(1)E中官能团的名称是 。
(2)B+D→F的化学方程式 。
(3)X的结构简式 。
(4)对于化合物X,下列说法正确的是 。
A.能发生水解反应 B.不与浓硝酸发生取代反应
C.能使Br2/CCl4溶液褪色 D.能发生银镜反应
(5)下列化合物中属于F的同分异构体的是 。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将有机物完全燃烧,生成CO2和H2O,将12 g该有机物完全燃烧产物通过浓硫酸,浓硫酸增重14.4 g,再通过碱石灰,又增重26.4 g。则该有机物的分子式为( )
A. C4H10 B. C2H6O
C. C3H8O D. C2H4O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乳酸乙酯是白酒的香气成分之一,广泛用于食品香精。适量添加可增加白酒中酯的浓度,增加白酒的香气,是清香型白酒的主体香成份。乳酸乙酯发生如图变化(已知烃A是衡量一个国家石油化工发展的重要标志)
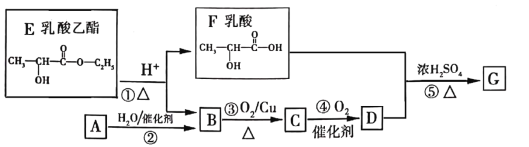
(1)A分子的空间构型是_______。
(2)D的化学式是_______________,F中含氧官能团的名称是______________。
(3)②的化学方程式是___________,⑤的反应类型是_________
(4)1mol乳酸与足量NaOH反应,消耗NaOH__________mol。
(5)绿色化学的核心内容之一是“原子经济性”,即原子的理论利用率为100%。下列转化符号绿色化学要求的是__________(填序号)。
a.乙醇制取乙醛 b.甲烷制备CH3Cl c.2CH3CHO+O2![]() 2CH3COOH
2CH3COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上,向500~600℃的铁屑中通入氯气生产无水氯化铁。现用如图所示的装置模拟上述过程进行实验。

(1)写出仪器的名称:a_______________,b___________________。
(2)A中反应的化学方程式为____________。
(3)装置B中加入的试剂是_____________。
(4)已知:向热铁屑中通入氯化氢气体可以生产无水氯化亚铁。为防止有杂质FeCl2生成,可在装置______和 ________(填字母)间增加一个盛有________的洗气瓶。
(5)装置D的作用是___________________。为防止水蒸气影响无水氯化铁的制取,请你提出一个对装置D的改进方案:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硒是人体必需的微量元素,右图是硒在周期表中的信息,关于硒元素的说法错误的是

A. 位于第四周期
B. 质量数为34
C. 原子最外层有6个电子
D. 相对原子质量为78.96
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com