
【题目】有某硫酸和硝酸的混合溶液20 mL,其中含硫酸的浓度为2 mol·L-1,含硝酸的浓度为1 mol·L-1,现向其中加入0.96 g铜粉,充分反应后(假设只生成NO气体),最多可收集到标准状况下的气体的体积为( )
A. 224 mLB. 168 mL
C. 112 mLD. 89.6 mL
【答案】A
【解析】
铜与稀硝酸反应的实质为8H++3Cu+2NO3-=3Cu2++2NO↑+4H2O,在溶液中每3molCu与8molH+完全反应生成2molNO,题中0.96g铜粉的物质的量为![]() =0.015mol,混合溶液中H+的物质的量为2mol·L-1×0.02L×2+1mol·L-1×0.02L=0.10mol,NO3-的物质的量为1mol·L-1×0.02L=0.02mol,根据离子方程式的关系:8H++3Cu+2NO3-=3Cu2++2NO↑+4H2O,显然氢离子过量,铜完全反应,生成的NO气体由铜的物质的量计算得出,生成NO的物质的量为0.01mol,在标准状况下的体积为0.01mol×22.4L/mol=0.224L=224mL。
=0.015mol,混合溶液中H+的物质的量为2mol·L-1×0.02L×2+1mol·L-1×0.02L=0.10mol,NO3-的物质的量为1mol·L-1×0.02L=0.02mol,根据离子方程式的关系:8H++3Cu+2NO3-=3Cu2++2NO↑+4H2O,显然氢离子过量,铜完全反应,生成的NO气体由铜的物质的量计算得出,生成NO的物质的量为0.01mol,在标准状况下的体积为0.01mol×22.4L/mol=0.224L=224mL。
故选A。


科目:高中化学 来源: 题型:
【题目】已知苯乙烯的结构为![]() ,有关该物质的下列说法正确的是( )
,有关该物质的下列说法正确的是( )
A. 与液溴混合后加入铁粉可发生取代反应
B. 该物质能使溴水和酸性高锰酸钾溶液褪色,褪色原理完全相同
C. 苯乙烯分子的所有原子不可能在同一平面上
D. 除去乙苯中混有的苯乙烯可以通入等量氢气反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列关于充电电池、干电池的叙述合理的是___________。
①干电池可以实现化学能向电能的转化和电能向化学能的转化
②锌锰干电池长时间连续使用时内装糊状物可能流出腐蚀电器
③充电电池可以无限制地反复放电、充电
④充电是使放电时的氧化还原反应逆向进行
(2)铅蓄电池中,正极材料为PbO2,负极材料为Pb,放电时其负极反应式为_____________。
(3)原电池在NaOH溶液介质中,铝为负极,其负极反应式为_______________。
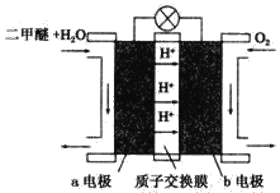
(4)如图为绿色电源“二甲醚(CH3OCH3)燃料电池”的工作原理示意图。b电极是_____极,请写出负极的电极反应方程式:___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中通入物质的量浓度均0.1mol·L-1的CH4与CO2,在一定条件下发生反应:CO2(g)+CH4(g)![]() 2CO(g)+2H2(g),测得CH4的平衡转化率与温度及压强的关系如图5,下列有关说法正确的是( )
2CO(g)+2H2(g),测得CH4的平衡转化率与温度及压强的关系如图5,下列有关说法正确的是( )

A. 上述反应的△H>0 B. 压强P1>P2>P3>P4
C. 1100℃该反应的平衡常数为64 D. 压强为P4时,在Y点:v(正)<v(逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A可以通过不同化学反应分别制得B、C和D三种物质,结构简式如图所示:

(1)A的分子式是____;B中的含氧官能团名称是____。
(2)A→B的反应类型是____;A~D中互为同分异构体的是_____(填代号)。
(3)D在酸性条件下水解的化学方程式是____。
(4)检验B中醛基的方法____。
(5)符合下列条件的A的同分异构体有____种。
①官能团种类不变且与苯环直接相连;②苯环上只有三个取代基。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是
A. 无色透明的溶液中:Fe3+、Mg2+、SCN–、Cl–
B.  =1×1012的溶液中:K+、Na +、CO32-、NO3-
=1×1012的溶液中:K+、Na +、CO32-、NO3-
C. c(Fe2+) =1mol·L1的溶液中:K+、NH4+、MnO4-、SO42-
D. 能使甲基橙变红的溶液中:Na+、NH4+、SO42-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图图装置测定中和热的实验步骤如下:
| ①用量筒量取50 mL 0.50mol·L-l盐酸倒入小烧杯中,测出盐酸温度; ②用另一量筒量取50mL 0.55mol/L NaOH溶液,并用另一温度计测出其温度; ③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液的最高温度。 |
回答下列问题:
(1)倒入NaOH溶液的正确操作是______________。
A.沿玻璃缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(2)使硫酸与NaOH溶液混合均匀的正确操作是______________。
A.用温度计小心搅拌 B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯 D.用套在温度计上的环形玻璃棒轻轻地搅动
(3)做了三次实验,每次取溶液各50 mL,并将实验数据记录如下:

已知盐酸、NaOH溶液的密度与水相同,中和后生成的溶液的比热容c=4. 2×10-3kJ/(g·℃),则该反应的中和热△H=____________________________。
(4)若用50 mL 0.55 mol·L-1的氨水(NH3·H2O)代替NaOH溶液进行上述实验,通过测得的反应热来计算中和热,测得的中和热△H的绝对值会___________(填“偏小”、“偏大”或“不变”)。
(5)若通过实验测定中和热的△H的绝对值常常小于57.3kJ/mol,其原因可能是______________。
A.实验装置保温、隔热效果差
B.测量HCl溶液的温度计用水洗净后才用来测NaOH溶液的温度
C.量取NaOH溶液的体积时仰视读数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作规范且能达到目的的是
目的 | 操作 | |
A. | 取20.00 mL盐酸 | 在50 mL酸式滴定管中装入盐酸,调整初始读数为30.00 mL后,将剩余盐酸放入锥形瓶 |
B. | 测定醋酸钠溶液pH | 用玻璃棒蘸取溶液,点在湿润的pH试纸上 |
C. | 清洗碘升华实验所用试管 | 先用酒精清洗,再用水清洗 |
D. | 配制浓度为0.010 | 称取KMnO4固体0.158 g,放入100 mL容量瓶中,加水溶解并稀释至刻度 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+2B(g)==C(g)的反应过程中能量变化如下图所示。下列相关说法正确的是 ( )

A. 正反应活化能大于逆反应活化能
B. 曲线b表示使用催化剂后的能量变化
C. 由图可知该反应的焓变△H=+91kJ/mol
D. 反应中将气体A换为固体反应,其他条件不变,反应放出热量大于91kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com