
【题目】两气体A和B的摩尔质量之比为2:1,则它们在同温、同压、同体积时的分子个数比应为( )
A.1:1
B.1:2
C.2:1
D.4:1
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源: 题型:
【题目】已知有关热化学方程式为:
① 4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) △H=-905kJ/mol;
4NO(g)+6H2O(g) △H=-905kJ/mol;
② 3H2(g)+N2(g)![]() 2NH3(g) △H=-92.4kJ/mol;
2NH3(g) △H=-92.4kJ/mol;
③ 2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ/mol;
④ N2(g)+O2(g)=2NO(g) △H=QkJ/mol;
(1)Q=___________。
(2)向某密闭容器中充入amolNH3、bmolO2后,测得反应体系中某种量值X与压强P、温度T之间的变化如图1所示,图2表示温度为T2时,当容器为1L恒容密闭容器时,容器中NH3的平衡转化率与反应开始时两种反应物的投料之比(用M表示)的关系。
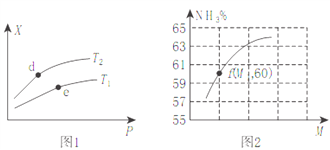
①若X表示NH3的百分含量,则T2_____T1(填>、<、无法确定);d、e两点的正反应的平衡常数K(d)_____K(e)。
②X还可以表示_____________。
a.混合气体的平均摩尔质量 b.NO的产率 c.△H值
③M=__________(用含a、b的式子表示,后同),若f点M=1.25,则此时O2的转化率为_________
(3)有科学家电解原理获得高产率的合成氨,则阴极上的电极反应式为(已知电解质能传递H+)_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两烧杯中各盛有100 mL 3 mol·L-1的盐酸和NaOH溶液,向两烧杯中分别加入等质量的铝粉,反应结束后,测得生成的气体体积比为V(甲)∶V(乙)=1:2,则加入铝粉的质量为( )
A. 1.8 g B. 2.7 g C. 3.6 g D. 5.4 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量NaOH溶液的烧杯中通入CO2气体,然后向该溶液中逐滴加入1mol/L盐酸.所加入盐酸溶液的体积与产生二氧化碳气体体积(标准状况)的关系如图所示:
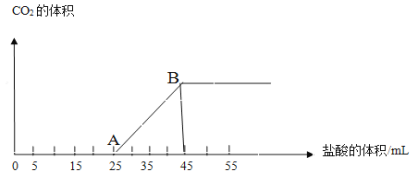
(1)写出OA段所发生反应的离子方程式_____。
(2)当加入35mL盐酸时,所产生的二氧化碳的体积(标准状况)是_____mL。
(3)通入CO2气体后,溶液中所含溶质及溶质的物质的量之比为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯异氰尿酸是一种极强的氧化剂和氯化剂,利用氰尿酸(图1)与次氯酸在一定pH下反应可制备三氯异氰尿酸(图2),若原料完全反应生成三氯异氰尿酸,下列说法正确的是
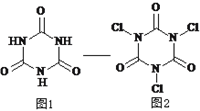
A. 氰尿酸的分子式为C6N3O3H3
B. HClO的电子式为 ![]()
C. 该转化过程有机物发生还原反应
D. 氰尿酸和次氯酸反应的物质的量之比为2 : 3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ. 分类法对研究化学物质和化学反应有重要的意义,请完成下列问题。今有七种物质: ①铝线 ②熔化的KNO3 ③氯气 ④NaCl晶体 ⑤液态氯化氢 ⑥石灰水 ⑦乙醇,其中能导电的物质是_______,属于电解质的是____,属于非电解质的是__。写出⑥与足量碳酸氢钠溶液反应的离子方程式:_____。
Ⅱ.实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL。根据这两种溶液的配制情况回答下列问题。
(1)在下图所示仪器中,配制上述溶液肯定不需要的是_________(填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是 _____________________________。
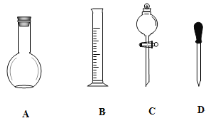
(2)在容量瓶的使用方法中,下列操作不正确的是____________
A.使用容量瓶前检验是否漏水
B.容量瓶用水洗净后,再用待配溶液洗涤
C.配制溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。
D.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
(3)根据计算用托盘天平称取NaOH固体的质量为_______g。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度______0.1mol/L(填“大于”“小于”或“等于”)。
(4)若用18.4mol/L的浓硫酸进行配制,所需该浓硫酸的体积为____________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有H+、NH4+、Mg2+、Al3+、CO32-、SO42-中的几种。
①若加入锌粒,最终产生无色无味的气体;
②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示,则下列说法正确的是( )
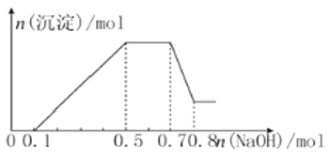
A. 溶液中的阳离子只有H+、Mg2+、Al3+
B. 溶液中n(NH4+)=0.2 mol
C. 溶液中一定不含CO32-,可能含有SO42-
D. n(H+)∶n(Al3+)∶n(Mg2+)=1∶1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。
(1).用双线桥法分析上述反应(只需标出电子得失的方向和数目)__________。
(2).上述反应中氧化剂是__________,氧化产物是__________。
(3).上述反应中氧化剂与还原剂的物质的量之比为__________。
(4).若反应中转移了0.6 mol电子,产生的气体在标准状况下的体积是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表达式中正确的是( )
A. 向氯化钙溶液中通入CO2:CaCl2+CO2+H2O=CaCO3↓+2HCl
B. 铁跟盐酸反应:Fe+2HCl=FeCl2+H2↑
C. NaHCO3溶液的电离方程式:NaHCO3=Na++H+ +CO32-
D. 向沸水中滴加 FeCl3 溶液制备Fe(OH)3 胶体:FeCl3+3H2O=Fe(OH)3↓+3HCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com