
����Ŀ��ij��Һ�п��ܺ���H����NH4+��Mg2����Al3����CO32-��SO42-�еļ��֡�
��������п�������ղ�����ɫ��ζ�����壻
��������NaOH��Һ��������ɫ�������Ҳ����ij����������NaOH�����ʵ���֮��Ĺ�ϵ��ͼ��ʾ,������˵����ȷ���ǣ� ��
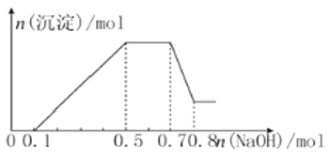
A. ��Һ�е�������ֻ��H����Mg2����Al3��
B. ��Һ��n(NH4+)��0.2 mol
C. ��Һ��һ������CO32-�����ܺ���SO42-
D. n(H��)��n(Al3��)��n(Mg2��)��1��1��1
���𰸡�B
��������
����ͼ���е����յ㣬�������������Ƶ���������Һ�и����ӵ�Ũ�ȡ�
�ɢ�֪��Һ��һ������H����һ��û��CO32-���ɢ�֪��Һ��һ������Mg2����Al3������ͼ���֪��Һ�л�һ������NH4+����n(NH4+)��0.7 mol��0.5 mol��0.2 mol��n(H��)��0.1 mol��n(Al3��)��0.8 mol��0.7 mol��0.1 mol������Al3����Mg2��������0.4 mol OH�������г���Al3������0.3 mol OH��������Mg2������0.1 mol OH��������Mg2����2OH�����ɵ�n(Mg2��)��0.05 mol��
A. ��Һ�е���������H����Mg2����Al3����NH4+����A������
B. ��Һ��n(NH4+)��0.2 mol����B��ȷ��
C. ��Һ��һ������CO32-�����ݵ���غ㣬��Һ�п϶���SO42-����C����
D. n(H��)��n(Al3��)��n(Mg2��)��2��2��1����D����
��ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ����������
(1)6.20 g Na2O �����к� Na+�����ʵ����� _________________��
(2)�������� NH3 �� H2S �У���ԭ�ӵĸ�������______________________��
(3) ����ˮ������Ӧ�Ļ�ѧ����ʽ_______________________________________��
(4) �������Ȼ�����Һ�м��������������Ƶ����ӷ���ʽ________________________��
(5)��ͨ���������������������������ڵ������ǣ�C6H12O6���ṩ������ά�����������ӦʽΪ��C6H12O6+6O26CO2+6H2O+�������÷�Ӧ�еĻ�ԭ����______�����ڸ÷�Ӧ������������������ڱ�״����Ϊ4.48L����Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йؽ������仯�����˵����ȷ����(����)
A.�Ʊ�����ú�����ԭ��֮һ����������������Ӧ
B.��ɫ��Ӧ�ǻ�ѧ�仯�������ò���������ɫ��Ӧʵ��
C.CaO��Na2O��Na2O2������������
D.���ó���ʯ��ˮ������NaHCO3��Na2CO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������A��B��Ħ������֮��Ϊ2��1����������ͬ�¡�ͬѹ��ͬ���ʱ�ķ��Ӹ�����ӦΪ��������
A.1��1
B.1��2
C.2��1
D.4��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ԫ��W��X��Y��Z��ԭ�������������ӡ�A��Ԫ��Y�ĵ��ʡ������£���Ũ��Һ��A�����ۻ�������������������ЩԪ����ɵĶ�Ԫ������ұ�����ɫ���塣�������ʵ�ת����ϵ��ͼ��ʾ������˵����ȷ����
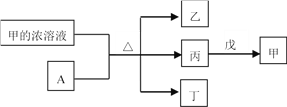
A. ������������Ԫ��������ͬ
B. �����Ӱ뾶��С��X��Y
C. ��̬�⻯��Ļ�ԭ�ԣ�X��Z
D. Y�ļ�������Z�ļ�������ˮ��Һ�пɴ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ���ǣ� ��
A.Ħ���ǹ��ʵ�λ�����߸�����������֮һ
B.���³�ѹ�£�11.2LCO2����������Ϊ0.5NA
C.H2SO4 ��Ħ������Ϊ98 g
D.6.02��1022��H2SO4���ӵ�����Ϊ9.8 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼����Ȼ�����γɻ�������������Ԫ�أ�CO��CO2��̼����������
��1���о��ͽ��������̼������ת�������ǵ�ǰ��ѧ�о���ǰ��������̫���ܵ������£�ȱ��������[Fe0.9O]�ֽܷ�CO2���������ͼ1��ʾ���������Ļ�ѧ����ʽ��______���ڹ�������ÿ����0.1molO2��ת�Ƶ���______mol��

��2���ڴ��������£���������̼��������Ϸ�Ӧ���ɼ��飬��Ŀǰ��ѧ��������̽���Ĵ��������еĶ�����̼�ķ���֮һ��
����֪��
���ۼ� | C=O | H��H | C��H | O��H |
����/(kJmol��1) | 745 | 436 | 413 | 463 |
��CO2(g)+4H2(g)![]() CH4(g)+2H2O(g) ��H=______kJmol��1��
CH4(g)+2H2O(g) ��H=______kJmol��1��
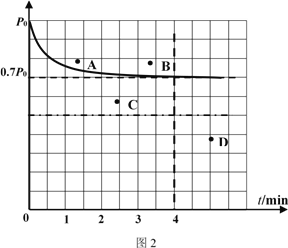
����1L�̶��ݻ����ܱ������м���4.0 mol H2(g)��1.0mol CO2����������������������þ�Ͻ𡢸���T1��ʹ֮��Ӧ������������������ѹǿ����ʱ��ı仯��ͼ2��ʾ����4 minʱ������������ܶ�Ϊ______���¶�T1 �£��÷�Ӧ�Ļ�ѧƽ�ⳣΪ______��������2 L�̶��ݻ����ܱ�������Ͷ�����������ͷ�Ӧ�¶Ⱦ����ֲ��䣬��Ӧ���´ﵽƽ��ʱ��Ӧ��ϵ�ڵ�ѹǿ�ĵ���______������ĸ����
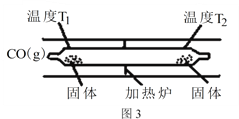
��3����ҵ�ϳ�ԭ����CO�����豸���ܵ�����������Ľ�����������Ӧ�������ʻ���������ʻ������ȷֽⷨ�Ʊ��ߴ�����ԭ�ϣ�Ҳ���л��ϳ��й���һ����̼��ԭ�ϣ�������������Ni(s)+4CO(g)![]() Ni(CO)4(g) ��H��0 Ni(CO)4(g)
Ni(CO)4(g) ��H��0 Ni(CO)4(g)![]() Ni(s)+4CO(g)����ͼ3��ʾ����ʯӢ��չܵ��¶�ΪT1һ�ˣ���������������CO(g)��һ��ʱ������¶�ΪT2��һ�˿ɵõ��������������¶�T1______T2����������������������������������Ӧ��ϵ��ѭ��ʹ�õ�����Ϊ______���ѧʽ����
Ni(s)+4CO(g)����ͼ3��ʾ����ʯӢ��չܵ��¶�ΪT1һ�ˣ���������������CO(g)��һ��ʱ������¶�ΪT2��һ�˿ɵõ��������������¶�T1______T2����������������������������������Ӧ��ϵ��ѭ��ʹ�õ�����Ϊ______���ѧʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪCaF2��H3BO3(��״�ṹ�����ڵ�H3BO3����ͨ��������)������ͭ���־���Ľṹʾ��ͼ����ش��������⣺
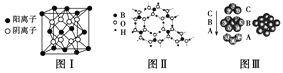
(1)ͼ����ʾ��CaF2��������Ca2������ҵȾ����F����Ϊ________��ͼ����δ��ŵ�ͭԭ���γɾ������Χ����ڵ�ͭԭ����Ϊ________��
(2)ͼ����ʾ�����ʽṹ�������ܲ��Ѵ�8���ӽṹ��ԭ����________��H3BO3��������ԭ�Ӹ����뼫�Լ�������Ϊ________��
(3)����ͭ���кܺõ���չ�ԡ����紫���ԣ��Դ�������Ľ�������________���ۡ�
(4)���־������۵���͵���________���侧�������ۻ�ʱ���˷�����֮��������Ϊ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڲ�ͬ�¶��£�ˮ��Һ��c(H��)��c(OH��)����ͼ��ʾ��ϵ�����������������ӹ���˵������ȷ����( )
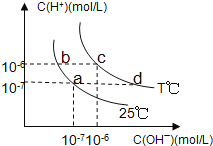
A. a���Ӧ����Һ�д������ڣ�Fe3+��Na+��Cl�D��SO42�D
B. b���Ӧ����Һ�д������ڣ�NH4+��Ba2+��OH�D��I�D
C. c���Ӧ����Һ�д������ڣ�Na+��Ba2+��Cl�D��HCO3�D
D. d���Ӧ����Һ�д������ڣ�Na+��K+��SO32�D��Cl�D
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com