
����Ŀ����ͼΪCaF2��H3BO3(��״�ṹ�����ڵ�H3BO3����ͨ��������)������ͭ���־���Ľṹʾ��ͼ����ش��������⣺
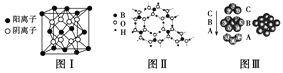
(1)ͼ����ʾ��CaF2��������Ca2������ҵȾ����F����Ϊ________��ͼ����δ��ŵ�ͭԭ���γɾ������Χ����ڵ�ͭԭ����Ϊ________��
(2)ͼ����ʾ�����ʽṹ�������ܲ��Ѵ�8���ӽṹ��ԭ����________��H3BO3��������ԭ�Ӹ����뼫�Լ�������Ϊ________��
(3)����ͭ���кܺõ���չ�ԡ����紫���ԣ��Դ�������Ľ�������________���ۡ�
(4)���־������۵���͵���________���侧�������ۻ�ʱ���˷�����֮��������Ϊ______��
���𰸡� 8 12 O 1��6 ���������� H3BO3 ���Ӽ�������
����������1����ͼ�������ϵ�һ��Ca2���ɿ�������4��F���������Աߵľ���������ҲӦ��4��F������һ��Ca2������8��F����ͭ���������������ܶѻ�����λ��Ϊ12����2��H�������ӣ�B��ͼ������ֻ�γ���������ӦΪ6�����ӣ�ֻ����Ϊ8���ӡ�H3BO3���ڷ��Ӿ��壬һ��B��������O������O����������H������һ��B��Ӧ6�����Լ�����3���������������ۿ��Ժܺõؽ��ͽ����ĵ��紫���Ժ���չ�Ե��������ʡ���4���۵��С���ɣ�ԭ�Ӿ���>���Ӿ���>���Ӿ��壬�������忴�������������H3BO3Ϊ���Ӿ��壬Ӧ��С���ۻ�ʱ�ƻ����Ӽ���������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס������ձ��и�ʢ��100 mL 3 mol��L��1�������NaOH��Һ�������ձ��зֱ��������������ۣ���Ӧ����������ɵ����������ΪV(��)��V(��)��1:2����������۵�����Ϊ( )
A. 1.8 g B. 2.7 g C. 3.6 g D. 5.4 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ�п��ܺ���H����NH4+��Mg2����Al3����CO32-��SO42-�еļ��֡�
��������п�������ղ�����ɫ��ζ�����壻
��������NaOH��Һ��������ɫ�������Ҳ����ij����������NaOH�����ʵ���֮��Ĺ�ϵ��ͼ��ʾ,������˵����ȷ���ǣ� ��
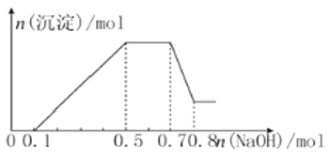
A. ��Һ�е�������ֻ��H����Mg2����Al3��
B. ��Һ��n(NH4+)��0.2 mol
C. ��Һ��һ������CO32-�����ܺ���SO42-
D. n(H��)��n(Al3��)��n(Mg2��)��1��1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ͭ�ڳ������ܱ�ϡ�����ܽ�,�䷴Ӧ�Ļ�ѧ����ʽ����3Cu+8HNO3(ϡ)=3Cu(NO3)2+2NO��+4H2O��
(1).��˫���ŷ�����������Ӧ(ֻ�������ӵ�ʧ�ķ������Ŀ)__________��
(2).������Ӧ����������__________,����������__________��
(3).������Ӧ���������뻹ԭ�������ʵ���֮��Ϊ__________��
(4).����Ӧ��ת����0.6 mol����,�����������ڱ�״���µ������__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������װ�û�����ܴﵽʵ��Ŀ�ĵ���
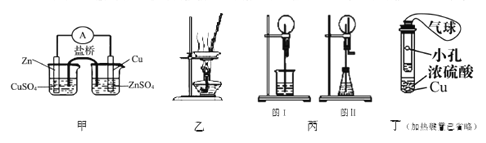
A. ��װ�ù���ͭпԭ���
B. ��ͼ����ʾװ������AlCl3������ҺȻ���������������Ʊ�AlCl3����
C. ��װ����ͼI��ƿ�г����������ձ���ʢװˮ����ͼII����ƿ�У�����������Cu��ϡ���ᣬͼI��ͼII��������Ȫ������ԭ����ͬ
D. ���ö�װ����ȡSO2���������仹ԭ�ԣ�С�Թ��е��Լ���Ϊ����KMnO4��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͭ���仯�����������������й㷺Ӧ��
(1)��ҵ���Ի�ͭ��(CuFeS2)Ϊԭ�ϣ����û�������������ͭ���м���̻ᷢ����Ӧ:2Cu2O+Cu2S![]() 6Cu+SO2���÷�Ӧ����������________����֤��Ӧ������������SO2�ķ�����___________��
6Cu+SO2���÷�Ӧ����������________����֤��Ӧ������������SO2�ķ�����___________��
(2)������ͭ˿����������ϡ�����У��¶ȿ�����50�棬����H2O2����Ӧһ��ʱ������µ�60�棬�ٷ�Ӧһ��ʱ�����Ƶ�����ͭ���¶ȿ�����50�桫60�������ԭ����˼ӿ췴Ӧ�����⣬����___________����CuSO4��Һ�м���һ������Na2SO3��NaCl��Һ���ȣ�����CuC1������д������CuCl�����ӷ���ʽ______________��
(3)��ʽ̼��ͭ���л��������̻���������ϡ�ũҩ�������й㷺��Ӧ�á�ij�����Ի�ͭ��(��Ҫ�ɷ�ΪCu2S��������Fe2O3��SiO2������)Ϊԭ���Ʊ���ʽ̼��ͭ����������:
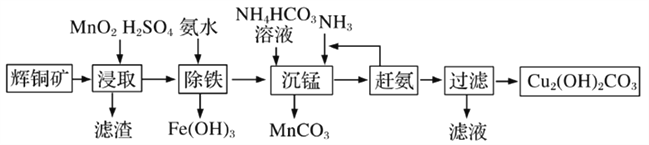
�ٻ�ͭ���ڽ�ȡǰҪ��������飬����ĺô���___________��
�ڽ�ȡ�����еõ�һ�ֵ��ʣ�д����ȡʱ��Ҫ��Ӧ�Ļ�ѧ����ʽ___________��
��д�������̡���Ӧʱ���ӷ���ʽ___________��
�ܡ���������һ����Ӧ��25����У����백ˮ������ҺpHΪ4����Һ��ͭ�������Ũ�Ȳ�����_________mol/L��(��֪Ksp[Cu(OH)2]=2.2��10-20)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵����ȷ����
A. 1mol�Ҵ������к��м��Լ�����ĿΪ8NA
B. 80��ʱ��1LpH=1��������Һ�У���H+����ĿΪ0.2NA
C. Na2O2��2.24LCO2��ȫ��Ӧ��ת�Ƶ��ӵ���ĿΪ0.1NA
D. 1molH2��1molI2���ܱ������г�ַ�Ӧ�����������ĿΪ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б���ʽ����ȷ���ǣ� ��
A. ���Ȼ�����Һ��ͨ��CO2��CaCl2��CO2��H2O��CaCO3����2HCl
B. �������ᷴӦ��Fe��2HCl��FeCl2��H2��
C. NaHCO3��Һ�ĵ��뷽��ʽ��NaHCO3��Na+��H+ ��CO32-
D. ���ˮ�еμ� FeCl3 ��Һ�Ʊ�Fe(OH)3 ���壺FeCl3��3H2O��Fe(OH)3����3HCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Fe��Fe2O3�Ļ���ﹲ13.6g������150mLϡH2SO4���ڱ�״�����ռ���1.12LH2��Fe��Fe2O3����ʣ�ࡣΪ�к�����H2SO4����ʹFeԪ��ȫ��ת��ΪFe(OH)2������������200mL 3mol/L��NaOH��Һ�����H2SO4�����ʵ���Ũ��Ϊ
A. 2.25mol/L B. 2mol/L C. 4mol/L D. 0.6mol/L
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com