
����Ŀ����. ���෨���о���ѧ���ʺͻ�ѧ��Ӧ����Ҫ�����壬������������⡣�����������ʣ� ������ ���ۻ���KNO3 ������ ��NaCl���� ��Һ̬�Ȼ��� ��ʯ��ˮ ���Ҵ��������ܵ����������_______�����ڵ���ʵ���____�����ڷǵ���ʵ���__��д����������̼��������Һ��Ӧ�����ӷ���ʽ��_____��
��.ʵ������Ҫ0.1mol/LNaOH��Һ450mL��0.5mol/L��������Һ500mL��������������Һ����������ش��������⡣
��1������ͼ��ʾ�����У�����������Һ�϶�����Ҫ����_________������ţ�����ͼ�����������⣬����������Һ����Ҫ�IJ��������� _____________________________��
��2��������ƿ��ʹ�÷����У����в�������ȷ����____________
A��ʹ������ƿǰ�����Ƿ�©ˮ
B������ƿ��ˮϴ�������ô�����Һϴ��
C��������Һʱ����������ǹ��壬�ѳƺõĹ�����ֽ��С�ĵ�������ƿ�У�������ˮ���ӽ��̶���1~2cm�����ý�ͷ�ιܼ�����ˮ���̶��ߡ�
D��������Һʱ����������Һ�壬����Ͳȡ�����ò�����������������ƿ�У�������ˮ���̶���1~2cm�����ý�ͷ�ιܼ�����ˮ���̶��ߡ�
E���Ǻ�ƿ������ʳָ��סƿ������һֻ����סƿ�ף�������ƿ������ת��Σ�ҡ�ȡ�
��3�����ݼ�����������ƽ��ȡNaOH���������Ϊ_______g����ʵ����������������ȷ��������ʱ���ӿ̶��ߣ���������ҺŨ��______0.1mol/L������ڡ���С�ڡ����ڡ�����
��4������18.4mol/L��Ũ����������ƣ������Ũ��������Ϊ____________mL��
���𰸡��٢ڢ� �ڢܢ� �� Ca2++2OH-+2HCO3-=CaCO3��+H2O+CO32- AC 500mL����ƿ���ձ��������� BCD 2.0g С�� 13.6
��������
��.�������ʵ����������ϵ���ʺͷǵ���ʵĸ�����������
��.(1)��������һ�����ʵ���Ũ�ȵ���Һʵ����Ҫ�IJ����ж���Ҫ���������������
(2)��������ƿ��ʹ�÷�����ע�������������ж���
(3)���ݹ�ʽm=nM=cvM�����㣻���ݶ���ʱ�۵�����Ҫ�Ͱ�Һ�����ʹ���ƽ������
(4)����ϡ��ǰ�����ʵ����������з��������㡣
��.�������ǽ������ʣ��ܵ��磬���ǼȲ��ǵ����Ҳ���Ƿǵ���ʣ����ۻ���KNO3�ܵ��磬���ڻ�������ڵ���ʣ����������ܵ��磬���ڵ��ʣ��Ȳ��ǵ����Ҳ���Ƿǵ���ʣ���NaCl���岻�ܵ��磬����ˮ������״̬���ܵ��磬���ڵ���ʣ���Һ̬�Ȼ��ⲻ�ܵ��磬����ˮ�ܵ��磬���ڵ�⣻��ʯ��ˮ�ܵ��磬���ڻ����Ȳ��ǵ����Ҳ���Ƿǵ���ʣ����Ҵ����ܵ��磬���ڷǵ���ʣ��ܵ���������Т٢ڢޣ����ڵ���ʵ��Тڢܢݣ����ڷǵ���ʵ��Тߣ�����ʯ��ˮ������̼��������Һ��Ӧ��Ca2++2OH-+2HCO3-=CaCO3��+2H2O+CO32-���ʴ�Ϊ���٢ڢ����ڢܢ�������Ca2++2OH-+2HCO3-=CaCO3��+2H2O+CO32-��
��.(1)����һ�����ʵ���Ũ�ȵ���Һ������������У�һ����������ƿ��������ƽ���ձ�������������ͷ�ιܡ���Ͳ���ò�����ƿ�ͷ�Һ©������ȱ�ٵ��������ձ�����������500mL����ƿ���ʴ�Ϊ��AC���ձ�����������500mL����ƿ��
(2)A������ƿ�ڲ������ӣ�ʹ������ƿǰ�����Ƿ�©ˮ����ȷ��B������ƿ��ˮϴ�������ô�����Һϴ�ӣ�����C������ƿ������Ϊϡ�ͺ��ܽ������������D������ƿ������Ϊϡ�ͺ��ܽ������������E����������ƿʹ��ʱ��ע�����ҡ������ƿ��Ӧ�øǺ�ƿ������ʳָ��סƿ������һֻ����סƿ�ף�������ƿ������ת��Σ�ҡ�ȣ���ȷ���ʴ�Ϊ��BCD��
(3)ʵ����û��450mL������ƿ��Ӧѡ��500mL������ƿ�����ƣ��ݹ�ʽm=nM=cvM=0.1mol/L��0.5L��40g/mol=2.0g��������ʱ���ӿ̶��ߣ���ʵ����Һ�������500mL��������Ũ��ƫС���ʴ�Ϊ��2.0g��С�ڣ�
(4)��Ũ��������ΪVmL��ϡ��ǰ������������������䣬��98%��1.84g/cm3V=0.5mol/L��0.50L��98g/mol�����V=13.6mL���ʴ�Ϊ��13.6��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)��ͼΪCO2���Ӿ���ṹ��һ���֣��۲�ͼ�Ρ���˵��ÿ�� CO2������Χ��________����֮�����ҵȾ�� CO2���ӣ��ýṹ��Ԫƽ��ռ��________��CO2���ӡ�

(2)��40 GPa��ѹ�£��ü��������ȵ�1800 Kʱ�����dzɹ��Ƶ�ԭ�Ӿ���ɱ�����ṹ��������SiO2ԭ�Ӿ������ƣ�����˵����ȷ����________��
A��ԭ�Ӿ���ɱ��������������������
B��ԭ�Ӿ���ɱ��кܸߵ��۵�ͷе�
C��ԭ�Ӿ���ɱ���Ӳ��С������������ĥ����
D��ԭ�Ӿ���ɱ���һ�������¿����������Ʒ�Ӧ
E��ÿĦ��ԭ�Ӿ���ɱ��к���4 mol C��O��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڷ�ɢϵ��˵������ȷ����(����)
A.���ܷ��������ЧӦ�ķ�ɢϵ���Ȼ�����Һ��ˮ��
B.���������(��������η۳�)�γ����ܽ��������ཡ����Σ������
C.����ķ�ɢ�����ӵ�ֱ��Ϊ1��10 nm
D.�Ȼ�����Һ��������������ı����������������ЧӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶����������������Ϊ2.0L�ĺ����ܱ������зֱ����һ������X��������Ӧ��pX(g) ![]() Y(g)+Z(g)������������±���ʾ��
Y(g)+Z(g)������������±���ʾ��
������� | �¶�(��) | ��ʼ���ʵ���(mol) | ƽ�����ʵ���(mol) | |
X(g) | Y(g) | Z(g) | ||
�� | 387 | 0.20 | 0.080 | 0.080 |
�� | 387 | 0.40 | 0.160 | 0.160 |
�� | T | 0.20 | 0.090 | 0.090 |
�ش��������⣺
��1�����������з�Ӧ��10min�ﵽƽ�⣬��ǰ10min��Y��ƽ����Ӧ����v(Y)=___________��������������������ʼʱX�ķ�Ӧ����v(X)��___________v(X)��(������������С��������������)��
��2����֪������ӦΪ���ȷ�Ӧ����T___________387(��������������С����)���ж�������___________��
��3����Ӧ����ʽ��X�Ļ�ѧ������p��ȡֵΪ___________����������X��ƽ��ת����Ϊ___________������ʼʱ���������г���0.1molX��0.15molY��0.10molZ����Ӧ����___________ (����������������)��Ӧ����������ж�������_____________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������A��B��Ħ������֮��Ϊ2��1����������ͬ�¡�ͬѹ��ͬ���ʱ�ķ��Ӹ�����ӦΪ��������
A.1��1
B.1��2
C.2��1
D.4��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ���ǣ� ��
A.1molH2O������Ϊ18g/mol
B.CH4��Ħ������Ϊ16g
C.3.01��1023��SO2���ӵ�����Ϊ32g
D.��״���£�1mol�κ����������Ϊ22.4L/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ���ǣ� ��
A.Ħ���ǹ��ʵ�λ�����߸�����������֮һ
B.���³�ѹ�£�11.2LCO2����������Ϊ0.5NA
C.H2SO4 ��Ħ������Ϊ98 g
D.6.02��1022��H2SO4���ӵ�����Ϊ9.8 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ��Ӧ������������ԭ��Ӧ����( )
A. CaCO3![]() CaO + CO2 �� B. 2NaOH +CO2
CaO + CO2 �� B. 2NaOH +CO2![]() Na2CO3+ H2O
Na2CO3+ H2O
C. NaOH+HCl==NaCl+H2O D. 2Al+Fe2O3![]() 2Fe+Al2O3
2Fe+Al2O3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ�����������һ��ֲ���к��п������õĻ�����M����֪M�ĺϳ�·������ͼ��ʾ:
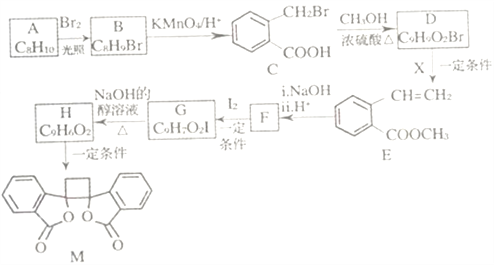
��֪:i.RCH2Br![]() R-HC=CH-R'��
R-HC=CH-R'��
ii.R-HC=CH-R'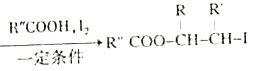 ��
��
iii.R-HC=CH-R'![]()
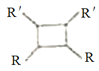 (����R��R'��R"�����⡢������)��
(����R��R'��R"�����⡢������)��
(1)A�Ļ�ѧ����Ϊ_______��D�����������ŵ�������______����H����M�ķ�Ӧ����Ϊ_____��
(2)�����Ƚ��ķ�������������������л���ṹ������
�ٿ�����_______(����ס���������ס��˴Ź�������)���C����Է���������
�ڲⶨB�Ľṹ:B�ĺ˴Ź���������ʾΪ_____��塣
(3)1molM������NaOH��Һ��Ӧ������_____molNaOH��
(4)X�ĽṹʽΪ_____��F�Ľṹ��ʽΪ______ ��
(5)��C����H�Ļ�ѧ����ʽΪ__________��
(6)��������������B��ͬ���칹�干______��(�����������칹)��
�ٷ����廯���� ����E������ͬ������ ���ܷ���������Ӧ ������������ˮ��������Ȼ�����Һ����ɫ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com