
【题目】I. 以下是实验室常用的部分仪器,请回答下列问题:
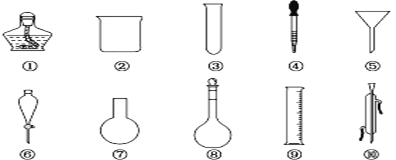
(1)序号为⑥和⑧的仪器的名称分别为__________________________。
(2)在分液操作中,必须用到上述仪器中的____________(填序号)。
(3)能作反应容器且可直接加热的仪器是上述中的____________(填名称)。
(4)配制一定物质的量浓度的溶液时要用到的仪器是________(填序号)。
(5)仪器上标有温度的有____________(填序号)。
II.(1)指出下列实验仪器和用品(已洗涤干净)使用时的第一步操作:
①淀粉碘化钾试纸检验Cl2的性质_____________________________;
②分液漏斗(分液)__________________________________________。
(2)下列有关实验的叙述中,合理的是________。
A.用碱式滴定管量取25.00 mL溴水
B.测定溶液的pH时用干燥、洁净的玻璃棒蘸取溶液,点在用蒸馏水湿润过的pH试纸上,再与标准比色卡比较
C.圆底烧瓶、锥形瓶、烧杯加热时都应垫上石棉网
D.使用容量瓶配制溶液时,俯视刻度线定容后所得溶液浓度偏高
E.滴定用的锥形瓶和滴定管都要用所盛溶液润洗
F.配制硫酸溶液时,可先在量筒内加入一定体积的水,再在搅拌下慢慢加入浓硫酸
G.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
【答案】分液漏斗 容量瓶 ②⑥ 试管 ②④⑧⑨ ⑧⑨ 用蒸馏水湿润试纸 检查是否漏水 CDG
【解析】
I. (1)序号为⑥和⑧的仪器的名称分别为:分液漏斗,容量瓶;综上所述,本题答案是:分液漏斗,容量瓶。
(2)分液是把两种互不混溶的液体分离开的操作方法。分液使用的仪器是分液漏斗,另外,分液还需要烧杯与铁架台进行辅助,故用到上述仪器中的②⑥;综上所述,本题答案是:②⑥。
(3)学过的可直接加热的仪器有:试管、蒸发皿、坩埚、燃烧匙,烧杯需要垫石棉网加热,试管可作为反应容器;综上所述,本题答案是:试管。
(4)一定物质的量浓度溶液的配制,所用仪器有托盘天平、药匙、量筒、胶头滴管、烧杯、玻璃棒,故选②④⑧⑨;综上所述,本题答案是:②④⑧⑨。
(5)容量瓶、量筒上标有温度,故选⑧⑨;综上所述,本题答案是:⑧⑨。
II.(1)①淀粉碘化钾试纸检验Cl2的性质时,应该先用蒸馏水润湿试纸再进行检验;因此,本题正确答案是:用蒸馏水润湿试纸。
②分液漏斗下端有玻璃旋塞,使用前应该检查分液漏斗的旋塞是否漏水;因此,本题正确答案是:检查是否漏水。
(2)A.溴水具有强氧化性,能够氧化碱式滴定管的橡胶管,应该使用酸式滴定管量取溴水,故A错误;
B.测定溶液的pH时,pH试纸不能够用蒸馏水湿润,否则导致溶液被稀释,影响测定结果,故B错误;
C.圆底烧瓶、锥形瓶、烧杯不能够直接加热,在加热时都应垫上石棉网,故C正确;
D.使用容量瓶配制溶液时,俯视刻度线定容,导致加入的蒸馏水体积偏小,所得溶液浓度偏高,故D正确;
E.滴定用的滴定管需要润洗,而锥形瓶不能够润洗,否则导致待测液物质的量偏大,测定结果偏高,故E错误;
F.量筒量取一定体积的浓硫酸,转移到盛有水的烧杯中,玻璃棒不断搅拌,冷却至室温;F错误;
G.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出,G正确;
综上所述,本题选CDG。


科目:高中化学 来源: 题型:
【题目】已知Al2H6燃烧热极高,是一种很好的生氢剂,它跟水反应生成H2,球棍模型如图(白球为Al,黑球为H)。下列推测肯定不正确的是
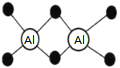
A. 该物质与水反应,属于氧化还原反应
B. Al2H6分子中氢为+1价,铝为﹣3价
C. Al2H6在空气中完全燃烧,产物为氧化铝和水
D. 氢铝化合物可能成为未来的储氢材料和火箭燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酯类是工业上重要的有机原料,具有广泛用途。乙酸苯甲酯![]() 对花香和果香的香韵具有提升作用,故常用于化妆品和食品工业。乙酸苯甲酯的合成路线如下:
对花香和果香的香韵具有提升作用,故常用于化妆品和食品工业。乙酸苯甲酯的合成路线如下:
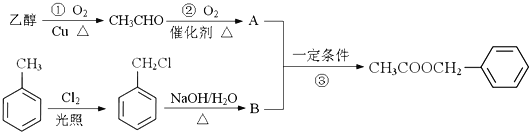
已知:R-Cl![]() R-OH,R-为烃基
R-OH,R-为烃基
(1)乙酸苯甲酯的分子式是________,B所含官能团的名称是________。
(2)写出反应③的化学反应方程式:________。反应①的反应类型是__________,反应③的反应类型是________________。
(3)下列转化中________(填序号)原子的理论利用率为100%,符合绿色化学的要求。
A.乙醇制取乙醛 B.由![]() 制备
制备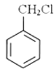 C.2CH3CHO+O2
C.2CH3CHO+O2![]() 2A
2A
(4)提纯乙酸苯甲酯的有关实验步骤如下:将反应液冷至室温后倒入分液漏斗中,分别用饱和碳酸钠溶液和水洗涤,分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏,收集馏分,得到乙酸苯甲酯。
回答下列问题:
①在洗涤、分液操作中。应充分振荡,然后静置,待分层后________(填标号)。
a.直接将乙酸苯甲酯从分液漏斗上口倒出
b.直按将乙酸苯甲酯从分液漏斗下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸苯甲酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸苯甲酯从上口放出
②实验中加入少量无水MgSO4的目的是__________________。
③在蒸馏操作中,仪器选择及安装都正确的是____________(填标号)。
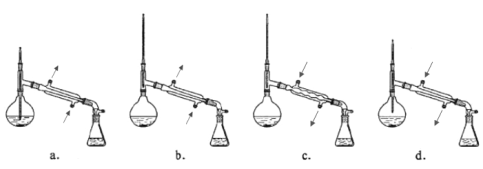
(注:箭头方向表示水流方向)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L容积不变的容器中,发生N2+3H2 ![]() 2NH3的反应。现通入4 mol H2和4 mol N2,10 s内用H2表示的反应速率为0.12 mol/(L·s),则10 s后容器中N2的物质的量是
2NH3的反应。现通入4 mol H2和4 mol N2,10 s内用H2表示的反应速率为0.12 mol/(L·s),则10 s后容器中N2的物质的量是
A. 1.6 mol B. 2.8 mol
C. 3.2 mol D. 3.6 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食品卫生与人们的身体健康密切相关,下列做法符合《食品卫生法》的是( )
A.用工业用盐腌制咸菜B.用小苏打发酵面粉
C.在牛奶中添加尿素D.用二氧化硫熏制银耳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学利用氯酸钾分解制氧气的反应,测定氧气的摩尔质量,实验步骤如下:
①把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量,质量为a g。
②装好实验装置。
③检查装置气密性。
④加热,开始反应,直到产生一定量的气体。
⑤停止加热(如图所示,导管出口高于液面)。
⑥测量收集到的气体的体积。
⑦准确称量试管和残留物的质量为b g。
⑧测量实验室的温度。
⑨把残留物倒入指定的容器中,洗净仪器,放回原处,把实验桌面收拾干净。
⑩处理实验数据,求出氧气的摩尔质量。

回答下列问题:
(1)如何检查装置的气密性? 。
(2)以下是测量收集到的气体体积必须包括的几个步骤:
①调整量筒内外液面高度使之相同;②使试管和量筒内的气体都冷却至室温;③读取量筒内气体的体积。这三步操作的正确顺序是 (请填写步骤代号)。
(3)测量收集到的气体体积时,如何使量筒内外液面的高度相同? 。
(4)如果实验中得到的氧气体积是c L(已换算为标准状况),水蒸气的影响忽略不计,氧气的摩尔质量的计算式为(含a、b、c,不必化简)M(O2)= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:
N2(g)+3H2(g)![]() 2NH3(g) △H=一92.6kJ/mol。实验测得起始、平衡时的有关数据如下表:
2NH3(g) △H=一92.6kJ/mol。实验测得起始、平衡时的有关数据如下表:
容器 | 起始各物质的物质的量/mol | 达平衡时体系能量的变化 | ||
N2 | H2 | NH3 | ||
① | 1 | 3 | 0 | 放出热量:23.15kJ |
② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
下列叙述不正确的是( )
A. 容器①、②中反应的平衡常数相等
B. 平衡时,两个容器中NH3的体积分数均为1/7
C. 容器②中达平衡时放出的热量Q=23.15kJ
D. 若容器①体积为0.5L,则平衡时放出的热量小于23.15kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下述实验中均有红棕色气体产生,对比分析所得结论不正确的是( )
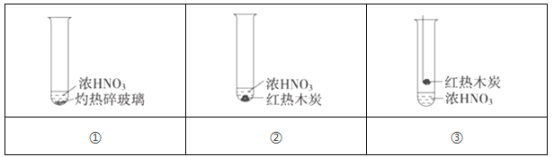
A. 由①中的红棕色气体,推断浓硝酸受热易分解,应保存在低温阴暗处
B. 红棕色气体不能表明②中木炭与浓硝酸发生了反应
C. 由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D. ③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com