
【题目】某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作步骤如下:
① 用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度以上
② 固定好滴定管并使滴定管尖嘴充满液体
④调节液面至“0”或“0”刻度线稍下,并记下读数
④移取20.00mL待测液注入洁净的锥形瓶中,并加入2滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数。
填空:(1)以上步骤有错误的是(填编号)_________,该错误操作会导致测定结果__________。(填“偏大”、“偏小”或“无影响”)
(2)步骤⑤中,在记录滴定管液面读数时,滴定管尖嘴有气泡,导致测定结果____________。(填“偏大”、“偏小”或“无影响”)
(3)判断滴定终点的现象是:___________________________________;
(4)如下图是某次滴定时的滴定管中的液面,其读数为_________mL

(5)根据下列数据:请计算待测盐酸溶液的浓度:_______________________mol·L-1
滴定次数 | 待测液体积(mL) | 标准烧碱体积(mL) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 20.00 | 0.40 | 20.40 |
第二次 | 20.00 | 4.00 | 24.00 |
第三次 | 20.00 | 2.00 | 24.10 |
【答案】① 偏大 偏小 当溶液恰好由无色变为粉红色且半分钟内不变色 22.60mL 0.2000 mol·L-1
【解析】
(1)滴定管水洗后需再用待装液润洗,否则会使滴定管中溶液浓度偏低,消耗溶液体积偏大,使测定结果偏大。
(2)若滴定前无气泡,滴定后有气泡,则溶液体积偏小,测定结果偏小。
(3)接近终点时,当滴加最后一滴溶液时,溶液变红且30s不褪色,即为终点。
(4)滴定管精确度为0.01mL,每一格表示1mL,图中读数为22.60mL。
(5)第一次和第二次消耗氢氧化钠溶液体积20.00mL,第三次消耗氢氧化钠溶液体积22.10mL,第三次数据应舍去。氢氧化钠溶液体积为20.00mL,氢氧化钠溶液浓度为0.2000mol·L-1,盐酸体积为20.00mL,由n(HCl)=n(NaOH)得盐酸浓度为0.2000 mol·L-1。


 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:
【题目】(1)下图中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择_____(填字母序号)。用电化学原理解释材料B需定期拆换的原因:________。
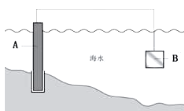
a.碳棒 b.锌板 c.铜板
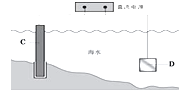
(2)下图,钢闸门C做__极。用氯化钠溶液模拟海水进行实验,D为石墨块,则D上的电极反应式为_______,检测该电极反应产物的方法是________。
(3)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。下图为“镁-次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
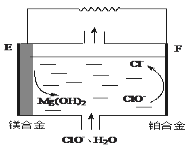
①E为该燃料电池的极___(填“正”或“负”)。F电极上的电极反应式为____。
②镁燃料电池负极容易发生自腐蚀产生氢气,使负极利用率降低,用化学用语(化学方程式)解释其原因__。
(4)乙醛酸(HOOC-CHO)是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图所示,该装置中阴、阳两极为惰性电极,两级室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。N级乙二酸直接反应生成乙醛酸。
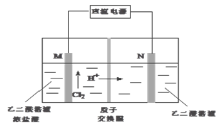
①N电极上的电极反应式为_________。
②若有2molH+通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在150℃,由任意比例组成的混合气体1L,在9L过量的氧气中充分燃烧后,恢复到反应前的温度,体积仍为10L,则该混合气体的成分可能是
A. C2H4和C3H4B. CH4和C2H6C. CH4和C2H2D. C2H6和C3H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校高一研究性学习小组将造成我省某市空气污染的主要原因分为以下四种:
A. 燃烧农作物秸秆 B.燃烧含硫煤 C.粉尘污染 D.机动车尾气污染
并就造成该市空气污染的最主要原因调查了该市100名市民和100位环保部门人士。调查结果如下图所示:
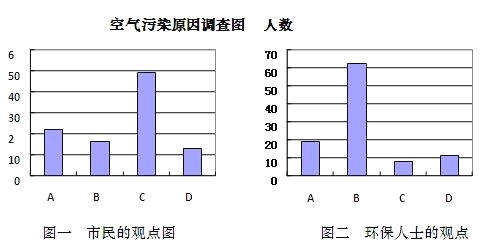
(1)调查结果显示:该市市民认为造成空气污染的最主要原因是___,环保人士认为造成该市空气污染的最主要原因是____。
(2)调查结果说明市民对造成空气污染的最主要原因认识不足。该最主要原因造成的大气污染的主要有害成分是_______,空气中该成分含量较高时,在空气中的氧气和水的共同作用下,会形成酸雾,其化学反应方程式为_________________________________
(3)下列措施能够减少空气中该成分排放量的是______________
①用天然气代替煤炭做民用燃料 ②改进燃烧技术,提高热能利用率 ③工厂生产时将燃煤锅炉的烟囱造得更高 ④燃煤中加入适量石灰石后使用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关铁的化合物的说法中,错误的是( )
A.Fe(OH)2是一种黑色固体,不稳定,在空气中易被氧化转变为红褐色
B.如图所示操作可制取Fe(OH)2
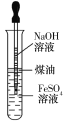
C.Fe3O4、Fe(OH)3都可以由化合反应制得
D.Fe(OH)3胶体呈红褐色、透明,能发生丁达尔效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“NaH2PO2还原法”制备高纯度氢碘酸和亚磷酸钠(Na2HPO3)的工业流程如图。
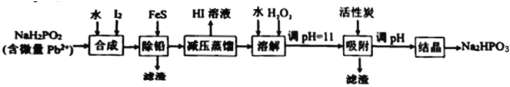
已知:25℃时,H3PO3的pKa1=1.3,pKa2=6.6。
(1)“合成”过程,主要氧化产物为H3PO3,相应的化学方程式为___________。
(2)“除铅”过程,FeS除去微量Pb2+的离子方程式为___________。
(3)“减压蒸馏”过程,I-回收率为95%,则剩余固体的主要成分为___________(填化学式)。
(4)“调pH=11”的作用是___________。
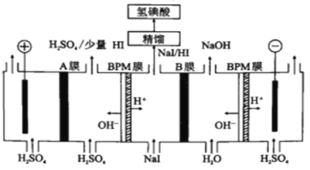
(5)氢碘酸也可以用“电解法”制备,装置如图所示。其中双极膜(BPM)是阴、阳复合膜,在直流电的作用下,阴、阳膜复合层间的H2O解离成H+和OH-;A、B为离子交换膜。
①B膜最佳应选择___________
②阳极的电极反应式是___________。
③少量的I-因为浓度差通过BPM膜,若撤去A膜,其缺点是:___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.4L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题:

(1)该混合液中,NaCl的物质的量为__mol,含溶质MgCl2的质量为__g。
(2)该混合液中CaCl2的物质的量为__mol,将该混合液加水稀释至体积为1L,稀释后溶液中Ca2+的物质的量浓度为__mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氧化还原反应的叙述正确的是( )
A.化学反应中电子转移的表示方法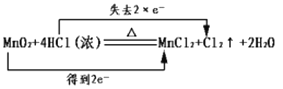
B.离子M2O7x-与S2-能在酸性溶液中发生如下反应:M2O7x-+3S2-+14H+=2M3+ +3S +7H2O,则M2O7x-中M的化合价为+7
C.在常温下发生以下几个反应:①16H++10Z-+2XO4-=2X2++5Z2+8H2O②2A2++B2=2A3++2B-③2B-+Z2 =B2+2Z-根据上述反应,可知道氧化性强弱顺序为:XO4->Z2>B2>A3+
D.已知硝酸铵在一定温度下分解为5NH4NO3=4N2↑+2HNO3+9H2O↑,被氧化的元素和被还原的元素的质量之比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,水存在如下电离:H2O![]() H++OH- H>0,下列叙述正确的是
H++OH- H>0,下列叙述正确的是
A.向水中滴入少量稀盐酸,平衡逆向移动,Kw减小
B.将水加热,Kw增大,pH减小
C.向水中加入少量固体NH4Cl,平衡逆向移动,c(H+)降低
D.向水中加入少量固体硫酸钠,c(H+)=10-7mol/L,Kw不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com